PAM คือรอยโรคสีแบนที่ได้มาของเยื่อบุตา จากการเพิ่มจำนวนของเมลาโนไซต์ผิดปกติ แตกต่างจากปานตรงที่ไม่มีส่วนนูนแบ่งเป็นชนิดไม่มี atypia (ไม่ร้าย) และมี atypia (รอยโรคก่อนมะเร็ง)
ประมาณ 25-50% ของ PAM ที่มี atypia เปลี่ยนเป็นมะเร็งผิวหนังชนิดเมลาโนมาที่เยื่อบุตา
ประมาณ 60-75% ของมะเร็งผิวหนังชนิดเมลาโนมาที่เยื่อบุตา มีต้นกำเนิดจาก PAM
มีลักษณะ “เพิ่มขึ้นและลดลง” การหายไปของสีไม่ได้หมายถึงการหายขาด
การตัดชิ้นเนื้อ (map biopsy) เพื่อยืนยันการมี atypia และกำหนดแผนการรักษา
การติดตามผลอย่างสม่ำเสมอเป็นสิ่งจำเป็นเพื่อตรวจพบการเปลี่ยนแปลงเป็นมะเร็งตั้งแต่ระยะแรก
ภาวะเมลาโนซิสที่ได้มาปฐมภูมิ (primary acquired melanosis, PAM ) คือรอยโรคที่ได้มาของเยื่อบุตา มีลักษณะเป็นรอยสีน้ำตาลดำเป็นหย่อมๆ จากการเพิ่มจำนวนของเมลาโนไซต์ผิดปกติ สามารถเกิดได้ทุกส่วนของเยื่อบุตา ต่างจากปานตรงที่เป็นรอยโรคสีแบนไม่มีส่วนนูน
นอกจาก PAM ปฐมภูมิที่ไม่มีสาเหตุชัดเจนแล้ว การมีสีอาจเกิดจากการอักเสบเรื้อรัง เช่น โรคภูมิแพ้ การระคายเคืองจากเครื่องสำอางหรือสารเคมี หรือหลังการผ่าตัด (เมลาโนซิสทุติยภูมิ) PAM หมายถึงรอยโรคปฐมภูมิที่ไม่มีสาเหตุทุติยภูมิเหล่านี้
Q
PAM เป็นมะเร็งหรือไม่?
A
PAM เองไม่จำเป็นต้องเป็นมะเร็ง PAM ที่ไม่มี atypia เป็นชนิดไม่ร้าย มีความเสี่ยงต่ำในการเปลี่ยนเป็นมะเร็ง ในขณะที่ PAM ที่มี atypia เป็นรอยโรคก่อนมะเร็งที่เปลี่ยนเป็นมะเร็งผิวหนังชนิดเมลาโนมาที่เยื่อบุตา ในประมาณ 25-50% ของกรณี การยืนยันการมี atypia โดยการตัดชิ้นเนื้อเป็นสิ่งสำคัญ
PAM แบ่งออกเป็นสองกลุ่มหลักตามการมี atypia ทางเนื้อเยื่อวิทยา ในระยะหลัง เรียกอีกอย่างว่ารอยโรคเมลาโนไซต์ในเยื่อบุผิวเยื่อบุตา (conjunctival melanocytic intraepithelial lesion, C-MIL) และได้รับการจัดระเบียบใหม่ในการจำแนกของ WHO3)
การจำแนก PAM C-MIL ที่สอดคล้อง ความเสี่ยงในการเปลี่ยนเป็นมะเร็ง PAM ที่ไม่มีภาวะ atypiaC-MIL ระดับต่ำ ต่ำ (เปลี่ยนเป็นมะเร็งได้น้อย) PAM ที่มี atypia เล็กน้อยC-MIL ระดับปานกลาง ปานกลาง PAM ที่มี atypia รุนแรงC-MIL ระดับสูง / melanoma in situ ประมาณ 25-50%
คะแนน C-MIN 5 ขึ้นไปถือเป็น melanoma in situ และต้องได้รับการรักษาที่รุกมากขึ้น2) .
คิดเป็น 11% ของรอยโรคเยื่อบุตา ทั้งหมด2) พบมากที่สุดในคนผิวขาววัยกลางคนขึ้นไป และมักเป็นข้างเดียว ประมาณ 60-75% ของมะเร็งผิวหนังชนิดร้ายของเยื่อบุตา มี PAM เป็นรอยโรคก่อนหน้า ดังนั้นจึงถือเป็นรอยโรคก่อนมะเร็งที่สำคัญ อุบัติการณ์ในคนเอเชียต่ำกว่าคนผิวขาว
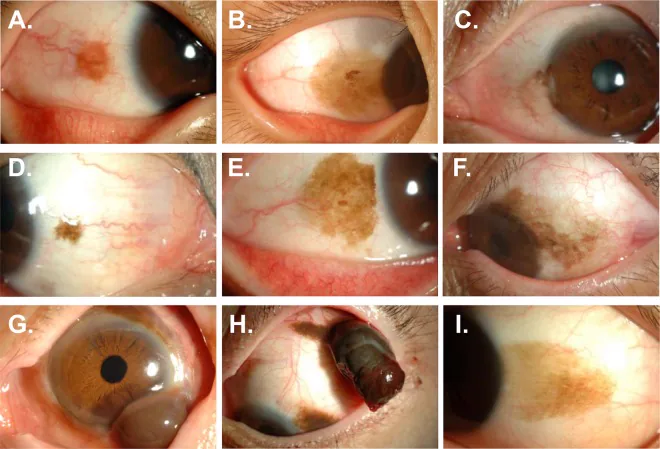
ภาพถ่ายส่วนหน้าของรอยโรคที่มีเม็ดสีของเยื่อบุตาตามการจำแนกทางจุลพยาธิวิทยา รวมถึง PAM ที่ไม่มี atypia (D, E) และ PAM ที่มี atypia (F) Kocaturk T, et al. Anterior segment photography of conjunctival pigmented lesions according to histological classification. Sci Rep. 2019;9:18204. Figure 2. PM
CI D: PMC6890774. License: CC BY.
ภาพถ่ายส่วนหน้าของรอยโรคที่มีเม็ดสีของเยื่อบุตา ตามการจำแนกทางจุลพยาธิวิทยา D และ E แสดง PAM ที่ไม่มี atypia (เม็ดสีแบนสีน้ำตาลอ่อนถึงน้ำตาลเข้มเป็นจุดๆ) F แสดง PAM ที่มี atypia สอดคล้องกับรูปแบบของ PAM และการจำแนก atypia ที่กล่าวถึงในหัวข้อ “2. อาการหลักและผลการตรวจทางคลินิก”
การปรากฏหรือเพิ่มขึ้นของรอยโรคที่มีเม็ดสีที่เยื่อบุตา
ในหลายกรณี ดำเนินไปโดยไม่มีอาการ
ปัญหาด้านความสวยงามมักเป็นแรงจูงใจในการมาพบแพทย์
ลักษณะของเม็ดสี : เม็ดสีเป็นจุดด่างจากสีน้ำตาลอ่อนถึงสีน้ำตาลเข้ม แสดงสีที่หลากหลายการมีหรือไม่มีนูน : แบน ไม่นูน นี่เป็นจุดสำคัญในการแยกความแตกต่างจากเนวัสและเมลาโนมาการกระจาย : สามารถเกิดได้ทุกส่วนของเยื่อบุตา อาจกระจายแบบต่อเนื่องหรือไม่ต่อเนื่องข้างเดียว : มักเกิดข้างเดียวการพลิกหนังตา : รอยโรคอาจซ่อนอยู่ในฟอร์นิกซ์หรือเยื่อบุตา หนังตา ดังนั้นการประเมินโดยการพลิกหนังตาจึงจำเป็น
เป็นลักษณะเฉพาะของ PAM คือปรากฏการณ์ “wax and wane” ที่เม็ดสีเพิ่มขึ้นและลดลงซ้ำๆ2) แม้ว่าเม็ดสีจะจางลงหรือหายไป รอยโรคเองก็ไม่ได้หายไป หากมองข้ามจุดนี้ อาจเข้าใจผิดว่าหายขาดและละเลยการติดตามผล
Q
ถ้าเม็ดสีจางลง แสดงว่าหายแล้วหรือ?
A
ไม่ใช่ PAM แสดงคลื่นของการเพิ่มขึ้นและลดลงที่เรียกว่า “wax and wane” แม้ว่าเม็ดสีจะจางลง รอยโรคก็ไม่ได้หายไป และทางพยาธิวิทยามักมีรอยโรคหลงเหลืออยู่ เช่นเดียวกันหลังการรักษาด้วยไมโตมัยซินซี หลังจากเม็ดสีหายไป จำเป็นต้องยืนยันการกำจัดด้วยการตัดชิ้นเนื้อแบบแผนที่
หากเกิดการเปลี่ยนแปลงดังต่อไปนี้ ควรไปพบแพทย์ผู้เชี่ยวชาญทันทีและพิจารณาตรวจชิ้นเนื้อ:
ขยายตัวอย่างรวดเร็ว
เกิดรอยนูน (ก้อน) ขึ้นบนรอยโรคที่เคยราบเรียบ
ปรากฏหลอดเลือดของเนื้องอก (feeder vessels)
PAM มักไม่มีอาการแสดงให้รู้สึก และมีแนวโน้มที่เม็ดสีจะเพิ่มขึ้นและลดลงสลับกัน การตรวจตาเป็นประจำพร้อมบันทึกภาพถ่ายช่วยให้เห็นการเปลี่ยนแปลงอย่างเป็นกลาง ซึ่งนำไปสู่การตรวจพบการเปลี่ยนเป็นมะเร็งได้ตั้งแต่ระยะแรก หากมีรอยโรคเม็ดสีใหม่เกิดขึ้น หรือรอยโรคเม็ดสีเดิมมีขนาดใหญ่ขึ้นหรือนูนขึ้น ควรรีบไปพบแพทย์
สาเหตุโดยตรงของการเกิด PAM ยังไม่ชัดเจน แต่มีพื้นฐานมาจากการเพิ่มจำนวนผิดปกติของเมลาโนไซต์ภายในเยื่อบุผิว แตกต่างจากเมลาโนซิสทุติยภูมิ (ที่จะกล่าวถึงต่อไป) ซึ่งเกิดขึ้นโดยไม่มีปัจจัยภายนอกที่จำเพาะ
ความผิดปกติของเนื้อเยื่อ : PAM ที่มีความผิดปกติของเซลล์เป็นปัจจัยเสี่ยงสูงสุด โดยเฉพาะความผิดปกติระดับรุนแรง (คะแนน C-MIN 5 ขึ้นไป) มีอัตราการเปลี่ยนเป็นมะเร็งสูงขอบเขตของรอยโรค : รอยโรคที่กว้างอาจมีความเสี่ยงสูงขึ้นการกลายพันธุ์ของโปรโมเตอร์ TERT : ตรวจพบใน PAM ที่มีความผิดปกติระดับปานกลางถึงรุนแรง และบ่งชี้ลักษณะของมะเร็งผิวหนังชนิดเมลาโนมาในระยะเริ่มต้น 2)
รอยโรคเม็ดสีที่มีสาเหตุดังต่อไปนี้ไม่ใช่ PAM แต่จัดเป็นเมลาโนซิสทุติยภูมิ:
การอักเสบเรื้อรัง เช่น โรคภูมิแพ้
การระคายเคืองจากเครื่องสำอางหรือสารเคมี
การสร้างเม็ดสีหลังการผ่าตัด
การสร้างเม็ดสีจากยา
เยื่อบุตา สัมผัสกับรังสีอัลตราไวโอเลตโดยตรง ดังนั้นการได้รับรังสียูวีจึงถือเป็นปัจจัยเสี่ยงประการหนึ่ง สาเหตุที่พบบ่อยในคนผิวขาวคือมีเมลานินน้อยและประสิทธิภาพการกรองรังสียูวีต่ำ
ขั้นแรก ประเมินรูปร่าง สี ขอบเขต และการมีอยู่ของรอยโรคที่นูนขึ้นมาอย่างละเอียดด้วยกล้องจุลทรรศน์ชนิดกรีด ต้องพลิกเปลือกตาเสมอเพื่อตรวจหารอยโรคในฟอร์นิกซ์และเยื่อบุตา ส่วนเปลือกตา
OCT ส่วนหน้าสามารถประเมินความลึกของรอยโรคและการจำกัดอยู่ภายในเยื่อบุผิว รอยโรคจะปรากฏเป็นรอยโรคที่มีการสะท้อนแสงสูง
เนื่องจาก PAM มีรูปแบบ “wax and wane” การบันทึกภาพถ่ายเป็นระยะตั้งแต่การตรวจครั้งแรกจึงเป็นพื้นฐานของการติดตามผล การเปลี่ยนแปลงของการกระจายของเม็ดสีจะถูกติดตามอย่างเป็นกลาง
นี่คือมาตรฐานทองคำสำหรับการวินิจฉัยที่แน่นอนของ PAM และการกำหนดแผนการรักษา
Q
Map biopsy (การตัดชิ้นเนื้อแบบแผนที่) คือการตรวจอะไร?
A
Map biopsy (การตัดชิ้นเนื้อแบบแผนที่) เป็นขั้นตอนการตัดชิ้นเนื้อซึ่งเก็บรอยโรคที่มีเม็ดสีของเยื่อบุตา อย่างเป็นระบบจากหลายตำแหน่ง โดยการทำแผนที่การกระจายของเซลล์ผิดปกติทั่วรอยโรค ทำให้สามารถระบุขอบเขตและระดับของความผิดปกติได้อย่างแม่นยำ การมีอยู่และระดับของความผิดปกติเป็นข้อมูลที่สำคัญที่สุดในการกำหนดแผนการรักษา (การสังเกตหรือการตัดออก)
PAM without atypiaPAM with atypia
การประเมินเครื่องหมายด้วยอิมมูโนฮิสโตเคมีมีประโยชน์สำหรับการวินิจฉัยที่แน่ชัดและการแยกความแตกต่างระหว่างชนิดไม่ร้ายแรงและร้ายแรง3) .
เครื่องหมาย ความสำคัญ หมายเหตุ PRAM E เครื่องหมายบ่งชี้ความร้ายแรงที่แข็งแกร่งที่สุด ให้ผลบวกใน PAM with atypia / มะเร็งผิวหนังเมลาโนมา1) Ki-67 ดัชนีการเพิ่มจำนวน ค่าสูงบ่งชี้ถึงความร้ายแรง p16 ยับยั้งเนื้องอก การหายไปบ่งชี้ถึงความร้ายกาจ1) S100, SOX10, HMB45 ร่วมกันของเซลล์เมลาโนไซต์ ไม่สามารถใช้แยกชนิดไม่ร้ายและร้ายได้
เนวัสเยื่อบุตา : นูน มีถุงน้ำคล้ายไข่มุก เกิดแต่กำเนิดถึงวัยหนุ่มสาวมะเร็งเมลาโนมาของเยื่อบุตา : นูนเป็นก้อน มีหลอดเลือดเนื้องอก มีแนวโน้มโตเร็วเมลาโนซิสทุติยภูมิ : มีสาเหตุชัดเจน เช่น การอักเสบ ยา เครื่องสำอางการสร้างเม็ดสีตามเชื้อชาติ : เป็นสองข้างและสมมาตร การกระจายตัวทั่วไปที่ลิมบัส และเยื่อบุตา ลูกตา
แนวทางการรักษา PAM ขึ้นอยู่กับการมีและระดับของ atypia ทางเนื้อเยื่อวิทยา
PAM ที่ไม่มี atypia
แนวทาง : สังเกตอาการ
เนื้อหา : ตรวจด้วยกล้องจุลทรรศน์ชนิดกรีด (slit-lamp) และบันทึกภาพถ่ายอย่างสม่ำเสมอต่อไป
ความถี่ : แนะนำให้มาตรวจทุก 3-6 เดือน
การพิจารณาตัดออก : หากมีปัญหาด้านความสวยงามหรือมีการเปลี่ยนแปลงระหว่างการติดตามผล ให้ทำการตัดออกและตรวจทางพยาธิวิทยา
PAM ร่วมกับ atypia
แนวทาง : การรักษาเชิงรุก
atypia เล็กน้อย : ตัดออก ± จี้เย็น
atypia รุนแรง (melanoma in situ) : ตัดออกกว้าง + จี้เย็น + การรักษาเฉพาะที่ด้วย MMC
ร่วมกัน : ติดตามผลเป็นระยะในทุกราย (ตรวจพบการเปลี่ยนแปลงเป็นมะเร็งระยะแรก)
การตัดออก : ตัดออกบริเวณที่สงสัย ทำการตรวจทางพยาธิวิทยาเพื่อแยกมะเร็งการจี้เย็น การจี้เย็น ด้วยวิธี double freeze-thaw ที่ขอบและฐานของรอยตัดเพื่อลดความเสี่ยงของรอยโรคที่เหลืออยู่
เคมีบำบัดเฉพาะที่ทำใน PAM ร่วมกับ atypia ที่ยืนยันทางจุลพยาธิวิทยา
ข้อบ่งชี้ : เฉพาะรอยโรคที่จำกัดอยู่ภายในเยื่อบุผิว (ไม่เหมาะสมสำหรับ melanoma ที่ลุกลาม)วิธีการ : ยาหยอดตา Mitomycin C 0.02% 5 ครั้ง/วัน นาน 1 สัปดาห์ หลายรอบ2) ข้อควรระวัง : ผลข้างเคียง ได้แก่ ความเสียหายต่อเซลล์ต้นกำเนิดลิมบัส (สูงถึง 12%), การตีบของจุดน้ำตา, และต้อกระจก
เป็นทางเลือกแทนไมโตมัยซิน C โดยใช้ IFNα-2b ทาเฉพาะที่ ข้อดีเหนือ MMC คือไม่ทำให้เกิดความเสียหายต่อเซลล์ต้นกำเนิดลิมบัส
เนื่องจากลักษณะ “wax and wane” ของ PAM การหายไปของเม็ดสีหลังการรักษาไม่ได้หมายความว่ารอยโรคถูกกำจัดแล้ว หลังการรักษาด้วยไมโตมัยซิน C จำเป็นต้องยืนยันการกำจัด PAM ทางจุลพยาธิวิทยาด้วยการตัดชิ้นเนื้อแบบแผนที่ การหยุดการติดตามอาจทำให้พลาดการเปลี่ยนแปลงเป็นมะเร็ง ดังนั้นการมาติดตามอย่างต่อเนื่องจึงสำคัญ
Q
จำเป็นต้องผ่าตัดทันทีเมื่อได้รับการวินิจฉัย PAM หรือไม่?
A
ไม่จำเป็นเสมอไป หากเป็น PAM without atypia (ไม่มี atypia) การติดตามเป็นระยะเป็นแนวทางพื้นฐาน ในทางกลับกัน PAM with atypia (มี atypia) เป็นรอยโรคก่อนมะเร็ง ดังนั้นจึงแนะนำให้รักษาอย่างจริงจัง เช่น การตัดออกหรือเคมีบำบัดเฉพาะที่ ขั้นตอนมาตรฐานคือการตรวจหา atypia โดยการตัดชิ้นเนื้อก่อนตัดสินใจแผนการรักษา
สาระสำคัญของ PAM คือการเพิ่มจำนวนผิดปกติของเมลาโนไซต์ภายในเยื่อบุตา ระยะที่ไม่มีการลุกลามเข้าไปในเนื้อเยื่อใต้เยื่อบุเรียกว่ารอยโรค “ภายในเยื่อบุ” และเมื่อเกิดการลุกลาม จะได้รับการวินิจฉัยว่าเป็นมะเร็งเมลาโนมา
ในแนวคิดสมัยใหม่ PAM ถูกเข้าใจว่าเป็นสเปกตรัมของรอยโรคเมลาโนไซต์ภายในเยื่อบุตา (C-MIL) 3)
เมลาโนซิสชนิดไม่ร้าย → C-MIL ระดับต่ำ → C-MIL ระดับสูง → melanoma in situ → melanoma ที่ลุกลาม
มีสเปกตรัมนี้ และ PAM with atypia สอดคล้องกับ C-MIL ระดับปานกลางถึงสูง
มีการรายงานการกลายพันธุ์ของโปรโมเตอร์ TERT (c.-124C>T) เกี่ยวข้องกับการเปลี่ยนเป็นมะเร็งจาก PAM ที่มี atypia 2) การกลายพันธุ์นี้กระตุ้น telomerase reverse transcriptase ส่งเสริมการทำให้เซลล์เป็นอมตะและการเปลี่ยนเป็นมะเร็ง นอกจากนี้ยังแสดงความสัมพันธ์กับภาระการกลายพันธุ์ของเนื้องอกที่สูง
PAM คิดเป็นประมาณ 60-75% ของต้นกำเนิดของมะเร็งผิวหนังชนิดเมลาโนมาชนิดร้ายของเยื่อบุตา ซึ่งบ่งชี้ว่า PAM สามารถลุกลามเป็นมะเร็งผิวหนังชนิดเมลาโนมาชนิดร้ายที่แพร่กระจายได้หากปล่อยทิ้งไว้หรือถูกมองข้าม ยืนยันความสำคัญของการวินิจฉัยตั้งแต่เนิ่นๆ และการจัดการที่เหมาะสม
การกำหนดมาตรฐานสากลของระบบการจำแนกประเภท C-MIL และคะแนน C-MIN กำลังดำเนินการอยู่ 3) คาดว่าจะช่วยเพิ่มความสามารถในการทำซ้ำในการวินิจฉัยระหว่างนักพยาธิวิทยา และเพิ่มความแม่นยำในการเลือกการรักษาตามระดับของ atypia
ชุดอิมมูโนฮิสโตเคมีที่รวมเครื่องหมาย เช่น PRAM E, p16 และ Ki-67 กำลังทำให้สามารถจำแนกประเภทใหม่ของรอยโรคที่ก่อนหน้านี้ถือว่า “ไม่แน่นอน” 1) ซึ่งอาจช่วยให้สามารถระบุความจำเป็นและเวลาของการตัดชิ้นเนื้อได้แม่นยำยิ่งขึ้น
เทคโนโลยีการติดตามแบบไม่รุกล้ำโดยใช้ OCT ส่วนหน้าและกล้องจุลทรรศน์คอนโฟคอล ในร่างกายกำลังได้รับการพัฒนา คาดว่าจะเป็นวิธีการประเมินความก้าวหน้าของ PAM แบบเรียลไทม์โดยไม่ต้องตัดชิ้นเนื้อ
Eder และคณะ (2024) แสดงให้เห็นว่าใน 5 กรณีของรอยโรคการเพิ่มจำนวนของเมลาโนไซต์ที่เยื่อบุตา ผิดปกติซึ่งประเมินได้ยากด้วยการตรวจทางจุลพยาธิวิทยาทั่วไป สามารถจำแนกประเภทใหม่ได้โดยใช้ชุดอิมมูโนฮิสโตเคมี (PRAM E, p16, HMB45, Ki-67 ฯลฯ) และการวิเคราะห์ FISH 1) นอกจากนี้ยังมีการชี้ให้เห็นถึงความเป็นไปได้ในการแยกความแตกต่างระหว่างชนิดไม่ร้ายและร้ายด้วยการวิเคราะห์ microRNA
การวิจัยกำลังดำเนินการเกี่ยวกับการทำโปรไฟล์โมเลกุล รวมถึงการกลายพันธุ์ของโปรโมเตอร์ TERT เพื่อทำนายความเสี่ยงของการเปลี่ยน PAM เป็นเมลาโนมาเป็นรายบุคคล 2) กลยุทธ์การรักษาเฉพาะบุคคลโดยอาศัยการประเมินความเสี่ยงระดับโมเลกุลคาดว่าจะเป็นไปได้ในอนาคต
Eder A, Milman T, Mudhar HS , et al. Unusual conjunctival melanocytic proliferations: report of five cases and review of the literature. Surv Ophthalmol. 2024; PMC12208716.
Goemaere J, Lauwers N, de Keizer ROB, et al. Bone metastasis in a case of primary acquired melanosis with atypia resulting from conjunctival melanoma. Am J Ophthalmol Case Rep. 2023; PMC9763362.
Englisch CN, Berger T, Flockerzi F, et al. Conjunctival melanoma with pronounced central corneal invasion: one-year relapse free follow-up. Am J Ophthalmol Case Rep. 2024; PMC11403272.
ถาม AI เกี่ยวกับบทความนี้
คัดลอกข้อความบทความแล้ววางในผู้ช่วย AI ที่คุณต้องการใช้
เปิดผู้ช่วย AI ด้านล่าง แล้ววางข้อความที่คัดลอกลงในช่องแชต