PAM without atypia

原発性後天性メラノーシス(PAM)
ひとめでわかるポイント
Section titled “ひとめでわかるポイント”1. 原発性後天性メラノーシス(PAM)とは
Section titled “1. 原発性後天性メラノーシス(PAM)とは”原発性後天性メラノーシス(primary acquired melanosis, PAM)は、メラノサイトの異常増殖によって斑紋状の黒褐色色素沈着を呈する後天性の結膜病変である。結膜のどの部位にも発生しうる。母斑(nevus)と異なり、隆起を伴わない平坦な色素病変であることが特徴である。
特に原因を持たない原発性後天性メラノーシスのほか、アレルギー疾患などの慢性炎症、化粧品や化学物質による刺激、あるいは手術後などに色素が沈着する場合もある(二次性メラノーシス)。PAMはこれら二次性の原因を持たない原発性の病変を指す。
PAM自体は必ずしも悪性ではない。PAM without atypia(異型なし)は良性で悪性転化リスクは低い。一方、PAM with atypia(異型あり)は約25〜50%が結膜悪性黒色腫に転化する前がん病変である。異型の有無を生検で確認することが重要である。
PAMの病理学的分類
Section titled “PAMの病理学的分類”PAMは組織学的な異型の有無により大きく2群に分類される。近年は結膜メラノサイト上皮内病変(conjunctival melanocytic intraepithelial lesion, C-MIL)とも呼ばれ、WHO分類でも再整理されている3)。
| PAM分類 | 対応するC-MIL | 悪性転化リスク |
|---|---|---|
| PAM without atypia(異型なし) | 低悪性度C-MIL | 低い(稀に転化) |
| PAM with atypia・軽度 | 中等度悪性度C-MIL | 中程度 |
| PAM with atypia・高度 | 高悪性度C-MIL / melanoma in situ | 約25〜50% |
C-MINスコア5以上はmelanoma in situと見なされ、より積極的な治療が必要となる2)。
全結膜病変の11%を占める2)。中年以降の白人に最も多く発症し、ほぼ常に片側性である。結膜悪性黒色腫の約60〜75%がPAMを前駆病変とするため、前がん病変として特に重要視される。東洋人では白人と比べて発症頻度が低い。
2. 主な症状と臨床所見
Section titled “2. 主な症状と臨床所見”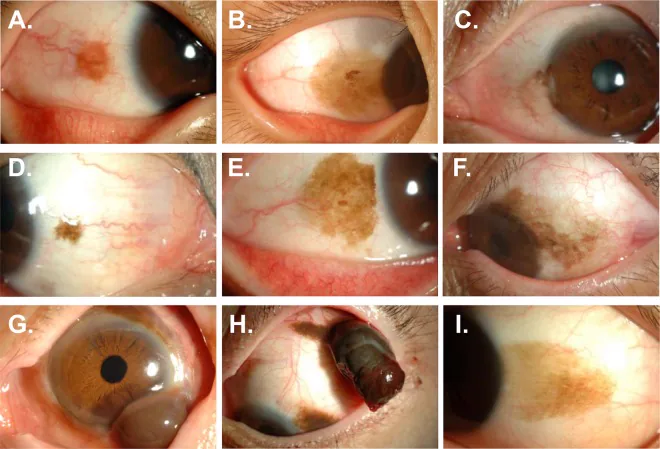
- 結膜の色素性病変の出現、または増大
- 多くの場合、無症状のまま経過する
- 整容的な問題が受診動機となることが多い
臨床所見(医師が診察で確認する所見)
Section titled “臨床所見(医師が診察で確認する所見)”- 色素沈着の形態:淡褐色〜濃褐色の斑紋状色素沈着。多様な色調を呈する。
- 隆起の有無:平坦で隆起を伴わない。これが母斑・メラノーマとの重要な鑑別点である。
- 分布:結膜のどの部位にも発生。連続または非連続性に広がることがある。
- 片側性:通常、片側性で発症する。
- 眼瞼翻転:円蓋部・眼瞼結膜に病変が隠れることがあるため、眼瞼翻転による評価が不可欠である。
「wax and wane」について
Section titled “「wax and wane」について”PAMの特徴的な経過として、色素沈着が増減を繰り返す「wax and wane」現象がある2)。色素が薄くなったり消失したりしても、病変そのものが消失したわけではない。この点を見落とすと、治癒したと誤解して経過観察を怠るリスクがある。
そうではない。PAMは「wax and wane」と呼ばれる増減の波を示す。色素が薄くなっても病変が消失したわけではなく、病理学的に病変が残存していることが多い。マイトマイシンC治療後も同様であり、色素消失後にマッピング生検で根絶を確認する必要がある。
悪性化を示唆する所見
Section titled “悪性化を示唆する所見”以下の変化が生じた場合は速やかに専門医を受診し、生検を検討する:
- 急速な拡大
- 平坦だった病変に隆起(結節形成)が生じる
- 腫瘍血管(feeder vessels)の出現
3. 原因とリスク要因
Section titled “3. 原因とリスク要因”PAMの原因
Section titled “PAMの原因”PAMの直接的な発生原因は明確ではないが、メラノサイトの上皮内における異常増殖が基盤にある。二次性メラノーシス(後述)と異なり、特定の外因なしに発症する。
悪性転化のリスク因子
Section titled “悪性転化のリスク因子”- 組織学的異型:PAM with atypiaであることが最大のリスク。特に高度異型(C-MINスコア5以上)では悪性転化率が高い。
- 病変の範囲:広範な病変ほどリスクが高い可能性がある。
- TERTプロモーター変異:PAMの中等度〜重度異型で検出され、melanoma in situとしての性質を示唆する2)。
二次性メラノーシスとの鑑別
Section titled “二次性メラノーシスとの鑑別”以下の誘因を持つ色素病変はPAMではなく、二次性メラノーシスとして区別する:
- アレルギー疾患などの慢性炎症
- 化粧品・化学物質による刺激
- 手術後の色素沈着
- 薬剤性色素沈着
紫外線との関連
Section titled “紫外線との関連”結膜は紫外線に直接曝露されるため、紫外線曝露がリスク要因の一つとして考えられている。白人に多い理由として、メラニン量が少なく紫外線フィルター効果が小さいことが挙げられる。
4. 診断と検査方法
Section titled “4. 診断と検査方法”細隙灯顕微鏡検査
Section titled “細隙灯顕微鏡検査”まず細隙灯顕微鏡で病変の形態・色調・境界・隆起の有無を詳細に評価する。眼瞼翻転を必ず行い、円蓋部・眼瞼結膜の病変を確認する。
前眼部光干渉断層計(AS-OCT)
Section titled “前眼部光干渉断層計(AS-OCT)”前眼部OCTにより病変の深達度と上皮内限局性を評価できる。過反射性病変として描出される。
PAMは「wax and wane」を示すため、初診時から定期的な写真記録が経過観察の基本となる。色素分布の変化を客観的に追跡する。
Map biopsy(マッピング生検)
Section titled “Map biopsy(マッピング生検)”PAMの確定診断と治療方針決定のゴールドスタンダードである。
Map biopsy(マッピング生検)とは、結膜の色素病変を複数の部位から系統的に採取する生検手技である。病変全体の異型分布をマッピングすることで、異型の範囲・程度を正確に把握できる。異型の有無・程度が治療方針(経過観察か切除か)を決定する最重要情報となる。
組織学的所見
Section titled “組織学的所見”- PAM without atypia:上皮基底層の最小限のメラノサイト増殖
- PAM with atypia:異型メラノサイトの孤立/融合巣、パジェット様進展、大型異常細胞、明瞭な核小体、高い核細胞質比、核分裂像
免疫組織化学マーカー
Section titled “免疫組織化学マーカー”免疫組織化学によるマーカー評価が確定診断と良悪性の鑑別に有用である3)。
| マーカー | 意義 | 備考 |
|---|---|---|
| PRAME | 最有力な悪性化マーカー | PAM with atypia / メラノーマで陽性1) |
| Ki-67 | 増殖指数 | 高値は悪性を示唆 |
| p16 | 腫瘍抑制 | 消失は悪性を示唆1) |
| S100, SOX10, HMB45 | メラノサイト系共通 | 良悪性の区別には使えない |
- 結膜母斑:隆起あり、タピオカ様封入嚢胞を伴う。先天性〜若年発症。
- 結膜悪性黒色腫:隆起・結節形成、腫瘍血管あり。急速に増大する傾向。
- 二次性メラノーシス:炎症・薬剤・化粧品など明確な誘因あり。
- 人種性色素沈着:両眼性・対称性。角膜縁・球結膜の定型的な分布。
5. 標準的な治療法
Section titled “5. 標準的な治療法”PAMの治療方針は、組織学的な異型の有無と程度によって決定される。
PAM with atypia
方針:積極的な治療介入。
軽度異型:切除 ± 冷凍凝固術。
高度異型(melanoma in situ):広範切除 + 冷凍凝固術 + MMC局所療法。
共通:全例で定期的な経過観察(悪性転化の早期発見)。
- 切除:疑わしい範囲を含めた切除を行う。悪性鑑別のために病理学的検査を行う。
- 冷凍凝固術:切除縁・切除底にダブルフリーズソー方式で追加することで、残存病変のリスクを低減する。
マイトマイシンC(MMC)局所化学療法
Section titled “マイトマイシンC(MMC)局所化学療法”組織学的に証明されたPAM with atypiaに対して、局所化学療法を行う。
- 適応:上皮内限定病変のみ(浸潤性メラノーマには不適切)
- プロトコール:0.02% マイトマイシンC点眼 5回/日 × 1週間を複数セッション施行2)
- 注意点:輪部幹細胞障害(最大12%)、涙点狭窄、白内障などの副作用がある
インターフェロンα-2b(IFNα-2b)
Section titled “インターフェロンα-2b(IFNα-2b)”マイトマイシンCの代替選択肢として、IFNα-2bの局所投与が用いられる。輪部幹細胞障害を生じないことがMMCに対する利点である。
必ずしもそうではない。PAM without atypia(異型なし)であれば、定期的な経過観察が基本方針である。一方、PAM with atypia(異型あり)は前がん病変であるため、切除や局所化学療法などの積極的な治療が推奨される。生検で異型の有無を確認してから治療方針を決定するのが標準的な手順である。
6. 病態生理学・詳細な発症機序
Section titled “6. 病態生理学・詳細な発症機序”メラノサイトの上皮内異常増殖
Section titled “メラノサイトの上皮内異常増殖”PAMの本態は、結膜上皮内におけるメラノサイトの異常増殖である。上皮下組織への浸潤がない段階が「上皮内」病変であり、浸潤が生じた時点で悪性黒色腫と診断される。
C-MILスペクトラム
Section titled “C-MILスペクトラム”現代の概念では、PAMはC-MIL(結膜メラノサイト上皮内病変)というスペクトラムとして理解される3)。
良性メラノーシス → 低悪性度C-MIL → 高悪性度C-MIL → melanoma in situ → 浸潤性メラノーマ
というスペクトラムが存在し、PAM with atypiaが中〜高悪性度C-MILに対応する。
悪性転化の分子機序
Section titled “悪性転化の分子機序”PAM with atypiaからの悪性転化には、TERTプロモーター変異(c.-124C>T)の関与が報告されている2)。同変異はテロメラーゼ逆転写酵素の活性化をもたらし、細胞の不死化と悪性転化を促進する。また高い腫瘍変異負荷との関連も示されている。
結膜悪性黒色腫との関係
Section titled “結膜悪性黒色腫との関係”結膜悪性黒色腫の発生源として、PAMが約60〜75%を占める。これはPAMが放置・見逃されることで浸潤性悪性黒色腫に進行することを示しており、早期診断・適切な管理の重要性を裏付けている。
7. 最新の研究と今後の展望
Section titled “7. 最新の研究と今後の展望”C-MIL分類の標準化
Section titled “C-MIL分類の標準化”C-MIL分類システムとC-MINスコアリングの国際的な標準化が進んでいる3)。これにより病理医間の診断再現性が向上し、異型程度に応じた治療選択の精度が高まることが期待される。
PRAME等の免疫組織化学による非侵襲的評価
Section titled “PRAME等の免疫組織化学による非侵襲的評価”PRAME、p16、Ki-67などのマーカーを組み合わせた免疫組織化学パネルにより、従来「不確定」とされた病変の再分類が可能になりつつある1)。これにより生検の必要性・タイミングをより正確に判断できる可能性がある。
前眼部OCTおよび共焦点顕微鏡
Section titled “前眼部OCTおよび共焦点顕微鏡”前眼部OCTや生体共焦点顕微鏡を用いた非侵襲的モニタリング技術の開発が進んでいる。生検を行わずにPAMの進展をリアルタイムに評価する手段として期待される。
Eder et al.(2024)は、通常の組織学的検査では評価困難な非典型的結膜メラノサイト増殖病変の5例において、免疫組織化学パネル(PRAME、p16、HMB45、Ki-67等)とFISH解析を組み合わせることで再分類が可能であることを示した1)。microRNA profilingによる良悪性鑑別の可能性も示唆されている。
PAMの分子プロファイリング
Section titled “PAMの分子プロファイリング”TERTプロモーター変異をはじめとする分子プロファイリングにより、PAMからメラノーマへの転化リスクを個別に予測する研究が進んでいる2)。将来的には分子的リスク評価に基づく個別化治療戦略が可能になる見込みである。
8. 参考文献
Section titled “8. 参考文献”- Eder A, Milman T, Mudhar HS, et al. Unusual conjunctival melanocytic proliferations: report of five cases and review of the literature. Surv Ophthalmol. 2024; PMC12208716.
- Goemaere J, Lauwers N, de Keizer ROB, et al. Bone metastasis in a case of primary acquired melanosis with atypia resulting from conjunctival melanoma. Am J Ophthalmol Case Rep. 2023; PMC9763362.
- Englisch CN, Berger T, Flockerzi F, et al. Conjunctival melanoma with pronounced central corneal invasion: one-year relapse free follow-up. Am J Ophthalmol Case Rep. 2024; PMC11403272.
