色素性メラノーマ(70%)
好発部位:球結膜に約90%が発生し、側頭象限に63%が局在する4, 6)。
外観:黒褐色〜茶褐色の隆起性病変。腫瘍に向かう豊富な栄養血管(feeder vessels)を伴う。
強膜との関係:強膜への癒着が認められることがある。腫瘍と角膜縁の平均距離は2mm、61%が角膜縁に到達する2)。

結膜に原発する悪性黒色腫は、結膜のメラノサイトに由来する悪性腫瘍である。欧米ではしばしば見られるが、わが国ではまれである。後天性メラノーシス(PAM)が発生母地となることが多い。
世界的な発生率は0.3〜0.8/100万人/年で、北欧・北米で最も高い。過去50年で増加傾向にある。米国では年間約130例、欧州では約320例の新規症例が推定される8)。アジア人の年齢調整発生率は0.15/100万人/年と低く、白人に最も多い(91.2%)1, 8)。
平均発症年齢は55〜65歳で、20歳未満の発症は極めて稀である1, 4, 5, 6)。5年疾患特異的生存率は約82.9%、10年では69.3%と報告されている8)。
発生母地による内訳:
結膜メラノーマは球結膜が紫外線に直接曝露されるため、粘膜メラノーマの中で唯一、紫外線曝露との関連が示唆される4)。
結膜悪性黒色腫の発生率は0.3〜0.8/100万人/年と稀な疾患だが、過去50年で増加傾向にある。アジア人は白人と比べて発症リスクが低く、0.15/100万人/年と報告されている。小児例は全結膜メラノーマの1%のみを占め、20歳未満の発症は極めて稀である。
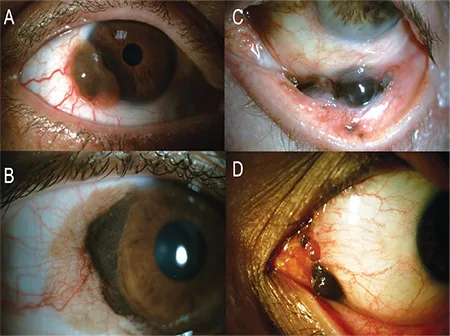
臨床的には眼球結膜や眼瞼結膜の隆起を伴う黒褐色病変で、腫瘍に向かって豊富な血管の分布が見られる。
色素性メラノーマ(70%)
好発部位:球結膜に約90%が発生し、側頭象限に63%が局在する4, 6)。
外観:黒褐色〜茶褐色の隆起性病変。腫瘍に向かう豊富な栄養血管(feeder vessels)を伴う。
強膜との関係:強膜への癒着が認められることがある。腫瘍と角膜縁の平均距離は2mm、61%が角膜縁に到達する2)。
無色素性メラノーマ(30%)
外観:ピンク〜赤色の腫瘤で、色素をほとんど含まない。
誤診リスク:扁平上皮癌や他の赤色結膜腫瘤と誤診されやすい3)。
予後:低色素性・無色素性は予後不良と関連する可能性がある。
画像評価:
ある。結膜メラノーマの約30%は無色素性(amelanotic)で、ピンク〜赤色の腫瘤として現れる。無色素性メラノーマは扁平上皮癌などと外観が類似するため誤診されやすく、診断の遅れにつながることがある。疑わしい結膜腫瘤には生検による病理診断が不可欠である。
以下の因子は転移・死亡リスクの上昇と関連する1, 4, 5, 6, 8)。
AJCC(米国がん合同委員会)病期分類は予後と強く相関する1)。
| 病期 | 5年累積死亡率 |
|---|---|
| cT1 | 2.5% |
| cT2 | 28.6% |
| cT3 | 31.6% |
| cT3c(眼窩浸潤) | 100% |
T3腫瘍の5年推定遠隔転移率は42%、5年死亡率は23%である1)。
転移はリンパ行性が主要経路である。側頭結膜病変は耳前リンパ節に、鼻側結膜病変は顎下リンパ節に転移しやすい。遠隔転移(血行性)は脳・肺・肝臓・皮膚・副腎などに生じる6, 1)。リンパ節転移は診断後2.3年で15〜41%に認められ、全身転移は3年で9〜25%に生じる。リンパ節転移が検出されない場合でも38%に遠隔血行性臓器転移が発生する6)。
腫瘍厚(特に2mm超)、病変部位(涙丘が最も予後不良)、AJCC病期分類、結節型の形態、リンパ管浸潤、眼窩浸潤などが主要な予後不良因子である。切除の完全性も大きく影響し、不完全切除例では約49.3%が再発する。センチネルリンパ節陽性例は死亡リスクが上昇する。
確定診断には生検が必要である。病理組織学的にはメラニン色素を含み、明瞭な核小体を有する核/胞体比の大きな細胞の増殖からなる。メラニン色素が多い場合は病理標本の脱色素処理を要する。
免疫組織化学染色は確定診断と鑑別に不可欠である。
| マーカー | 特徴 | 備考 |
|---|---|---|
| HMB-45 | メラノサイト系で陽性 | 診断に有用2, 8) |
| SOX10 | メラノサイト系で陽性 | 高感度1, 4) |
| Melan-A/MART-1 | メラノサイト系で陽性 | 汎用マーカー3, 5, 6) |
| S-100 | メラノサイト系で陽性 | 感度高いが特異度低1) |
| PRAME | メラノーマで陽性、母斑で陰性 | 最有力な鑑別マーカー5) |
| Ki-67 | メラノーマで10〜15%以上 | 増殖指数3, 4) |
| p16 | メラノーマで消失 | 母斑では保持5) |
メラノーマ確定例では系統的な全身評価が必要である。
周囲組織を含めた腫瘍の外科的切除が基本である。術中・術後のMMCやインターフェロンα-2bの局所投与も有効である。腫瘍が広範にわたり結膜下への浸潤が著しい場合には、眼窩内容除去術が必要となることがある。
手術療法
補助療法
冷凍凝固術:ダブルフリーズソー方式で切除底・縁に施行。結膜を挙上して強膜損傷を回避する3)
MMC局所化学療法:
IFNα-2b:輪部幹細胞障害を生じないMMCの代替3)
放射線療法:小線源治療または体外照射3)
センチネルリンパ節生検:腫瘍厚2mm超で検討7)
広範切除後の結膜再建には以下が用いられる4, 5)。
腫瘍細胞の播種(局所再発や転移)を防ぐため、術中に器具で腫瘍に直接触れず、灌流液(BSS)も使用しないドライな環境で切除する手技である。3〜5mmの安全域を確保して腫瘍全体を一塊で切除することで、不完全切除による再発リスクを低減する。腫瘍細胞の結膜への播種を最小限に抑える点で、通常の切除と根本的に異なる。
結膜メラノーマは、遺伝学的にぶどう膜メラノーマではなく皮膚メラノーマと類似する。紫外線関連のドライバー変異(C>T転換)としてBRAF・NF1・RASが主要である。ぶどう膜メラノーマのマーカー(BAP1、GNAQ、GNA11、SF3B1)は結膜メラノーマでは陰性であることが確認されている1)。
Lally et al.(2022)の101例を対象とした研究では、4つの高頻度変異が同定されている1)。
NF1変異(33〜50%)
BRAF変異(29〜46%)
頻度:2番目に多い変異。V600E変異が80〜90%。
分布:球結膜のメラノーマに多い(日光曝露部位)4)。
予後:転移・死亡との有意な関連はなし。標的療法(BRAF阻害薬)の治療標的となる。
NRAS変異(11〜26%)
頻度:3番目に多い変異。
予後:転移・死亡リスク増加、特に死亡リスクは約5倍1)。
特徴:BRAF変異と相互排他的。
ATRX変異(25%)
TERTプロモーター変異(c.-124C>T)はテロメラーゼ逆転写酵素に影響を与え、転移性結膜メラノーマとの関連が報告されている1, 8, 6)。PAMの中等度〜重度異型でも検出され(約8%)、上皮内メラノーマとしての性質を示唆する6)。また高い腫瘍変異負荷との関連も示されている4)。結膜メラノーマの32〜64%にTERT変異が認められ、予後との関連が注目されている8)。
高いPD-L1発現と免疫系関連遺伝子が豊富な転写サブタイプの存在が確認されており、これが免疫チェックポイント阻害薬使用の理論的根拠となっている。BRAF阻害薬・MEK阻害薬・PD-L1阻害薬のデータは有望だが、現時点では限定的である。
Chou et al.(2023)は94歳男性のT3c結膜メラノーマ症例で分子プロファイルを解析した。NF1変異とTERTプロモーター変異(c.-124C>T、VAF 31.4%)を同定し、BRAF・NRAS・cKITはすべて陰性であった。NF1変異とNRAS陰性の組み合わせが、転移なしという比較的良好な経過の一因として考察されている1)。
PD-1阻害薬(pembrolizumab、nivolumab)およびCTLA-4阻害薬(ipilimumab)が転移性・局所進行性結膜メラノーマに試みられている4, 8)。
代表的な報告として、Sagiv et al.(2018)はpembrolizumabまたはnivolumabによるPD-1阻害療法を5例に実施し、一部で完全奏効が得られたことを報告している8)。axitinib + nivolumabの組み合わせを用いたPhase 2試験(未治療進行・転移粘膜メラノーマ対象)が進行中である。
転移性結膜メラノーマに対する全身療法の標準レジメンはいまだ未確立であり、各症例での慎重な判断が求められる。
BRAF変異陽性例へのBRAF阻害薬単独(vemurafenib)またはBRAF/MEK阻害薬の併用(dabrafenib + trametinib、encorafenib + binimetinib)が試みられている4, 8)。
これらの薬剤は一部で局所腫瘍の縮小効果が報告されているが、多くは単症例または少数例の報告であり、長期成績は限定的である。MAPK経路とAKT経路の同時標的による相乗効果の可能性も検討中である3)。
免疫組織化学パネル(PRAME、p16、HMB-45、Ki-67、Cyclin D1)の活用により、従来「不確定」とされた病変の再分類が可能となりつつある5)。C-MIL(結膜メラノサイト上皮内病変)分類(WHO第5版、2022年)の国際標準化も進んでいる。
皮膚メラノーマとの遺伝学的類似性(BRAF・NF1・NRAS変異、高PD-L1発現)を根拠に、PD-1阻害薬(pembrolizumab、nivolumab)やCTLA-4阻害薬、BRAF阻害薬が転移性・局所進行性症例に試みられている。ただし大規模な臨床試験は行われておらず、現時点でエビデンスは限定的であり、標準レジメンは未確立である。国際的な多施設共同研究による大規模データの蓄積が急務とされている。