母斑
結膜メラノサイト系腫瘍
1. 結膜メラノサイト系腫瘍とは
Section titled “1. 結膜メラノサイト系腫瘍とは”結膜メラノサイト系腫瘍は、結膜のメラノサイトに由来する良性および悪性の新生物の総称である。主に3つのカテゴリに分類される。
- 母斑(nevus):先天性の良性腫瘍。最も一般的な結膜メラノサイト系腫瘍であり、悪性転換リスクは全体で約1%。
- 原発性獲得性メラノーシス:中年以降に発症する後天性の色素病変。異型を伴わないもの(良性)と、異型を伴うもの(前がん病変)に分けられる。近年は結膜メラノサイト上皮内病変(conjunctival melanocytic intraepithelial lesion, C-MIL)とも呼ばれ4)、C-MINスコア5以上はmelanoma in situと見なされる8)。
- 結膜メラノーマ(悪性黒色腫):全眼腫瘍の約2%、全眼メラノーマの5〜7%を占める悪性腫瘍1, 4, 5, 6)。
結膜メラノーマの世界的発生率は約0.3〜0.8/100万人/年で、北欧・北米で最も高い。過去50年で発生率は増加傾向にある。米国では年間約130例、欧州では約320例の新規症例が推定される。アジア人の年齢調整発生率は0.15/100万人/年と低く2)、白人に最も多く(91.2%)、アフロカリブ系は2.4%にとどまる。
平均発症年齢は55〜65歳で、20歳未満は極めて稀である5)。小児例は全結膜メラノーマの1%のみを占める9)。原発性獲得性メラノーシスは全結膜病変の11%を占め8)、メラノーマの起源としては最も一般的(約60〜75%)である。
メラノーマの起源別内訳:
- 原発性獲得性メラノーシス由来:約60〜75%(最も一般的)
- de novo(新規発生):約19%
- 母斑由来:7〜20%
結膜メラノーマは、球結膜が紫外線に直接曝露されるため、粘膜メラノーマの中で唯一、紫外線曝露との関連が示唆される腫瘍である6)。メラニンがUVB放射線を約2倍フィルタリングすることが、有色人種での発症が少ない理由として考えられている。
結膜メラノーマの発生率は0.3〜0.8/100万人/年と比較的稀な疾患だが、過去50年で増加傾向にある。一方、母斑は最も一般的な結膜メラノサイト系腫瘍であり、良性であることがほとんどである。
2. 主な症状と臨床所見
Section titled “2. 主な症状と臨床所見”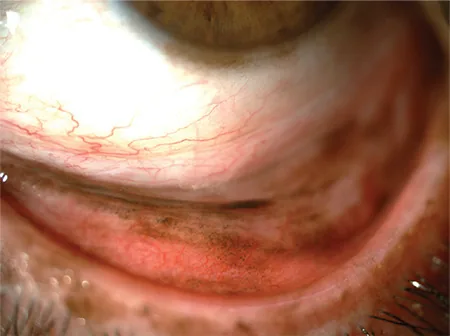
- 新しい色素性病変の出現、または既存病変の増大に気づいて受診するケースが多い
- 斑点やしこりの自覚、刺激感、疼痛4)
- 掻痒感、霧視、視力低下(角膜浸潤例)4)
- 接触時の出血を伴うこともある6)
- 無症状のまま経過し、健診や定期検査で偶然発見される場合もある5)
母斑・原発性獲得性メラノーシス・メラノーマはそれぞれ異なる臨床像を呈する。
原発性獲得性メラノーシス
患者背景:中年〜高齢者、主に白人、ほぼ常に片側性。
外観:淡褐色〜濃褐色の平坦な色素病変。多様な色調を呈する。
分布:結膜のどの部位にも発生。連続または非連続性。円蓋部・眼瞼結膜に隠れることがあるため、眼瞼翻転が評価に重要。
経過:「wax and wane」(増減の波)を示すことがある。色素消失は原発性獲得性メラノーシスの消失を意味しない8)。
結膜メラノーマ
そうではない。結膜の色素性病変の中では良性の母斑が最も一般的であり、悪性転換リスクは全体で約1%にとどまる。病変の部位・嚢胞の有無・発症時期・変化のパターンが良悪性の鑑別に重要であり、疑わしい変化があれば専門医への受診が推奨される。
3. 原因とリスク要因
Section titled “3. 原因とリスク要因”予後不良因子
Section titled “予後不良因子”以下の因子は転移・死亡リスクの上昇と関連する1, 4, 5, 6, 8)。
- 腫瘍厚 >2mm:1mm増加ごとのHR 1.20
- 深部浸潤:HR 2.35
- リンパ管浸潤:HR 7.49
- 潰瘍形成:HR 7.01
- T3腫瘍:HR 17.44
- 結節型メラノーマ:転移リスクRR 6.00〜8.44、死亡リスクRR 25.49〜35.49
- 病変部位:円蓋部・眼瞼結膜 > 球結膜。涙丘病変は3年死亡率50%と最も予後不良
- 眼窩浸潤
- 不完全切除:不完全切除例では約49.3%が再発
- 低色素性/無色素性メラノーマ
- 腫瘍関連リンパ管新生5)
AJCC(米国がん合同委員会)病期分類と死亡率
Section titled “AJCC(米国がん合同委員会)病期分類と死亡率”AJCC病期分類は予後と強く相関する1)。
| 病期 | 5年累積死亡率 |
|---|---|
| cT1 | 2.5% |
| cT2 | 28.6% |
| cT3 | 31.6% |
| cT3c(眼窩浸潤) | 100% |
T3腫瘍の5年推定遠隔転移率は42%、5年死亡率は23%である1)。
転移パターン
Section titled “転移パターン”転移はリンパ行性が主要経路である。側頭結膜病変は耳前リンパ節に、鼻側結膜病変は顎下リンパ節に転移しやすい。遠隔転移(血行性)は脳・肺・肝臓・皮膚・副腎・心臓・腹膜・膵臓・腸管・腎臓・骨・脾臓などに生じる6, 1)。リンパ節転移は診断後2.3年で15〜41%に認められ、全身転移は3年で9〜25%に生じる。なお、リンパ節転移が検出されない場合でも38%に遠隔血行性臓器転移が発生する8)。
腫瘍厚(特に2mm超)、病変部位(涙丘が最も予後不良)、AJCC病期分類、結節型の形態、リンパ管浸潤、眼窩浸潤などが主要な予後不良因子である。切除の完全性も大きく影響し、不完全切除例では約49.3%が再発する。
4. 診断と検査方法
Section titled “4. 診断と検査方法”- 細隙灯顕微鏡検査:病変の形態・色調・境界・嚢胞の有無を評価
- 前眼部光干渉断層計(AS-OCT):病変の深達度とボウマン膜の評価。過反射性病変として描出4)
- 超音波生体顕微鏡(UBM):腫瘍厚の計測と強膜浸潤の有無を確認5)
- 超音波検査:母斑の嚢胞検出
- 眼瞼翻転:原発性獲得性メラノーシスが円蓋部・眼瞼結膜に隠れることがあるため必須
- 写真記録:経過観察における変化の客観的評価
メラノーマ確定例では系統的な全身評価が必要である。
- PET/CT:全身転移の検索1, 9)
- 脳・眼窩MRI1, 4)
- 腹部超音波、胸部X線6, 4)
- リンパ節触診(耳前・顎下・頸部):毎回の外来受診時
- 頸部リンパ節超音波(重度の原発性獲得性メラノーシス/メラノーマ症例では年1回)8)
組織学的診断
Section titled “組織学的診断”確定診断には生検が必要である。
母斑の組織学的所見:
- 境界部または上皮下領域の母斑細胞巣
- 結膜封入嚢胞が特徴的
原発性獲得性メラノーシスの組織学的所見:
- 異型なし:上皮基底層の最小限のメラノサイト増殖
- 異型あり:異型メラノサイトの孤立/融合巣、パジェット様進展、大型異常細胞、明瞭な核小体、高い核細胞質比、核分裂像
メラノーマの組織学的所見:
- 上皮下層へのメラノーマ細胞浸潤
- 多形核、大型核、顕著な核小体、核分裂活性、豊富な細胞質5)
- パジェット様増殖、放射状上皮内進展、基底層の帯状炎症5)
免疫組織化学マーカー
Section titled “免疫組織化学マーカー”免疫組織化学は確定診断と良悪性の鑑別に不可欠である。WHO第5版でメラノサイトマーカー免疫組織化学が望ましい診断基準として採用されている8)。
| マーカー | 母斑 | メラノーマ | 備考 |
|---|---|---|---|
| S100 | + | + | メラノサイト系共通1) |
| SOX10 | + | + | メラノサイト系共通1, 4) |
| HMB45 | + | + | メラノサイト系共通1, 3, 9) |
| Melan-A/MART-1 | + | + | メラノサイト系共通3, 5, 6) |
| Ki-67 | 低値 | 10〜15%以上 | 増殖指数3, 4) |
| p16 | 保持 | 消失 | 腫瘍抑制7) |
| PRAME | − | + | 最有力な鑑別マーカー7) |
| bcl2 | − | 中〜強陽性 | アポトーシス抑制3) |
不確定メラノサイト増殖の特殊分類
Section titled “不確定メラノサイト増殖の特殊分類”良悪性に明確に分類できない病変が存在する7)。
- 深在性浸潤性母斑(deep penetrating nevus, DPN):WNT/βカテニン経路の活性化、BRAF V600E変異全例陽性、NRAS変異陰性、PRAME陰性、Ki-67低値。女性:男性 = 1.3:1、平均年齢25歳。切除後の再発・転移報告なし。
- 母斑様メラノーマ(nevoid melanoma):形態は母斑様だが悪性の挙動を示す。p16消失、PRAME陽性、Ki-67高値。BAP1不活性化と関連。管理はメラノーマに準ずる。
- 人種性色素沈着(complexion-associated melanosis)
- 色素性アクセンフェルト係蹄
- 結膜扁平上皮癌→ 無色素性メラノーマとの鑑別が特に重要5)
- 二次性色素沈着(マスカラなどの外因性色素沈着)
- 色素性眼内腫瘍の結膜下進展
5. 標準的な治療法
Section titled “5. 標準的な治療法”通常は写真記録を含む経過観察のみ。増大・色の変化がある場合は切除を検討する。ただし思春期の変化はホルモン変化・炎症・嚢胞増大が原因のことが多く、成人後の急激な変化が悪性化の指標となる。
原発性獲得性メラノーシスの管理
Section titled “原発性獲得性メラノーシスの管理”- 生検:疑わしい病変には切開生検/切除生検/マップ生検を慎重に実施
- 手術:臨床的に疑わしい範囲に応じて切除縁への冷凍凝固術を追加
- 局所化学療法:組織学的に証明された異型を伴う原発性獲得性メラノーシスにはマイトマイシンCまたはインターフェロンα-2bの局所投与を検討
- マイトマイシンC 0.02%:5回/日 × 1週間のセッションを複数回施行8)
- 上皮内限定病変のみが対象(浸潤性メラノーマには不適切)
- 経過管理の注意点:原発性獲得性メラノーシスの「wax and wane」により色素が消失しても病変が消失したとは限らない。マイトマイシンC治療後はマッピング生検で原発性獲得性メラノーシスの根絶を確認すべきである8)。
結膜メラノーマの手術療法
Section titled “結膜メラノーマの手術療法”外科的完全切除が第一選択である。以下の原則が重要である。
- 切除マージン:3〜5mmの安全域を確保した腫瘍全切除(一部文献では2〜4mm5))
- ノータッチ・テクニック:器具で腫瘍に直接触れず、腫瘍細胞の播種を防ぐ5, 9)
- ドライ・テクニック:灌流液(BSS)を使用せずに切除する
- 強膜浸潤例:強膜結膜切除術を施行
- 角膜浸潤例:アルコール角膜上皮剥離を推奨し、ホッケーナイフで角膜部分を一塊切除する4)
冷凍凝固術: ダブルフリーズソー方式で切除底・縁に施行する。結膜を挙上して行い、強膜損傷を回避する5)。
マイトマイシンC局所化学療法:
- 術中:0.02% マイトマイシンC microsponge 180秒間適用4)
- 術後:0.02% マイトマイシンC点眼 4回/日 × 7日間、1週間休薬で3サイクル4)
- 用量は報告により0.002%〜0.04%と幅がある5)
- 一次治療でのマイトマイシンC再発率は33〜100%、補助療法としての再発率は0〜66%5)
インターフェロンα-2b: 輪部幹細胞障害を生じないため、マイトマイシンCの代替選択肢として位置づけられる5)。
放射線療法: 小線源治療(brachytherapy)または体外照射5)。
広範切除後の結膜再建には以下が用いられる4, 5)。
- 羊膜移植:抗炎症・抗線維化・抗血管新生効果を有する
- 口腔粘膜移植
- 対側眼結膜移植
進行例の治療
Section titled “進行例の治療”- 眼窩内容除去術:広範/再発例に適応。切除後の再建には遊離橈側前腕皮弁、側頭頭頂筋膜弁、前外側大腿皮弁などが使用される2)。
- 眼球摘出術:眼内進展例に適応。
センチネルリンパ節生検
Section titled “センチネルリンパ節生検”腫瘍厚が2mmを超える症例では、センチネルリンパ節生検の実施を検討すべきである9)。
腫瘍細胞の播種(seedingによる局所再発や転移)を防ぐため、術中に器具で腫瘍に直接触れず、また灌流液(BSS)も使用しないドライな環境で切除する手技である。3〜5mmの安全域を確保して腫瘍全体を一塊で切除することで、不完全切除による再発リスクを低減する。
6. 病態生理学・詳細な発症機序
Section titled “6. 病態生理学・詳細な発症機序”皮膚メラノーマとの遺伝学的類似性
Section titled “皮膚メラノーマとの遺伝学的類似性”結膜メラノーマは、遺伝学的にぶどう膜メラノーマではなく皮膚メラノーマと類似する。紫外線関連のドライバー変異としてBRAF・NF1・RASが主要である。ぶどう膜メラノーマのマーカー(BAP1、GNAQ、GNA11、SF3B1)は結膜メラノーマでは陰性であることが確認されている1)。
主要分子変異
Section titled “主要分子変異”Lally et al.(2022)の101例を対象とした研究では、4つの高頻度変異が同定されている1)。
NF1変異(39%)
BRAF変異(31%)
頻度:2番目に多い変異。V600E変異が80〜90%。
分布:球結膜のメラノーマに多い(日光曝露部位)6)。
予後:転移・死亡との有意な関連はなし。標的療法(BRAF阻害薬)の治療標的となる。
NRAS変異(26%)
頻度:3番目に多い変異。
予後:転移・死亡リスク増加、特に死亡リスクは約5倍。
特徴:BRAF変異と相互排他的。
ATRX変異(25%)
頻度:4番目に多い変異。
予後:NF1変異と同様、2年・5年での低転移率と関連する。
TERTプロモーター変異
Section titled “TERTプロモーター変異”TERT c.-124C>T変異はテロメラーゼ逆転写酵素に影響を与え、転移性結膜メラノーマとの関連が報告されている1, 8, 6)。原発性獲得性メラノーシスの中等度〜重度異型でも検出され、上皮内メラノーマ(melanoma in situ)としての性質を示唆する8)。また高い腫瘍変異負荷との関連も示されている6)。
Chou et al.(2023)は94歳男性のT3c結膜メラノーマ症例で分子プロファイルを解析した。NF1変異(c.4339C>T、VAF 31.5%;c.5606T>A、VAF 32.0%)とTERTプロモーター変異(c.-124C>T、VAF 31.4%)を同定し、BRAF・NRAS・cKITはすべて陰性であった。NF1変異とNRAS陰性の組み合わせが、転移なしという比較的良好な経過の一因として考察されている1)。
免疫腫瘍微小環境
Section titled “免疫腫瘍微小環境”高いPD-L1発現と免疫系関連遺伝子が豊富な転写サブタイプの存在が確認されており、これが免疫チェックポイント阻害薬使用の理論的根拠となっている。BRAF阻害薬・MEK阻害薬・PD-L1阻害薬のデータは有望だが、現時点では限定的である。
7. 最新の研究と今後の展望(研究段階の報告)
Section titled “7. 最新の研究と今後の展望(研究段階の報告)”免疫チェックポイント阻害薬
Section titled “免疫チェックポイント阻害薬”PD-1阻害薬(pembrolizumab、nivolumab)が転移性結膜メラノーマに試みられている5)。ネオアジュバント(術前)免疫チェックポイント阻害薬の報告も存在する4)。
Goemaere et al.(2023)の原発性獲得性メラノーシス由来の骨転移症例では、nivolumabと脊椎への放射線療法が施行されたが、その後paclitaxel + carboplatinが追加され、最終的に緩和ケアへ移行した8)。転移性結膜メラノーマに対する全身療法の標準レジメンはいまだ未確立である。
BRAF変異陽性例へのBRAF阻害薬の使用が試みられている。MAPK経路とAKT経路の同時標的による相乗効果の可能性も検討中である5)。
診断技術の進歩
Section titled “診断技術の進歩”免疫組織化学パネル(PRAME、p16、HMB45、Ki-67、beta-catenin、Cyclin D1)の活用により、従来「不確定」とされた病変が再分類可能となりつつある7)。
Eder et al.(2024)はDPN 34例のFISH解析でBRAF V600E全例陽性、NRAS Q61R全例陰性を確認した。また、microRNA profilingによる良悪性鑑別の可能性も示唆されている7, 8)。FISH解析ではRREB1(6p25)、CCND1(11q13)、MYB(6q23)、MYC(8q24)の評価が行われている。
小児例への対応
Section titled “小児例への対応”Vishnevskia-Dai et al.(2023)は7歳男児の鼻側球結膜に発生した無色素性de novoメラノーマ(8mm×2.5mm)を報告した。ノータッチ・テクニックと4mmマージンによる切除、冷凍凝固術、羊膜移植を施行し、73ヶ月の無再発経過が得られた9)。小児例では組織学的にSpitz母斑との鑑別が特に重要である。
羊膜移植の長期成績
Section titled “羊膜移植の長期成績”広範切除後の羊膜移植は良好な上皮化をもたらすが、軽度の輪部幹細胞不全、瘢痕性角結膜炎、稀な局所再発が報告されている5)。
皮膚メラノーマとの遺伝学的類似性(BRAF・NF1・NRAS変異、高PD-L1発現)を根拠に、PD-1阻害薬(pembrolizumab、nivolumabなど)やBRAF阻害薬が転移性症例に試みられている。ただし大規模な臨床試験は行われておらず、現時点でエビデンスは限定的であり、標準レジメンは未確立である。
8. 参考文献
Section titled “8. 参考文献”- Chou LT, Lozeau DF, Boyle NS. A rare case of a long-standing, extensive and invasive conjunctival melanoma without systemic metastasis. Am J Ophthalmol Case Rep. 2023; PMC10121375.
- Tan JA, Khoo ET, Al-Chalabi MMM, Mohd Zainal H, Wan Sulaiman WA. Orbital Exenteration and Reconstruction Using a Free Radial Forearm Flap in Conjunctival Melanoma: Old but Gold. Cureus. 2023;15(7):e42572. doi:10.7759/cureus.42572. PMID:37637587. PMCID:PMC10460132.
- Montazer F, Heshmati SM, Asgari S, et al. Conjunctival melanoma: a case presentation. Iran J Pathol. 2023; PMC10646746.
- Englisch CN, Berger T, Flockerzi F, et al. Conjunctival melanoma with pronounced central corneal invasion: one-year relapse free follow-up. Am J Ophthalmol Case Rep. 2024; PMC11403272.
- Menna F, Tschopp M, Meyer P, et al. A case of conjunctival melanoma presenting as a squamous cell carcinoma. Case Rep Ophthalmol. 2024; PMC11509494.
- Okongwu CC, Adewara BA, Olaofe OO, Soremekun AI, Ayodele SO, Abdullahi YO, et al. Malignant melanoma of the conjunctiva metastasizing to the submandibular gland: a case report and review of the literature. BMC Ophthalmol. 2025;25(1):130. doi:10.1186/s12886-025-03949-5. PMID:40082862. PMCID:PMC11905526.
- Eder A, Milman T, Mudhar HS, et al. Unusual conjunctival melanocytic proliferations: report of five cases and review of the literature. Surv Ophthalmol. 2024; PMC12208716.
- Goemaere J, Lauwers N, de Keizer ROB, et al. Bone metastasis in a case of primary acquired melanosis with atypia resulting from conjunctiva melanoma. Am J Ophthalmol Case Rep. 2023;29:101730. doi:10.1016/j.ajoc.2022.101730. PMID:36561878; PMCID:PMC9763362.
- Vishnevskia-Dai V, Davidy T, Zloto O. Amelanotic conjunctival melanoma in a child. Am J Ophthalmol Case Rep. 2023; PMC9792290.
