색소성 흑색종 (70%)
호발 부위: 약 90%가 구결막에서 발생하며, 63%가 측두 사분면에 국한됩니다4, 6).
외관: 흑갈색에서 다갈색의 융기성 병변. 종양을 향하는 풍부한 영양 혈관(feeder vessels)을 동반합니다.
공막과의 관계: 공막에 유착이 인정되는 경우가 있습니다. 종양과 각막 윤부의 평균 거리는 2mm이며, 61%가 각막 윤부에 도달합니다2).

결막 악성 흑색종은 결막의 멜라닌 세포에서 유래하는 악성 종양입니다. 서양에서는 흔하지만 일본에서는 드뭅니다. 원발성 후천성 흑색증(PAM)이 발생 모태가 되는 경우가 많습니다.
전 세계 발생률은 0.3-0.8/100만 명/년이며, 북유럽과 북미에서 가장 높습니다. 지난 50년 동안 증가 추세에 있습니다. 미국에서는 연간 약 130건, 유럽에서는 약 320건의 새로운 사례가 추정됩니다8). 아시아인의 연령 표준화 발생률은 0.15/100만 명/년으로 낮으며, 백인에서 가장 흔합니다(91.2%)1, 8).
평균 발병 연령은 55-65세이며, 20세 미만 발병은 극히 드뭅니다1, 4, 5, 6). 5년 질병 특이 생존율은 약 82.9%, 10년은 69.3%로 보고됩니다8).
발생 모태에 따른 분류:
결막 흑색종은 구결막이 자외선에 직접 노출되기 때문에 점막 흑색종 중 유일하게 자외선 노출과의 연관성이 시사되는 질환입니다4).
결막 악성 흑색종의 발생률은 0.3~0.8/100만 명/년으로 드문 질환이지만, 지난 50년 동안 증가 추세에 있습니다. 아시아인은 백인에 비해 발병 위험이 낮아 0.15/100만 명/년으로 보고됩니다. 소아 증례는 전체 결막 흑색종의 1%에 불과하며, 20세 미만에서의 발병은 극히 드뭅니다.
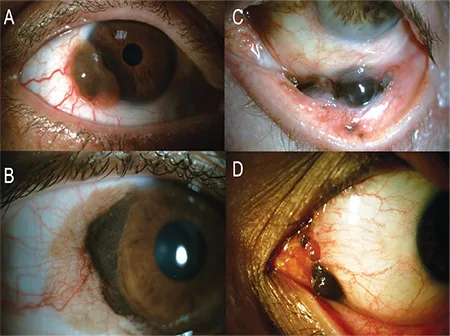
임상적으로는 안구 결막이나 안검 결막의 융기를 동반한 흑갈색 병변으로, 종양을 향한 풍부한 혈관 분포가 관찰됩니다.
색소성 흑색종 (70%)
호발 부위: 약 90%가 구결막에서 발생하며, 63%가 측두 사분면에 국한됩니다4, 6).
외관: 흑갈색에서 다갈색의 융기성 병변. 종양을 향하는 풍부한 영양 혈관(feeder vessels)을 동반합니다.
공막과의 관계: 공막에 유착이 인정되는 경우가 있습니다. 종양과 각막 윤부의 평균 거리는 2mm이며, 61%가 각막 윤부에 도달합니다2).
무색소성 흑색종 (30%)
외관: 분홍색에서 적색의 종괴로, 색소를 거의 포함하지 않습니다.
오진 위험: 편평세포암이나 다른 적색 결막 종괴로 오진되기 쉽습니다3).
예후: 저색소성 및 무색소성은 예후 불량과 관련될 수 있습니다.
영상 평가:
있습니다. 결막 흑색종의 약 30%는 무색소성(amelanotic)이며, 분홍색에서 적색의 종괴로 나타납니다. 무색소성 흑색종은 편평세포암 등과 외관이 유사하여 오진되기 쉽고, 진단 지연으로 이어질 수 있습니다. 의심되는 결막 종괴에는 생검을 통한 병리 진단이 필수적입니다.
다음 인자는 전이 및 사망 위험 증가와 관련됩니다1, 4, 5, 6, 8).
AJCC(미국암합동위원회) 병기 분류는 예후와 강한 상관관계가 있습니다1).
| 병기 | 5년 누적 사망률 |
|---|---|
| cT1 | 2.5% |
| cT2 | 28.6% |
| cT3 | 31.6% |
| cT3c (안와 침범) | 100% |
T3 종양의 5년 추정 원격 전이율은 42%, 5년 사망률은 23%입니다1).
전이는 림프성 경로가 주요 경로입니다. 측두 결막 병변은 이개 전 림프절로, 비측 결막 병변은 악하 림프절로 전이되기 쉽습니다. 원격 전이(혈행성)는 뇌, 폐, 간, 피부, 부신 등에 발생합니다6, 1). 림프절 전이는 진단 후 중앙값 2.3년에 1541%에서 발견되며, 전신 전이는 3년에 925%에서 발생합니다. 림프절 전이가 검출되지 않은 경우에도 38%에서 원격 혈행성 장기 전이가 발생합니다6).
종양 두께(특히 2mm 초과), 병변 부위(누구 가장 예후 불량), AJCC 병기, 결절형 형태, 림프관 침범, 안와 침범 등이 주요 예후 불량 인자입니다. 절제의 완전성도 크게 영향을 미치며, 불완전 절제례의 약 49.3%가 재발합니다. 감시 림프절 양성례는 사망 위험이 상승합니다.
확진을 위해서는 생검이 필요합니다. 조직병리학적으로 멜라닌 색소를 포함하고, 뚜렷한 핵소체를 가진 큰 핵/세포질 비율의 세포 증식으로 구성됩니다. 멜라닌 색소가 많은 경우 병리 표본의 탈색소 처리가 필요합니다.
면역조직화학염색은 확진 및 감별 진단에 필수적입니다.
| 마커 | 특징 | 비고 |
|---|---|---|
| HMB-45 | 멜라닌세포계에서 양성 | 진단에 유용2, 8) |
| SOX10 | 멜라닌세포 계열에서 양성 | 고감도 1, 4) |
| Melan-A/MART-1 | 멜라닌세포 계열에서 양성 | 범용 마커 3, 5, 6) |
| S-100 | 멜라닌세포 계열에서 양성 | 민감도는 높지만 특이도 낮음 1) |
| PRAME | 흑색종에서 양성, 모반에서 음성 | 가장 유력한 감별 마커 5) |
| Ki-67 | 흑색종에서 10~15% 이상 | 증식 지수 3, 4) |
| p16 | 흑색종에서 소실 | 모반에서 유지5) |
흑색종 확진 예에서는 체계적인 전신 평가가 필요합니다.
주변 조직을 포함한 종양의 외과적 절제가 기본입니다. 수술 중 및 수술 후 MMC나 인터페론 알파-2b의 국소 투여도 효과적입니다. 종양이 광범위하고 결막하 침윤이 심한 경우 안와 내용물 제거술이 필요할 수 있습니다.
수술 요법
절제 마진: 3~5mm의 안전 여백을 확보한 종양 완전 절제 4, 8)
노터치 기법: 기구로 종양에 직접 닿지 않아 종양 세포의 파종을 방지 4, 8)
드라이 기법: 관류액(BSS)을 사용하지 않고 절제
각막 침윤 예: 알코올 각막 상피 박리 + 호키 나이프로 일괄 절제 2)
안와 내용물 제거술: 광범위·재발 예에 적응 (진행 예)
안구 적출술: 안내 진행 예에 적응
보조 요법
냉동 응고술: 이중 동결-해동 방식으로 절제 바닥과 가장자리에 시행. 결막을 거상하여 공막 손상을 피함 3)
MMC 국소 화학 요법:
IFNα-2b: 윤부 줄기세포 손상을 일으키지 않는 MMC 대체제 3)
방사선 요법: 근접치료 또는 외부 방사선 조사3)
전초림프절 생검: 종양 두께 2mm 초과 시 고려7)
광범위 절제 후 결막 재건에는 다음이 사용됩니다4, 5).
종양 세포의 파종(국소 재발 또는 전이)을 방지하기 위해, 수술 중 기구로 종양에 직접 닿지 않고 관류액(BSS)도 사용하지 않는 건조한 환경에서 절제하는 술기입니다. 3~5mm의 안전 여백을 확보하여 종양 전체를 일괄 절제함으로써 불완전 절제로 인한 재발 위험을 줄입니다. 종양 세포의 결막 파종을 최소화한다는 점에서 일반 절제와 근본적으로 다릅니다.
결막 흑색종은 유전학적으로 포도막 흑색종이 아니라 피부 흑색종과 유사합니다. 자외선 관련 드라이버 돌연변이(C>T 전환)로 BRAF, NF1, RAS가 주요합니다. 포도막 흑색종의 마커(BAP1, GNAQ, GNA11, SF3B1)는 결막 흑색종에서 음성임이 확인되었습니다1).
Lally 등(2022)의 101례를 대상으로 한 연구에서 4가지 고빈도 변이가 확인되었습니다1).
NF1 변이 (33–50%)
빈도: 가장 흔한 변이.
예후: NF1 변이 단독은 2년 및 5년 낮은 전이율과 관련됩니다.
특징: BRAF 변이와 공존 가능. ATRX 변이와 자주 공존함8).
BRAF 변이 (29–46%)
빈도: 두 번째로 흔한 변이. V600E 변이가 80–90%를 차지합니다.
분포: 구결막 흑색종(일광 노출 부위)에 흔함4).
예후: 전이 또는 사망과 유의한 연관성 없음. 표적 치료(BRAF 억제제)의 치료 표적이 됩니다.
NRAS 변이 (11–26%)
빈도: 세 번째로 흔한 변이.
예후: 전이 및 사망 위험 증가, 특히 사망 위험은 약 5배1).
특징: BRAF 변이와 상호 배타적입니다.
ATRX 변이 (25%)
빈도: 네 번째로 흔한 돌연변이.
예후: NF1 돌연변이와 유사하게 2년 및 5년 낮은 전이율과 관련됨.
특징: NF1 돌연변이와 자주 공존함8).
TERT 프로모터 돌연변이(c.-124C>T)는 텔로머라제 역전사효소에 영향을 미치며 전이성 결막 흑색종과의 연관성이 보고되었습니다1, 8, 6). PAM의 중등도중증 이형성에서도 검출되며(약 8%), 상피내 흑색종의 특성을 시사합니다6). 또한 높은 종양 돌연변이 부담과의 연관성도 나타났습니다4). 결막 흑색종의 3264%에서 TERT 돌연변이가 확인되며, 예후와의 연관성이 주목받고 있습니다8).
높은 PD-L1 발현과 면역 관련 유전자가 풍부한 전사 아형의 존재가 확인되었으며, 이는 면역관문억제제 사용의 이론적 근거가 됩니다. BRAF 억제제, MEK 억제제, PD-L1 억제제에 대한 데이터는 유망하지만 현재 제한적입니다.
Chou et al.(2023)은 94세 남성의 T3c 결막 흑색종 증례에서 분자 프로파일을 분석했습니다. NF1 돌연변이와 TERT 프로모터 돌연변이(c.-124C>T, VAF 31.4%)를 동정했으며, BRAF, NRAS, cKIT은 모두 음성이었습니다. NF1 돌연변이와 NRAS 음성의 조합이 전이 없이 비교적 양호한 경과를 보인 한 요인으로 고려됩니다1).
PD-1 억제제(pembrolizumab, nivolumab) 및 CTLA-4 억제제(ipilimumab)가 전이성 및 국소 진행성 결막 흑색종에 시도되고 있습니다4, 8).
대표적인 보고로, Sagiv et al.(2018)은 pembrolizumab 또는 nivolumab에 의한 PD-1 억제 요법을 5명의 환자에게 시행하여 일부에서 완전 관해를 얻었다고 보고했습니다8). axitinib + nivolumab 병용 요법을 사용한 2상 시험(치료 경험이 없는 진행성 또는 전이성 점막 흑색종 대상)이 진행 중입니다.
전이성 결막 흑색종에 대한 전신 요법의 표준 요법은 아직 확립되지 않았으며, 각 증례에서 신중한 판단이 필요합니다.
BRAF 돌연변이 양성 증례에서 BRAF 억제제 단독(vemurafenib) 또는 BRAF/MEK 억제제 병용(dabrafenib + trametinib, encorafenib + binimetinib)이 시도되고 있습니다4, 8).
이들 약물은 일부에서 국소 종양 축소 효과가 보고되었으나, 대부분 단일 증례 또는 소수 증례 보고이며 장기 성적은 제한적입니다. MAPK 경로와 AKT 경로의 동시 표적을 통한 상승 효과 가능성도 검토 중입니다3).
면역조직화학 패널(PRAME, p16, HMB-45, Ki-67, Cyclin D1)의 활용으로 기존에 ‘불확정’으로 간주되었던 병변의 재분류가 가능해지고 있습니다5). C-MIL(결막 멜라닌세포 상피내 병변) 분류(WHO 제5판, 2022년)의 국제 표준화도 진행 중입니다.
피부 흑색종과의 유전적 유사성(BRAF, NF1, NRAS 돌연변이, 높은 PD-L1 발현)을 근거로 PD-1 억제제(pembrolizumab, nivolumab), CTLA-4 억제제, BRAF 억제제가 전이성 및 국소 진행성 증례에서 시도되고 있습니다. 그러나 대규모 임상 시험은 수행되지 않았으며, 현재 증거는 제한적이고 표준 요법은 확립되지 않았습니다. 국제 다기관 공동 연구를 통한 대규모 데이터 축적이 시급합니다.