特发性

急性渗出性多形性卵黄样黄斑病变(AEPVM)
一目了然的要点
Section titled “一目了然的要点”1. 什么是急性渗出性多形卵黄状黄斑病变?
Section titled “1. 什么是急性渗出性多形卵黄状黄斑病变?”急性渗出性多形卵黄状黄斑病变(Acute Exudative Polymorphous Vitelliform Maculopathy; AEPVM)是一种罕见的视网膜疾病,其特征是与浆液性视网膜脱离一致的双侧多发性黄白色视网膜下病变。1988年由Gass等人首次报道(Trans Am Ophthalmol Soc 1988)。
发病年龄范围从13岁到69岁,无性别差异。1)主要发生在白种人,但其他种族也有报道。文献中特发性病例仅约20例,极为罕见。1)
AEPVM根据病因分为以下两种类型:
- 特发性:认为与病毒感染或自身免疫机制有关
- 副肿瘤性:由恶性肿瘤或免疫检查点抑制剂引起
该疾病在ICD-10中归类为H35.89(其他特指的视网膜疾病)。
特发性AEPVM的文献报道仅约20例,是一种极为罕见的疾病。1)包括副肿瘤性病例在内,报告数量正在增加,但两种类型在全球范围内病例数都很少。
2. 主要症状和临床发现
Section titled “2. 主要症状和临床发现”主要眼底表现为双眼对称性、多发性黄白色视网膜下病变。病变形态多样,可呈圆形、椭圆形、曲线形等。主要位于黄斑部,但沿血管弓也可能出现水疱样病变。1)
病变内的卵黄样物质因重力向下沉淀,可形成半月状液面(假性前房积脓)。1)无玻璃体炎症或血管炎表现,无视乳头异常。1)
急性期和恢复期的眼底表现不同。以下展示两个阶段的所见。
急性期与恢复期的比较如下所示。
| 阶段 | 眼底所见 | 视力 |
|---|---|---|
| 急性期 | 多发性卵黄样病变 + 浆液性视网膜脱离 | 下降 |
| 恢复期 | 浆液消失→卵黄样物质向下沉淀 | 改善趋势 |
3. 原因与风险因素
Section titled “3. 原因与风险因素”AEPVM分为特发性和副肿瘤性两种类型,各自具有不同的原因和病理机制。
副肿瘤性
黑色素瘤:皮肤黑色素瘤和脉络膜黑色素瘤是最常见的致病恶性肿瘤。
其他恶性肿瘤:已报道与肺癌、乳腺癌、结肠癌等相关。
免疫检查点抑制剂:可能与BRAF抑制剂(维莫非尼、达拉非尼)和PD-1抑制剂(帕博利珠单抗、纳武利尤单抗)的使用相关。
发病机制:认为肿瘤抗原与视网膜抗原的交叉反应(分子模拟)引发针对RPE和感光细胞的自身免疫反应。
4. 诊断与检查方法
Section titled “4. 诊断与检查方法”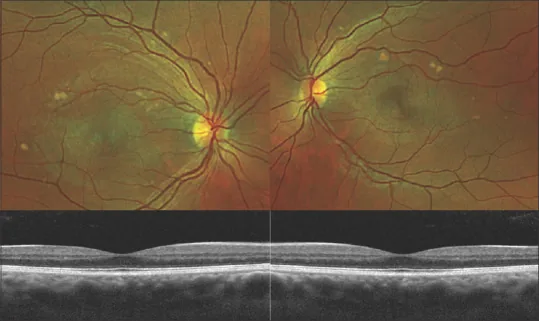
AEPVM的诊断是排除性诊断,需要系统性地排除类似疾病。多模态影像学检查的组合是诊断的关键。1)
影像学检查
功能与基因检查
FA和自发荧光检查(FAF)的反转模式是本病的特征性表现。
| 表现 | FA | FAF |
|---|---|---|
| 卵黄样物质 | 低荧光 | 高自发荧光 |
| 浆液部分 | 轻度高荧光 | 无荧光 |
AEPVM需要与以下疾病进行鉴别。
- Best卵黄样黄斑营养不良(BVMD):通过基因检测(BEST1突变)进行鉴别。AEPVM没有BEST1突变。1)
- 成人型卵黄样黄斑营养不良(AVMD):通过PRPH2突变的有无进行鉴别。
- Vogt-小柳-原田病(VKH):FA显示视盘强荧光和针尖样渗漏。AEPVM无渗漏,可据此鉴别。
- 原发性玻璃体视网膜淋巴瘤:与AEPVM相比,更易呈不对称性,常伴有玻璃体混浊。
5. 标准治疗方法
Section titled “5. 标准治疗方法”AEPVM尚无确定的药物治疗。特发性AEPVM是一种自限性疾病,可预期自然恢复。
- 以观察为主:定期进行眼底检查和OCT监测。Fernandes等人的报告显示,6个月后完全缓解。1)
- 类固醇治疗:对特发性AEPVM的疗效尚未确认,目前不推荐作为标准治疗。
- 合并脉络膜新生血管(CNV)的病例:若出现CNV,适用抗VEGF药物的玻璃体内注射。
- 副肿瘤性AEPVM:若怀疑与免疫检查点抑制剂(BRAF抑制剂、PD-1抑制剂)相关,应根据原发肿瘤的治疗情况与肿瘤科协作判断是否停药。也可考虑更换为其他免疫疗法。
特发性AEPVM是自限性疾病,多数病例可预期视力自然恢复。Fernandes等人的病例中,6个月后双眼最佳矫正视力改善至20/25,OCT显示视网膜下液完全消失。1)但恢复程度因病例而异。
6. 病理生理学与详细发病机制
Section titled “6. 病理生理学与详细发病机制”AEPVM的确切发病机制尚不明确。目前提出的主要假说如下。
RPE功能障碍假说
Section titled “RPE功能障碍假说”视网膜色素上皮(RPE)功能障碍导致脂褐素积累,引起浆液性视网膜脱离。神经感觉视网膜与RPE的物理分离损害了光感受器外节的正常吞噬功能。脱落的光感受器外节被认为积聚在视网膜外层和视网膜下腔(Spaide假说)。FAF上观察到的高自发荧光反映了这种脂褐素和荧光色素的积累。
自身免疫假说
Section titled “自身免疫假说”针对RPE和光感受器蛋白的自身抗体被认为参与发病机制。以下被报道为推测的自身抗体靶抗原:
- 恢复蛋白
- 转导素-α
- 过氧化物酶3(PRDX3):在特发性AEPVM急性期检测到抗PRDX3抗体,并在缓解后消失的病例已有报道。
- 碳酸酐酶2
- 120kDa光感受器蛋白
- 145kDa光感受器间视黄醇结合蛋白
在副肿瘤性病例中,推测肿瘤抗原与视网膜及RPE的共同抗原之间的交叉免疫反应(分子模拟)导致卵黄样病变的形成。
7. 最新研究与未来展望(研究阶段报告)
Section titled “7. 最新研究与未来展望(研究阶段报告)”通过多模态成像建立诊断
Section titled “通过多模态成像建立诊断”彩色眼底照相、SD-OCT和FAF的结合使得无需侵入性检查即可临床诊断AEPVM成为可能。1)每种模态提供互补信息,其中FAF和FA的反转模式是诊断的关键。
基因检测的标准化
Section titled “基因检测的标准化”利用下一代测序面板可以全面检测BEST1、PRPH2等基因突变。基因检测的标准化有助于提高排除诊断的准确性。1)
免疫检查点抑制剂时代的新挑战
Section titled “免疫检查点抑制剂时代的新挑战”随着BRAF抑制剂(维莫非尼、达拉非尼)和PD-1抑制剂(帕博利珠单抗、纳武利尤单抗)的普及,这些药物与副肿瘤性AEPVM的关联已成为新的临床挑战。随着免疫治疗的普及,副肿瘤性AEPVM的报告病例可能会增加。
病例积累和大规模研究的必要性
Section titled “病例积累和大规模研究的必要性”文献中报道的特发性AEPVM病例仅约20例。1)为了阐明病因和开发治疗方法,需要多中心合作进行病例积累和大规模前瞻性研究。
Fernandes等人(2023)报告了一例60多岁男性的特发性AEPVM病例,全身检查和下一代测序面板基因检测均为阴性。6个月后,最佳矫正视力改善至双眼20/25,SD-OCT证实视网膜下液完全消失。1)
8. 参考文献
Section titled “8. 参考文献”- Fernandes JS, Gomes PP, Neves P, et al. Idiopathic acute exudative polymorphous vitelliform maculopathy: the importance of multimodal imaging, systemic workup and genetic testing. BMJ Case Rep. 2023;16:e253969.
- Osman M, Mehana O, Eissa M, Zeineldin S, Sinha A. Coronavirus Disease 2019-induced Acute Exudative Polymorphous Vitelliform Maculopathy. Middle East Afr J Ophthalmol. 2022;29(4):235-237. PMID: 38162565.
- Lentzsch AM, Dooling V, Wegner I, Di Cristanziano V, Sadda SR, Freund KB, et al. ACUTE EXUDATIVE POLYMORPHOUS VITELLIFORM MACULOPATHY ASSOCIATED WITH PRIMARY EPSTEIN-BARR VIRUS INFECTION. Retin Cases Brief Rep. 2022;16(6):740-746. PMID: 33031214.
