特發性

急性滲出性多形卵黃狀黃斑病變(AEPVM)
一目瞭然的要點
Section titled “一目瞭然的要點”1. 什麼是急性滲出性多形卵黃狀黃斑病變?
Section titled “1. 什麼是急性滲出性多形卵黃狀黃斑病變?”急性滲出性多形卵黃狀黃斑病變(Acute Exudative Polymorphous Vitelliform Maculopathy; AEPVM)是一種罕見的視網膜疾病,其特徵是與漿液性視網膜剝離一致的雙側多發性黃白色視網膜下病變。1988年由Gass等人首次報告(Trans Am Ophthalmol Soc 1988)。
發病年齡範圍從13歲到69歲,無性別差異。1)主要發生在白種人,但其他種族也有報告。文獻上特發性病例僅約20例,極為罕見。1)
AEPVM根據病因分為以下兩種類型:
- 特發性:認為與病毒感染或自體免疫機制有關
- 副腫瘤性:由惡性腫瘤或免疫檢查點抑制劑引起
該疾病在ICD-10中歸類為H35.89(其他特指的視網膜疾病)。
特發性AEPVM的文獻報告僅約20例,是一種極為罕見的疾病。1)包括副腫瘤性病例在內,報告數量正在增加,但兩種類型在全球範圍內病例數都很少。
2. 主要症狀和臨床發現
Section titled “2. 主要症狀和臨床發現”- 雙眼視力下降:亞急性發病,數週內進展。1)
- 視力模糊:常發生於雙眼。
- 視物變形:伴隨黃斑部病變出現。
- 頭痛:特發性AEPVM急性期可能出現。
主要眼底表現為雙眼對稱性、多發性黃白色視網膜下病變。病變形態多樣,可呈圓形、橢圓形、曲線形等。主要位於黃斑部,但沿血管弓也可能出現水皰樣病變。1)
病變內的卵黃樣物質因重力向下沉澱,可形成半月狀液面(假性前房蓄膿)。1)無玻璃體炎症或血管炎表現,無視乳頭異常。1)
急性期和恢復期的眼底表現不同。以下展示兩個階段的所見。
急性期與恢復期的比較如下所示。
| 階段 | 眼底所見 | 視力 |
|---|---|---|
| 急性期 | 多發性卵黃樣病變 + 漿液性視網膜剝離 | 下降 |
| 恢復期 | 漿液消失→卵黃樣物質向下沉澱 | 改善趨勢 |
3. 原因與風險因素
Section titled “3. 原因與風險因素”AEPVM分為特發性和副腫瘤性兩種類型,各自具有不同的原因和病理機制。
副腫瘤性
黑色素瘤:皮膚黑色素瘤和脈絡膜黑色素瘤是最常見的致病惡性腫瘤。
其他惡性腫瘤:已報告與肺癌、乳癌、結腸癌等相關。
免疫檢查點抑制劑:可能與BRAF抑制劑(維莫非尼、達拉非尼)和PD-1抑制劑(帕博利珠單抗、納武利尤單抗)的使用相關。
發病機制:認為腫瘤抗原與視網膜抗原的交叉反應(分子擬態)引發針對RPE和感光細胞的自體免疫反應。
4. 診斷與檢查方法
Section titled “4. 診斷與檢查方法”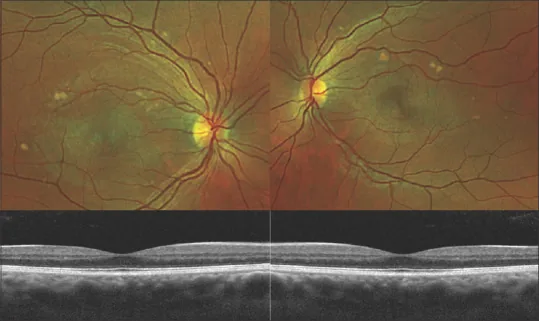
AEPVM的診斷是排除性診斷,需要系統性地排除類似疾病。多模態影像學檢查的組合是診斷的關鍵。1)
影像學檢查
OCT(光學同調斷層掃描):檢測穹頂狀神經感覺視網膜剝離和高反射或等反射的視網膜下沉積物。恢復期可觀察到漿液消失和RPE重新貼附。橢圓體帶增厚也可見。1)
FAF(眼底自體螢光):卵黃樣物質呈高自體螢光。這是診斷中最重要的檢查。1)反映脂褐素和螢光色素的積累。
FA(螢光素眼底血管攝影):卵黃樣物質呈低螢光或無螢光。特徵性地表現出與FAF相反的圖案。未見滲漏。
功能與基因檢查
FA和自體螢光檢查(FAF)的反轉模式是本疾病的特徵性發現。
| 發現 | FA | FAF |
|---|---|---|
| 卵黃狀物質 | 低螢光 | 高自體螢光 |
| 漿液部分 | 輕度高螢光 | 無螢光 |
AEPVM需與以下疾病進行鑑別。
- Best卵黃狀黃斑失養症(BVMD):透過基因檢測(BEST1突變)鑑別。AEPVM沒有BEST1突變。1)
- 成人型中心窩卵黃狀失養症(AVMD):透過PRPH2突變的有無鑑別。
- 原田病(Vogt-小柳-原田病;VKH):FA顯示視神經盤強螢光和針點狀滲漏。AEPVM無滲漏,可據此鑑別。
- 原發性玻璃體視網膜淋巴瘤:與AEPVM相比,較易呈不對稱性,且常伴隨玻璃體混濁。
Best病是由BEST1基因突變引起的遺傳性疾病,可透過基因檢測鑑別。AEPVM的次世代定序基因檢測顯示BEST1和PRPH2突變陰性。1)發病過程(急性或緩慢)和家族史也有助於鑑別。
5. 標準治療方法
Section titled “5. 標準治療方法”AEPVM尚無確立的藥物治療。特發性AEPVM是一種自限性疾病,可預期自然恢復。
- 以觀察為主要原則:定期進行眼底檢查和OCT監測。Fernandes等人的報告顯示,6個月後達到完全緩解。1)
- 類固醇治療:對特發性AEPVM的療效尚未確認,目前不建議作為標準治療。
- 合併脈絡膜新生血管(CNV)的病例:若出現CNV,適用抗VEGF藥物的玻璃體內注射。
- 副腫瘤性AEPVM:若懷疑與免疫檢查點抑制劑(BRAF抑制劑、PD-1抑制劑)相關,應根據原發腫瘤的治療情況與腫瘤科協調判斷是否停藥。也可考慮更換為其他免疫療法。
特發性AEPVM是自限性疾病,多數病例可預期視力自然恢復。Fernandes等人的病例中,6個月後雙眼最佳矯正視力改善至20/25,OCT顯示視網膜下液完全消失。1)但恢復程度因病例而異。
6. 病理生理學與詳細發病機轉
Section titled “6. 病理生理學與詳細發病機轉”AEPVM的確切發病機轉仍不清楚。目前提出的主要假說如下。
RPE功能障礙假說
Section titled “RPE功能障礙假說”視網膜色素上皮(RPE)功能障礙導致脂褐素累積,引起漿液性視網膜剝離。神經感覺視網膜與RPE的物理分離損害了光感受器外節的正常吞噬功能。脫落的光感受器外節被認為積聚在視網膜外層和視網膜下腔(Spaide假說)。FAF上觀察到的高自發螢光反映了這種脂褐素和螢光色素的累積。
自體免疫假說
Section titled “自體免疫假說”針對RPE和光感受器蛋白的自體抗體被認為參與發病機轉。以下被報導為推測的自體抗體標靶抗原:
- 恢復蛋白
- 轉導素-α
- 過氧化物酶3(PRDX3):在特發性AEPVM急性期檢測到抗PRDX3抗體,並在緩解後消失的病例已有報導。
- 碳酸酐酶2
- 120kDa光感受器蛋白
- 145kDa光感受器間視黃醇結合蛋白
在副腫瘤性病例中,推測腫瘤抗原與視網膜及RPE的共同抗原之間的交叉免疫反應(分子擬態)導致卵黃樣病變的形成。
7. 最新研究與未來展望(研究階段報告)
Section titled “7. 最新研究與未來展望(研究階段報告)”透過多模態影像建立診斷
Section titled “透過多模態影像建立診斷”彩色眼底攝影、SD-OCT和FAF的結合使得無需侵入性檢查即可臨床診斷AEPVM成為可能。1)每種模態提供互補資訊,其中FAF和FA的反轉模式是診斷的關鍵。
基因檢測的標準化
Section titled “基因檢測的標準化”利用次世代定序面板可以全面檢測BEST1、PRPH2等基因突變。基因檢測的標準化有助於提高排除診斷的準確性。1)
免疫檢查點抑制劑時代的新挑戰
Section titled “免疫檢查點抑制劑時代的新挑戰”隨著BRAF抑制劑(vemurafenib、dabrafenib)和PD-1抑制劑(pembrolizumab、nivolumab)的普及,這些藥物與副腫瘤性AEPVM的關聯已成為新的臨床挑戰。隨著免疫治療的普及,副腫瘤性AEPVM的報告病例可能會增加。
病例累積和大規模研究的必要性
Section titled “病例累積和大規模研究的必要性”文獻中報告的特發性AEPVM病例僅約20例。1)為了闡明病因和開發治療方法,需要多中心合作進行病例累積和大規模前瞻性研究。
Fernandes等人(2023)報告了一例60多歲男性的特發性AEPVM病例,全身檢查和次世代定序面板基因檢測均為陰性。6個月後,最佳矯正視力改善至雙眼20/25,SD-OCT證實視網膜下液完全消失。1)
8. 參考文獻
Section titled “8. 參考文獻”- Fernandes JS, Gomes PP, Neves P, et al. Idiopathic acute exudative polymorphous vitelliform maculopathy: the importance of multimodal imaging, systemic workup and genetic testing. BMJ Case Rep. 2023;16:e253969.
- Osman M, Mehana O, Eissa M, Zeineldin S, Sinha A. Coronavirus Disease 2019-induced Acute Exudative Polymorphous Vitelliform Maculopathy. Middle East Afr J Ophthalmol. 2022;29(4):235-237. PMID: 38162565.
- Lentzsch AM, Dooling V, Wegner I, Di Cristanziano V, Sadda SR, Freund KB, et al. ACUTE EXUDATIVE POLYMORPHOUS VITELLIFORM MACULOPATHY ASSOCIATED WITH PRIMARY EPSTEIN-BARR VIRUS INFECTION. Retin Cases Brief Rep. 2022;16(6):740-746. PMID: 33031214.
