โรคจุดรับภาพอักเสบเฉียบพลันชนิดมีสารคัดหลั่งและมีรอยโรคสีไข่แดงหลายรูปแบบ (AEPVM ) เป็นโรคจอประสาทตา ที่พบได้ยากมาก โดยมีลักษณะเป็นรอยโรคใต้จอประสาทตา สีเหลืองหลายจุดในตาทั้งสองข้าง
แบ่งเป็น 2 ชนิด คือ ชนิดไม่ทราบสาเหตุ และชนิดที่สัมพันธ์กับมะเร็ง (เกี่ยวข้องกับเนื้องอกมะเร็งหรือยายับยั้งจุดตรวจภูมิคุ้มกัน)
การตรวจออโตฟลูออเรสเซนซ์ (FAF ) เป็นการตรวจสำคัญในการวินิจฉัย โดยมีลักษณะเฉพาะคือการเรืองแสงอัตโนมัติสูงของสารคล้ายไข่แดง 1)
การตรวจทางพันธุกรรม (การหาลำดับรุ่นถัดไป) มีความสำคัญในการแยกโรคจากโรคที่คล้ายคลึงกัน เช่น โรคจอประสาทตา เสื่อมชนิดเบสต์ 1)
ชนิดไม่ทราบสาเหตุเป็นโรคที่จำกัดตัวเอง และในหลายกรณี การมองเห็น จะฟื้นคืนตามธรรมชาติ
ในชนิดพารานีโอพลาสติก อาการทางตาอาจเกิดขึ้นก่อนการตรวจพบเนื้องอกปฐมภูมิ
รายงานผู้ป่วยชนิดไม่ทราบสาเหตุในเอกสารมีเพียงประมาณ 20 ราย ซึ่งเป็นโรคที่หายากมาก 1)
โรคจุดรับภาพเสื่อมชนิดไข่แดงหลายรูปแบบเฉียบพลัน (Acute Exudative Polymorphous Vitelliform Maculopathy; AEPVM ) เป็นโรคจอประสาทตา ที่หายาก โดยมีลักษณะเฉพาะคือรอยโรคใต้จอประสาทตา สีขาวเหลืองหลายจุดทั้งสองข้างซึ่งสอดคล้องกับจอประสาทตาลอกชนิดมีน้ำใต้จอประสาทตา รายงานครั้งแรกโดย Gass และคณะในปี 1988 (Trans Am Ophthalmol Soc 1988)
อายุที่เริ่มป่วยอยู่ระหว่าง 13 ถึง 69 ปี และไม่มีความแตกต่างทางเพศ 1) ส่วนใหญ่เกิดในคนผิวขาว แต่ก็มีรายงานในเชื้อชาติอื่นด้วย ผู้ป่วยชนิดไม่ทราบสาเหตุในเอกสารมีเพียงประมาณ 20 ราย ซึ่งน้อยมาก 1)
AEPVM แบ่งตามสาเหตุออกเป็น 2 ชนิดดังนี้:
ชนิดไม่ทราบสาเหตุ (idiopathic) : เชื่อว่าเกี่ยวข้องกับการติดเชื้อไวรัสหรือกลไกภูมิต้านตนเองชนิดพารานีโอพลาสติก (paraneoplastic) : เกิดจากเนื้องอกมะเร็งหรือยาที่ยับยั้งจุดตรวจภูมิคุ้มกัน
โรคนี้จัดอยู่ใน ICD-10 รหัส H35.89 (โรคจอประสาทตา ที่ระบุอื่นๆ)
Q
AEPVM เป็นโรคที่หายากแค่ไหน?
A
ผู้ป่วย AEPVM ชนิดไม่ทราบสาเหตุที่รายงานในเอกสารมีเพียงประมาณ 20 ราย ซึ่งเป็นโรคที่หายากมาก 1) หากรวมชนิดพารานีโอพลาสติก จำนวนรายงานจะเพิ่มขึ้น แต่ทั้งสองชนิดมีจำนวนผู้ป่วยน้อยทั่วโลก
การมองเห็น ลดลงทั้งสองข้าง1) ตามัว : มักเกิดในทั้งสองข้างภาพบิดเบี้ยว (metamorphopsia)จอประสาทตา ส่วนกลางปวดศีรษะ : อาจพบได้ในระยะเฉียบพลันของ AEPVM ไม่ทราบสาเหตุ
ลักษณะสำคัญที่พบในจอตา คือ รอยโรคใต้จอตาสีขาวเหลือง หลายจุด และสมมาตรทั้งสองข้าง รูปร่างของรอยโรคหลากหลาย อาจเป็นวงกลม วงรี หรือโค้ง มักอยู่บริเวณจอประสาทตา ส่วนกลาง แต่อาจพบรอยโรคแบบตุ่มน้ำตามแนวเส้นเลือดได้ 1)
สารคล้ายไข่แดงภายในรอยโรคอาจตกตะกอนลงด้านล่างตามแรงโน้มถ่วง ทำให้เกิดระดับของเหลวรูปพระจันทร์เสี้ยว (pseudohypopyon) 1) ไม่พบการอักเสบของวุ้นตา หรือหลอดเลือดอักเสบ และไม่มีความผิดปกติของหัวประสาทตา 1)
ลักษณะจอตาแตกต่างกันระหว่างระยะเฉียบพลันและระยะฟื้นตัว ด้านล่างนี้คือลักษณะของทั้งสองระยะ
ด้านล่างนี้คือการเปรียบเทียบระหว่างระยะเฉียบพลันและระยะฟื้นตัว
ระยะ ลักษณะจอตา ความคมชัดของการมองเห็น เฉียบพลัน รอยโรคคล้ายไข่แดงหลายจุด + จอตาลอกแบบมีน้ำใต้จอตา ลดลง ระยะพักฟื้น น้ำในช่องว่างใต้จอประสาทตา หายไป → สารคล้ายไข่แดงตกตะกอนลงด้านล่าง แนวโน้มดีขึ้น
AEPVM แบ่งออกเป็น 2 ชนิด คือ ชนิดไม่ทราบสาเหตุและชนิดพารานีโอพลาสติก ซึ่งมีสาเหตุและพยาธิสภาพที่แตกต่างกัน
ชนิดไม่ทราบสาเหตุ
ประวัติการติดเชื้อมาก่อน : อาจมีอาการนำของการติดเชื้อไวรัส (HCV, คอกซากีบี, EB V, HIV, COVID-19), ซิฟิลิส, โรคไลม์ เป็นต้น
การบาดเจ็บที่ตา : มีรายงานว่าการบาดเจ็บที่ตาก่อนเกิดโรคเป็นปัจจัยกระตุ้น
สมมติฐานภูมิต้านตนเอง : ตรวจพบแอนติบอดีต่อเปอร์ออกซิเรดอกซิน 3 (PRDX3) ในระยะเฉียบพลันและหายไปหลังการทุเลา เชื่อว่าแอนติบอดีต่อตนเองต่อโปรตีน RPE และเซลล์รับแสง มีส่วนเกี่ยวข้องในพยาธิสภาพ
กรณีไม่ทราบสาเหตุแท้ : มีกรณีที่ไม่ทราบสาเหตุแท้ซึ่งการตรวจร่างกายและการตรวจทางพันธุกรรมทั้งหมดให้ผลลบ 1)
ชนิดพารานีโอพลาสติก
มะเร็งผิวหนังชนิดเมลาโนมา : มะเร็งผิวหนังชนิดเมลาโนมาและมะเร็งคอรอยด์ เมลาโนมาเป็นเนื้องอกร้ายที่พบบ่อยที่สุด
เนื้องอกร้ายอื่นๆ : มีรายงานความสัมพันธ์กับมะเร็งปอด เต้านม ลำไส้ใหญ่ เป็นต้น
สารยับยั้งจุดตรวจภูมิคุ้มกัน : อาจเกิดร่วมกับการใช้สารยับยั้ง BRAF (vemurafenib, dabrafenib) หรือสารยับยั้ง PD-1 (pembrolizumab, nivolumab)
กลไกการเกิด : เชื่อว่าปฏิกิริยาข้าม (molecular mimicry) ระหว่างแอนติเจนของเนื้องอกและแอนติเจนของจอประสาทตา ทำให้เกิดปฏิกิริยาภูมิต้านตนเองต่อ RPE และเซลล์รับแสง
หากเกิดการมองเห็น ลดลงโดยไม่ทราบสาเหตุหรือตามัวในตาทั้งสองข้าง ควรรีบไปพบจักษุแพทย์ทันที การวินิจฉัย AEPVM จำเป็นต้องมีการตรวจร่างกายอย่างละเอียด (เพื่อแยกเนื้องอกมะเร็ง) และการร่วมมือกับอายุรแพทย์และแพทย์ด้านมะเร็งอาจมีความสำคัญ หากคุณกำลังรักษาเนื้องอกมะเร็งด้วยยาที่ยับยั้งจุดตรวจสอบภูมิคุ้มกัน ควรแจ้งแพทย์ผู้รักษาทุกครั้งเมื่อมีการเปลี่ยนแปลงทางการมองเห็น
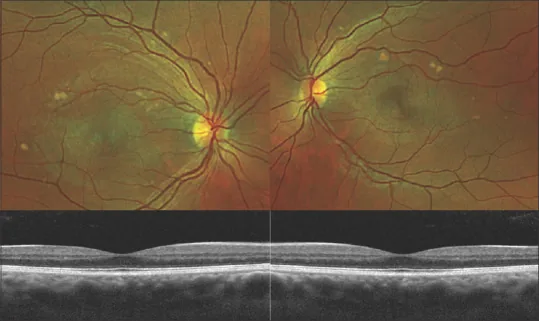
ภาพถ่ายจอตาและผล OCT ของ AEPVM Mohamed Osman; Omar Mehana; Mahmoud Eissa; et al. Coronavirus Disease 2019-induced Acute Exudative Polymorphous Vitelliform Maculopathy. Middle East African Journal of Ophthalmology. 2023 Sep 29. Figure 1. PM
CI D: PMC10754108. License: CC BY.
ภาพที่รวมภาพถ่ายจอตาและ OCT ของตาทั้งสองข้าง ช่วยให้เห็นการกระจายของรอยโรคที่จุดภาพชัด และการเปลี่ยนแปลงใต้จอตาได้ง่าย
การวินิจฉัย AEPVM เป็นการวินิจฉัยโดยการแยกโรค ต้องมีกระบวนการแยกโรคที่คล้ายคลึงกันอย่างเป็นระบบ การรวมกันของการถ่ายภาพหลายรูปแบบเป็นกุญแจสำคัญในการวินิจฉัย 1)
การตรวจภาพ
OCT (เครื่องตรวจชั้นตาด้วยแสง)RPE นอกจากนี้ยังพบความหนาของชั้น ellipsoid 1)
FAF (การเรืองแสงเองของจอตา)1) สะท้อนการสะสมของ lipofuscin และเม็ดสีเรืองแสง
FA (การถ่ายภาพหลอดเลือดด้วยฟลูออเรสซีน )FAF ไม่พบการรั่วซึม
การตรวจการทำงานและพันธุกรรม
EOG (การตรวจคลื่นไฟฟ้าจอตา)RPE
การตรวจคลื่นไฟฟ้าจอตา (ERG ) : อาจพบแอมพลิจูดลดลง
การตรวจพันธุกรรม : การค้นหาการกลายพันธุ์ของ BEST1 และ PRP H2 โดยใช้ชุดตรวจหาลำดับนิวคลีโอไทด์รุ่นใหม่มีความสำคัญ ผลลบต่อการกลายพันธุ์เหล่านี้สามารถแยกโรคจอตาเสื่อมชนิดไข่แดงของ Best ได้ 1)
การตรวจร่างกายอย่างละเอียด : การตรวจร่างกายทั้งหมดเพื่อแยกเนื้องอกมะเร็งเป็นสิ่งจำเป็น 1)
รูปแบบการกลับกันระหว่างการตรวจหลอดเลือดด้วยฟลูออเรสซีน (FA ) และการตรวจการเรืองแสงเอง (FAF ) เป็นลักษณะเฉพาะของโรคนี้
ลักษณะที่พบ FA FAF สารคล้ายไข่แดง การเรืองแสงต่ำ การเรืองแสงเองสูง ส่วนที่เป็นน้ำ การเรืองแสงสูงเล็กน้อย ไม่มีการเรืองแสง
AEPVM จำเป็นต้องแยกจากโรคต่อไปนี้:
โรคจอประสาทตา เสื่อมชนิดเบสต์ (BVMD) : แยกโดยการตรวจทางพันธุกรรม (การกลายพันธุ์ของ BEST1) AEPVM ไม่มีการกลายพันธุ์ของ BEST1 1) โรคจอประสาทตา เสื่อมชนิดไข่แดงในผู้ใหญ่ (AVMD) : แยกโดยการมีหรือไม่มีการกลายพันธุ์ของ PRP H2โรคฮาราดะ (Vogt-Koyanagi-Harada; VKH)FA จะเห็นการเรืองแสงสูงของจานประสาทตา และการรั่วแบบจุด AEPVM ไม่มีการรั่วมะเร็งต่อมน้ำเหลืองจอตาและวุ้นตา ปฐมภูมิ : มักไม่สมมาตรเมื่อเทียบกับ AEPVM และมักมีวุ้นตา ขุ่นร่วมด้วย
Q
จะแยกโรค Best (จอประสาทตาเสื่อมชนิดไข่แดง) ออกจาก AEPVM ได้อย่างไร?
A
โรค Best เป็นโรคทางพันธุกรรมจากการกลายพันธุ์ของยีน BEST1 และสามารถแยกได้ด้วยการตรวจทางพันธุกรรม ใน AEPVM การตรวจยีนด้วยการหาลำดับรุ่นใหม่จะให้ผลลบต่อการกลายพันธุ์ BEST1 และ PRP H2 1) นอกจากนี้ ลักษณะการเกิด (เฉียบพลันหรือค่อยเป็นค่อยไป) และประวัติครอบครัวยังช่วยในการวินิจฉัยแยกโรค
ไม่มีการรักษาด้วยยาที่เป็นมาตรฐานสำหรับ AEPVM AEPVM ที่ไม่ทราบสาเหตุเป็นโรคที่จำกัดตัวเอง (self-limiting) และคาดว่าจะฟื้นตัวได้เอง
การสังเกตเป็นหลัก : ตรวจอวัยวะตาเป็นระยะและติดตามด้วย OCT ในรายงานของ Fernandes et al. พบว่าหายขาดสมบูรณ์หลังจาก 6 เดือน 1) การรักษาด้วยสเตียรอยด์ : ยังไม่ยืนยันประสิทธิภาพใน AEPVM ที่ไม่ทราบสาเหตุ และปัจจุบันไม่แนะนำให้ใช้เป็นการรักษามาตรฐานกรณีที่มีเส้นเลือดใหม่ในคอรอยด์ (CNV ) : หากเกิด CNV การฉีดยา anti-VEGF เข้าในวุ้นตา เป็นสิ่งที่บ่งชี้AEPVM แบบพารานีโอพลาสติก
Q
การพยากรณ์การมองเห็นของ AEPVM ที่ไม่ทราบสาเหตุเป็นอย่างไร?
A
AEPVM ที่ไม่ทราบสาเหตุเป็นโรคที่จำกัดตัวเอง และในกรณีส่วนใหญ่คาดว่าจะฟื้นตัวการมองเห็น ได้เอง ในกรณีของ Fernandes et al. ค่าสายตาที่ดีที่สุดที่แก้ไขแล้วดีขึ้นเป็น 20/25 ในทั้งสองตาหลัง 6 เดือน และ OCT แสดงให้เห็นว่าของเหลวใต้จอประสาทตา หายไปหมด 1) อย่างไรก็ตาม ระดับการฟื้นตัวแตกต่างกันไปในแต่ละกรณี
กลไกที่แน่ชัดของการเกิด AEPVM ยังไม่เป็นที่เข้าใจอย่างสมบูรณ์ สมมติฐานหลักที่เสนอในปัจจุบันมีดังนี้:
ความผิดปกติของเยื่อบุผิวสีจอประสาทตา (RPE ) ทำให้เกิดการสะสมของ lipofuscin นำไปสู่จอประสาทตาลอก แบบมีน้ำใต้จอประสาทตา การแยกตัวทางกายภาพระหว่างจอประสาทตา ชั้นรับความรู้สึกและ RPE ทำให้การทำหน้าที่ฟาโกไซโทซิสตามปกติของส่วนนอกเซลล์รับแสง บกพร่อง เชื่อว่าส่วนนอกที่หลุดลอกจะสะสมในชั้นนอกของจอประสาทตา และช่องใต้จอประสาทตา (สมมติฐาน Spaide) การเรืองแสงอัตโนมัติสูงที่สังเกตได้ใน FAF สะท้อนถึงการสะสมของ lipofuscin และเม็ดสีเรืองแสงเหล่านี้
เชื่อว่าแอนติบอดีต่อตนเองต่อโปรตีน RPE และเซลล์รับแสง มีส่วนเกี่ยวข้องในการเกิดโรค มีรายงานแอนติเจนเป้าหมายของแอนติบอดีต่อตนเองที่สันนิษฐานดังต่อไปนี้:
รีคัฟเวอริน ทรานส์ดิวซิน-อัลฟา เปอร์ออกซิเรดอกซิน 3 (PRDX3) : มีรายงานกรณีที่ตรวจพบแอนติบอดีต่อ PRDX3 ในระยะเฉียบพลันของ AEPVM ที่ไม่ทราบสาเหตุ และหายไปหลังจากการทุเลาคาร์บอนิกแอนไฮเดรส 2 โปรตีนเซลล์รับแสง ขนาด 120 kDa โปรตีนจับรีตินอยด์ระหว่างเซลล์รับแสง ขนาด 145 kDa
ในกรณีพารานีโอพลาสติก เชื่อว่าปฏิกิริยาภูมิคุ้มกันข้าม (การเลียนแบบโมเลกุล) ระหว่างแอนติเจนของเนื้องอกและแอนติเจนร่วมของจอประสาทตา /RPE ทำให้เกิดรอยโรคคล้ายไข่แดง
ด้วยการรวมการถ่ายภาพจอประสาทตาสี , SD-OCT และ FAF ทำให้สามารถวินิจฉัยทางคลินิกของ AEPVM ได้โดยไม่ต้องตรวจแบบรุกราน 1) แต่ละรูปแบบให้ข้อมูลเสริมกัน และโดยเฉพาะรูปแบบการกลับกันระหว่าง FAF และ FA เป็นกุญแจสำคัญในการวินิจฉัย
ด้วยการใช้แผงการหาลำดับรุ่นถัดไป สามารถค้นหาการกลายพันธุ์ของยีน เช่น BEST1 และ PRP H2 ได้อย่างครอบคลุม การทำให้การตรวจทางพันธุกรรมเป็นมาตรฐานช่วยเพิ่มความแม่นยำของการวินิจฉัยแยกโรค 1)
ด้วยการแพร่หลายของสารยับยั้ง BRAF (vemurafenib, dabrafenib) และสารยับยั้ง PD-1 (pembrolizumab, nivolumab) ความสัมพันธ์ระหว่างยาเหล่านี้กับ AEPVM ที่เกี่ยวข้องกับเนื้องอกกลายเป็นความท้าทายทางคลินิกใหม่ เมื่อการรักษาด้วยภูมิคุ้มกันแพร่หลายมากขึ้น รายงานผู้ป่วย AEPVM ที่เกี่ยวข้องกับเนื้องอกอาจเพิ่มขึ้น
ผู้ป่วย AEPVM ที่ไม่ทราบสาเหตุในเอกสารมีเพียงประมาณ 20 ราย 1) เพื่ออธิบายสาเหตุและพัฒนาการรักษา จำเป็นต้องมีการรวบรวมผู้ป่วยจากหลายสถาบันและการศึกษาไปข้างหน้าขนาดใหญ่
Fernandes และคณะ (2023) รายงานผู้ป่วย AEPVM ที่ไม่ทราบสาเหตุในชายอายุ 60 ปี ซึ่งการตรวจร่างกายทั่วร่างกายและการตรวจทางพันธุกรรมด้วยแผงการหาลำดับรุ่นถัดไปให้ผลลบทั้งหมด หลังจาก 6 เดือน ค่าสายตาที่ดีที่สุดที่แก้ไขแล้วดีขึ้นเป็น 20/25 ในทั้งสองข้าง และ SD-OCT แสดงให้เห็นว่าของเหลวใต้จอประสาทตา หายไปอย่างสมบูรณ์ 1)
Fernandes JS, Gomes PP, Neves P, et al. Idiopathic acute exudative polymorphous vitelliform maculopathy: the importance of multimodal imaging, systemic workup and genetic testing. BMJ Case Rep. 2023;16:e253969.
Osman M, Mehana O, Eissa M, Zeineldin S, Sinha A. Coronavirus Disease 2019-induced Acute Exudative Polymorphous Vitelliform Maculopathy. Middle East Afr J Ophthalmol. 2022;29(4):235-237. PMID: 38162565.
Lentzsch AM, Dooling V, Wegner I, Di Cristanziano V, Sadda SR, Freund KB, et al. ACUTE EXUDATIVE POLYMORP HOUS VITELLIFORM MACULOPATHY ASSOCI ATED WITH PRIMARY EPSTEIN-BARR VIRUS INF ECTION. Retin Cases Brief Rep. 2022;16(6):740-746. PMID: 33031214.
ถาม AI เกี่ยวกับบทความนี้
คัดลอกข้อความบทความแล้ววางในผู้ช่วย AI ที่คุณต้องการใช้
เปิดผู้ช่วย AI ด้านล่าง แล้ววางข้อความที่คัดลอกลงในช่องแชต