药物沉积
上皮沉积:高亲脂性药物在上皮内蓄积,形成漩涡状或线状混浊。
实质沉积:从角膜缘血管网渗出的成分沉积在实质中。
内皮沉积:积聚在房水中的药物附着在内皮表面。

药物诱发性角膜并发症是局部使用(滴眼液)或全身用药引起的角膜损伤的总称。损伤可发生在角膜的上皮、基质或内皮任何一层1)。
病理生理学大致分为以下三类。
药物沉积
上皮沉积:高亲脂性药物在上皮内蓄积,形成漩涡状或线状混浊。
实质沉积:从角膜缘血管网渗出的成分沉积在实质中。
内皮沉积:积聚在房水中的药物附着在内皮表面。
细胞毒性
滴眼液主药:抗生素、抗真菌药、非甾体抗炎药、β受体阻滞剂、表面麻醉剂等的直接毒性。
防腐剂:苯扎氯铵(BAK)用于约70%的眼科制剂,对结膜和角膜上皮细胞产生细胞毒性(细胞死亡、紧密连接破坏、凋亡、免疫炎症反应)2)。
全身用药:抗癌药物转移到泪液中,损伤角膜上皮。
过敏
速发型:滴眼后数小时内出现结膜充血和水肿,2-3天自然消退。
迟发型:作为接触性皮炎或药物性假性类天疱疮慢性进展。
局部用药直接作用于角膜。全身用药通过泪膜、房水和房角血管系统到达角膜。角膜药物沉积可能是视网膜疾病的前兆,因此全身评估很重要。
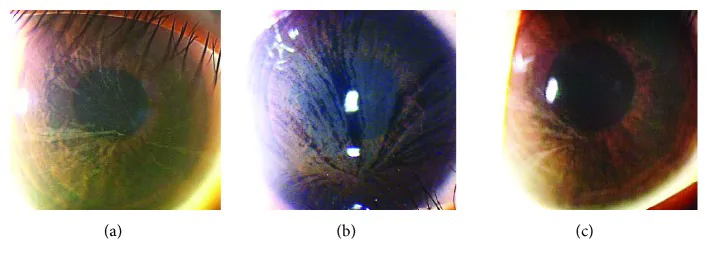
轻度药物沉积通常无症状。细胞毒性或过敏损伤时出现以下症状:
药物毒性引起的角膜上皮损伤根据严重程度逐步进展。
轻至中度
重度
药物毒性角膜上皮病变中,角膜上皮损伤比结膜上皮损伤更突出。而干眼症则先出现结膜上皮损伤,这是鉴别的关键点。荧光素染色显示由于上皮屏障功能下降而出现的特征性晚期染色(浴缸角膜病变)。
首先,用药史的问询最为重要。请确认是否使用过胺碘酮、羟氯喹、吲哚美辛等全身用药,以及是否使用多种眼药水。由于法布里病也会出现类似的角膜表现,需通过家族史和皮肤、肾脏症状评估进行鉴别诊断。
脂溶性高的药物沉积在上皮内,形成漩涡状混浊(角膜涡状混浊)。由于与法布里病的表现相似,用药史的问询对诊断至关重要。
| 药物分类 | 代表药物 | 备注 |
|---|---|---|
| 抗心律失常药 | 胺碘酮 | 高剂量时几乎100% |
| 抗疟药 | 羟氯喹、氯喹 | 也需注意视网膜病变 |
| 非甾体抗炎药 | 吲哚美辛 | 漩涡状至线状 |
其他药物如他莫昔芬、萘普生、阿托伐醌、苏拉明、氯法齐明和金制剂也可引起漩涡状角膜病变。
滴眼液毒性:防腐剂(BAC)是最常见的原因。β受体阻滞剂、前列腺素类药物、NSAID滴眼液和氨基糖苷类抗生素的主要成分也具有上皮毒性。滴眼次数越多、种类越多、使用时间越长,越容易发生损伤。
抗癌药物毒性:进入泪液的抗癌药物会损伤角膜上皮。由于角膜上皮表达EGFR和HER2,针对这些靶点的药物具有较高的上皮损伤风险。
ROCK抑制剂:奈他舒地尔可能导致角膜上皮水疱和网状图案。停药后2-4周消失。
从角膜缘血管网渗出的成分沉积在实质层。通常不伴有炎症表现。
胺碘酮角膜病变通常不影响视力。角膜上皮深层可见褐色漩涡状沉积物,但多数无症状。少数患者可能主诉畏光或光晕。停药后3至20个月角膜恢复透明。然而,由于胺碘酮也有报道引起缺血性视神经病变,如果出现视力下降,还应进行视神经评估。
最重要的诊断步骤是详细询问用药史。同时检查滴眼液(种类、次数、使用时间、是否含防腐剂)和全身用药。
评估药物沉积的部位和性质。鉴别是上皮内还是上皮下,以及基质的深度。
评估角膜上皮损伤所必需。药物毒性具有以下特征:
药物性漩涡角膜病变需与法布里病鉴别。法布里病伴有家族史、皮肤血管角化瘤、肾损害、四肢疼痛等全身症状。
治疗原则是停用或减量疑似致病药物。但若因原发病治疗(如抗癌药或青光眼药物)难以停药时,需与主治医生协作。
如果毒性引起的炎症伴有明显的充血和滤泡性结膜炎,可考虑使用类固醇滴眼液。但需注意防腐剂的影响以及类固醇导致的伤口愈合延迟。
局部给药:滴眼液通过泪膜直接接触角膜上皮。除了主药的细胞毒性外,防腐剂(如BAC)会损伤上皮细胞膜。
全身给药:药物通过三条途径到达角膜。
脂溶性高的药物(如胺碘酮、氯喹、吲哚美辛等)容易在角膜上皮内蓄积。它们在上皮深层形成漩涡状沉积,临床上与法布里病的角膜涡状混浊相似。胺碘酮角膜病变由Orlando分为I~IV级,与剂量和用药时间相关。
角膜上皮表达EGFR和HER2。靶向这些受体的抗癌药物(如西妥昔单抗、厄洛替尼、曲妥珠单抗等)直接抑制角膜上皮的增殖和分化,上皮损伤风险高。
如果防腐剂是主要原因,则有望改善2)。存在多种策略,包括替代防腐剂(SofZia、Polyquad、Purite)、不含防腐剂的制剂和缓释制剂2)。但是,如果毒性来自药物本身,更换为不含防腐剂的制剂可能无法获得充分改善。改善通常需要数周至数月,重要的是不要急于增加或更换治疗。