藥物沉積
上皮沉積:高親脂性藥物在上皮內蓄積,形成漩渦狀或線狀混濁。
實質沉積:從角膜緣血管網滲出的成分沉積在實質中。
內皮沉積:積聚在房水中的藥物附著在內皮表面。

藥物誘發性角膜併發症是局部使用(眼藥水)或全身用藥引起的角膜損傷的總稱。損傷可發生在角膜的上皮、基質或內皮任何一層1)。
病理生理學大致分為以下三類。
藥物沉積
上皮沉積:高親脂性藥物在上皮內蓄積,形成漩渦狀或線狀混濁。
實質沉積:從角膜緣血管網滲出的成分沉積在實質中。
內皮沉積:積聚在房水中的藥物附著在內皮表面。
細胞毒性
眼藥水主藥:抗生素、抗真菌藥、非類固醇抗發炎藥、β阻斷劑、表面麻醉劑等的直接毒性。
防腐劑:苯扎氯銨(BAK)用於約70%的眼科製劑,對結膜和角膜上皮細胞產生細胞毒性(細胞死亡、緊密連接破壞、凋亡、免疫炎症反應)2)。
全身用藥:抗癌藥物轉移到淚液中,損傷角膜上皮。
過敏
即時型:點眼後數小時內出現結膜充血和水腫,2-3天自然消退。
延遲型:作為接觸性皮膚炎或藥物性假性類天皰瘡慢性進展。
局部用藥直接作用於角膜。全身用藥通過淚膜、房水和隅角血管系統到達角膜。角膜藥物沉積可能是視網膜疾病的前兆,因此全身評估很重要。
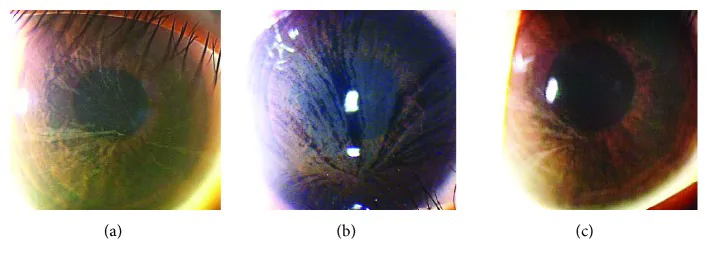
輕度藥物沉積通常無症狀。細胞毒性或過敏損傷時出現以下症狀:
藥物毒性引起的角膜上皮損傷根據嚴重程度逐步進展。
輕至中度
重度
藥物毒性角膜上皮病變中,角膜上皮損傷比結膜上皮損傷更突出。而乾眼症則先出現結膜上皮損傷,這是鑑別的關鍵點。螢光素染色顯示由於上皮屏障功能下降而出現的特徵性晚期染色(浴缸角膜病變)。
首先,用藥史的詢問最為重要。請確認是否使用過胺碘酮、羥氯喹、吲哚美辛等全身性藥物,以及是否使用多種眼藥水。由於法布瑞氏症也會出現類似的角膜表現,需透過家族史和皮膚、腎臟症狀評估進行鑑別診斷。
脂溶性高的藥物沉積在上皮內,形成漩渦狀混濁(角膜渦狀混濁)。由於與法布瑞氏症的表現相似,用藥史的詢問對診斷至關重要。
| 藥物分類 | 代表藥物 | 備註 |
|---|---|---|
| 抗心律不整藥 | 胺碘酮 | 高劑量時幾乎100% |
| 抗瘧藥 | 羥氯喹、氯喹 | 也需注意視網膜病變 |
| 非類固醇抗發炎藥 | 吲哚美辛 | 漩渦狀至線狀 |
其他藥物如泰莫西芬、萘普生、阿托伐醌、蘇拉明、氯法齊明和金製劑也可引起漩渦狀角膜病變。
眼藥水毒性:防腐劑(BAC)是最常見的原因。β阻斷劑、前列腺素類藥物、NSAID眼藥水和胺基醣苷類抗生素的主要成分也具有上皮毒性。點眼次數越多、種類越多、使用時間越長,越容易發生損傷。
抗癌藥物毒性:進入淚液的抗癌藥物會損傷角膜上皮。由於角膜上皮表現EGFR和HER2,針對這些靶點的藥物具有較高的上皮損傷風險。
ROCK抑制劑:奈他舒地爾可能導致角膜上皮水皰和網狀圖案。停藥後2-4週消失。
從輪部血管網滲出的成分沉積在實質層。通常不伴有發炎症狀。
胺碘酮角膜病變通常不影響視力。角膜上皮深層可見褐色漩渦狀沉積物,但多數無症狀。少數患者可能主訴畏光或光暈。停藥後3至20個月角膜恢復透明。然而,由於胺碘酮也有報導引起缺血性視神經病變,如果出現視力下降,還應進行視神經評估。
最重要的診斷步驟是詳細詢問用藥史。同時檢查眼藥水(種類、次數、使用時間、是否含防腐劑)和全身用藥。
評估藥物沉積的部位和性質。鑑別是上皮內還是上皮下,以及基質的深度。
評估角膜上皮損傷所必需。藥物毒性具有以下特徵:
藥物性漩渦角膜病變需與法布瑞氏症鑑別。法布瑞氏症伴有家族史、皮膚血管角化瘤、腎損害、四肢疼痛等全身症狀。
治療原則是停用或減量疑似致病藥物。但若因原發病治療(如抗癌藥或青光眼藥物)難以停藥時,需與主治醫師協作。
如果毒性引起的發炎伴有明顯的充血和濾泡性結膜炎,可考慮使用類固醇眼藥水。但需注意防腐劑的影響以及類固醇導致的傷口癒合延遲。
局部給藥:眼藥水通過淚膜直接接觸角膜上皮。除了主藥的細胞毒性外,防腐劑(如BAC)會損傷上皮細胞膜。
全身給藥:藥物通過三條途徑到達角膜。
脂溶性高的藥物(如胺碘酮、氯喹、吲哚美辛等)容易在角膜上皮內蓄積。它們在上皮深層形成漩渦狀沉積,臨床上與法布瑞氏症的角膜渦狀混濁相似。胺碘酮角膜病變由Orlando分為I~IV級,與劑量和用藥時間相關。
角膜上皮表現EGFR和HER2。靶向這些受體的抗癌藥物(如西妥昔單抗、厄洛替尼、曲妥珠單抗等)直接抑制角膜上皮的增殖和分化,上皮損傷風險高。
如果防腐劑是主要原因,則有望改善2)。存在多種策略,包括替代防腐劑(SofZia、Polyquad、Purite)、不含防腐劑的製劑和緩釋製劑2)。但是,如果毒性來自藥物本身,更換為不含防腐劑的製劑可能無法獲得充分改善。改善通常需要數週至數月,重要的是不要急於增加或更換治療。