药物性(最常见)

涡状角膜
一目了然的要点
Section titled “一目了然的要点”1. 什么是角膜涡状混浊
Section titled “1. 什么是角膜涡状混浊”角膜涡状混浊(cornea verticillata)是指角膜基底上皮层出现涡旋状图案的沉积物。也称为涡状角膜病变、旋涡状角膜病变或Fleischer涡。“verticillata”在拉丁语中意为“涡旋”。
通常无症状,常在裂隙灯显微镜检查时偶然发现。由药物、代谢底物或疾病副产物在角膜基底上皮溶酶体中积聚引起。胺碘酮和法布里病是最常见的原因。
角膜涡状纹通常不影响视力。少数患者可能会看到蓝绿色环或光晕,但大多数患者没有症状。药物引起的病例通常在停用致病药物后消失。角膜涡状纹本身不需要改变用药,但评估原发病(尤其是法布里病)很重要。
2. 主要症状和临床发现
Section titled “2. 主要症状和临床发现”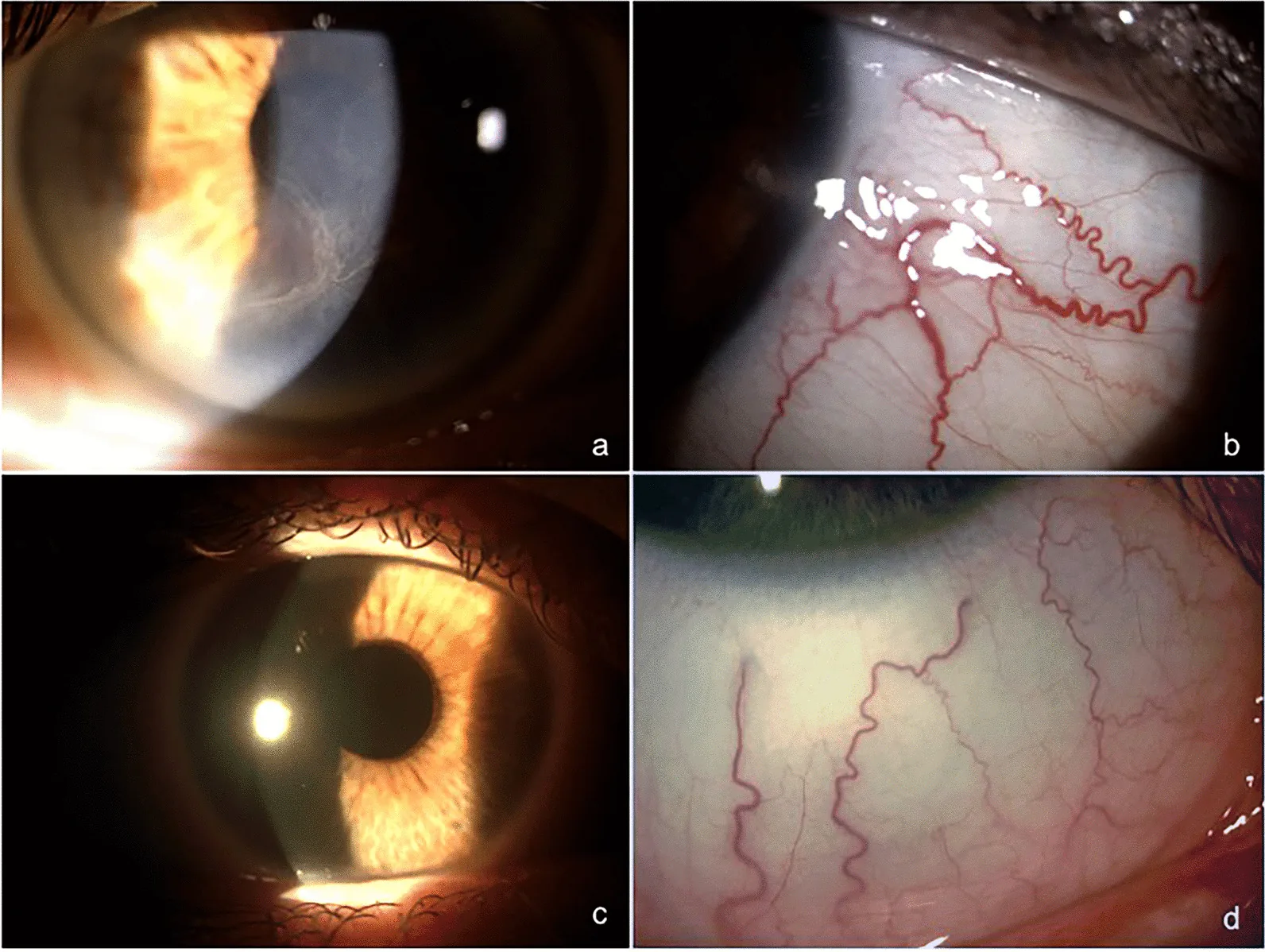
大多数角膜涡状纹患者无症状。少数患者可能会看到光晕或抱怨视物模糊。在奈他舒地尔引起的病例中,已报告有眩光和视物模糊2)。
裂隙灯显微镜检查显示角膜基底上皮有细小的金褐色至灰色涡旋状混浊。混浊通常以角膜下方为中心呈分支状扩散。荧光素染色阴性,几乎总是双眼性。
药物性和法布里病的混浊模式可能略有不同。药物性倾向于表现为末端有细小分支的水平线。法布里病则呈现曲线模式,在角膜周边变直前形成涡旋。
在胺碘酮角膜病变中,角膜中央稍下方的上皮深层可见褐色涡旋状沉积物,按Orlando分级为I至IV级。高剂量(400 mg/天)时几乎100%出现。
3. 原因和风险因素
Section titled “3. 原因和风险因素”法布里病(非药物性代表)
频率:约90%的患者出现涡状角膜病变
发病时间:相对早期(约6岁)出现
遗传方式:X连锁隐性遗传
机制:α-半乳糖苷酶A缺乏导致鞘糖脂积累
诊断意义:女性携带者中,涡状角膜病变可能是唯一的眼部表现1)
| 药物分类 | 代表药物 |
|---|---|
| 抗心律失常药 | 胺碘酮 |
| 抗疟药/免疫调节剂 | 羟氯喹/氯喹 |
| 非甾体抗炎药 | 吲哚美辛 |
| ROCK抑制剂 | 奈他舒地尔 |
| 抗精神病药 | 氯丙嗪 |
其他非药物性原因包括多发性骨髓瘤、全身性神经节苷脂沉积症、多种硫酸酯酶缺乏症和Lisch角膜营养不良。
引起漩涡状角膜病变的典型药物包括胺碘酮(抗心律失常药)、羟氯喹/氯喹(抗疟药)和吲哚美辛(非甾体抗炎药)。近年来,青光眼治疗药奈他舒地尔(ROCK抑制剂)也被报道可引起漩涡状角膜病变。这些药物具有阳离子和两亲性,积聚在角膜基底上皮的溶酶体中。停用致病药物有望改善。
4. 诊断与检查方法
Section titled “4. 诊断与检查方法”裂隙灯显微镜检查
Section titled “裂隙灯显微镜检查”巩膜散射法可清晰观察角膜上皮面的漩涡状混浊。后照法或配合钴蓝滤光片也有助于显示混浊模式。
共焦激光扫描显微镜(IVCM)
Section titled “共焦激光扫描显微镜(IVCM)”共聚焦激光扫描显微镜有助于鉴别药物性和法布里病。法布里病在角膜上皮、基质和角膜缘区域可见特征性的高反射沉积物,与疾病严重程度和全身受累相关。
法布里病的详细检查
Section titled “法布里病的详细检查”如果从涡状角膜怀疑法布里病,则进行以下检查。男性中,酶活性是可靠的指标,但女性由于莱昂化(X染色体失活),酶活性可能正常,因此基因检测必不可少1)。
- α-半乳糖苷酶A活性测定(DBS法)
- 血浆Lyso-Gb3(球三糖基鞘氨醇)测定
- GLA基因测序分析
有报道称,在年轻患者中心视网膜动脉阻塞(CRAO)或脑梗死的检查中发现涡状角膜,进而诊断为法布里病5)。在年轻血管事件患者中,通过眼科评估确认是否存在涡状角膜非常重要5)。
如果无用药史却出现涡状角膜,则怀疑法布里病。特别是年轻患者血管事件(脑梗死、CRAO)伴有涡状角膜时,高度怀疑。男性可通过α-半乳糖苷酶A活性降低确诊,但女性携带者酶活性可能正常,因此需要进行GLA基因检测。法布里病的早期诊断和治疗影响预后,因此发现涡状角膜是重要的契机。
5. 标准治疗方法
Section titled “5. 标准治疗方法”涡状角膜的管理
Section titled “涡状角膜的管理”涡状角膜本身通常无需治疗。沉积物不会对视力造成显著影响。仅涡状角膜表现时,无需更改药物方案或进一步检查。
停用致病药物后沉积物会消失。奈他舒地尔引起的涡状角膜和结膜色素沉着在停药14个月后完全消失2)。
玻璃体内注射甲氨蝶呤引起的涡状角膜,通过频繁使用人工泪液、洛替泼诺、局部叶酸(5 mg/mL)滴眼和口服叶酸,在3周内完全消失4)。玻璃体内注射后充分冲洗角膜表面有助于预防4)。
视网膜毒性的监测
Section titled “视网膜毒性的监测”使用羟氯喹、氯喹、氯丙嗪或他莫昔芬的患者存在视网膜毒性风险。涡状角膜病变的存在与视网膜毒性无直接相关性,但建议定期进行自动视野检查和SD-OCT监测。
法布里病的治疗
Section titled “法布里病的治疗”法布里病中的涡状角膜病变不是酶替代疗法(ERT)的直接适应症,但ERT用于全身管理。开始ERT后,已确认血中Lyso-Gb3水平下降1)。在一个家系中,母亲在ERT开始6个月后Lyso-Gb3从21.76降至12.72 nmol/L,儿子从156.50降至27.48 nmol/L1)。
6. 病理生理学与详细发病机制
Section titled “6. 病理生理学与详细发病机制”涡状图案的形成机制
Section titled “涡状图案的形成机制”角膜上皮从角膜缘干细胞向中心部向心性移动。含有药物或脂质的角膜缘干细胞沿此向心性移动路径迁移,形成涡状图案。
药物性机制
共同特性:阳离子且两亲性的药物渗透入角膜基底上皮的溶酶体。
蓄积过程:药物-脂质复合物抵抗酶解,作为沉积物蓄积。
胺碘酮:抑制溶酶体磷脂酶A2。
奈他舒地尔:推测机制为角膜上皮细胞内的磷脂沉积症2)。
法布里病的机制
酶缺乏:由于α-半乳糖苷酶A缺乏所致
蓄积物质:鞘糖脂(主要是Gb3)在溶酶体中蓄积
沉积部位:进行性蓄积于包括角膜在内的全身组织的溶酶体中
基因:GLA基因突变。已报道超过1000种突变1)
甲氨蝶呤引起的机制
Section titled “甲氨蝶呤引起的机制”玻璃体内注射甲氨蝶呤被认为对角膜缘干细胞有直接毒性4)。注射后药物渗漏到结膜下腔会损伤角膜缘干细胞,导致一过性角膜缘功能障碍和漩涡状角膜病变4)。由于是可逆的,推测损伤的是增殖中的干细胞而非干细胞龛4)。
与药物性角膜上皮病变的关系
Section titled “与药物性角膜上皮病变的关系”漩涡状角膜病变(vortex keratopathy)表现为当角膜上皮脱落持续增加,仅靠基底细胞增殖无法代偿时,表层细胞迁移覆盖角膜表面的形态。如果进展,可能通过上皮裂纹线发展为持续性上皮缺损。
7. 最新研究与未来展望
Section titled “7. 最新研究与未来展望”法布里病的GLA基因已鉴定出超过1000种突变,新突变报告不断。一项研究首次报道了移码突变c.484delT(p.W162Gfs*3)是经典型法布里病的病因1)。另一报告确认了马来西亚首例法布里病,漩涡状角膜成为诊断线索3)。
除了ROCK抑制剂引起的漩涡状角膜病变,新报告还描述了结膜色素沉着的并发症2)。色素沉着需与原发性获得性黑变病鉴别,但停药后消失是鉴别点2)。
一例年轻CRAO患者因漩涡状角膜发现法布里病的病例5),显示了眼科医生早期发现的重要性。
8. 参考文献
Section titled “8. 参考文献”- Giacalone I, Ruzzi L, Anania M, et al. The identification of a novel pathogenic variant of the GLA gene associated with a classic phenotype of Anderson-Fabry disease: a clinical and molecular study. Int J Mol Sci. 2025;26(2):470.
- Azargui S, Karanxha J, Oliver SCN, Kahook MY, Capitena Young CE. Netarsudil-associated conjunctival pigmentation. Am J Ophthalmol Case Rep. 2025;38:102311.
- Tang ASO, Wong QY, Ting IPL, et al. First 2 Fabry cases with novel mutation and their associated clusters in Malaysia. Am J Case Rep. 2021;22:e932923.
- Hasan N, Narde HK, Das AK, Chawla R. Unusual presentation of cornea verticillata with intravitreal methotrexate in a case of primary intraocular lymphoma. BMJ Case Rep. 2022;15:e246911.
- Nakata D, Okada H, Shimada Y, Tanikawa A, Horiguchi M, Ito Y. A case of Fabry disease with central retinal artery occlusion. Case Rep Ophthalmol. 2022;13:584-588.
