裂隙灯显微镜检查
后照法:显示角膜后表面细微颗粒状沉积物的最基本方法。
镜面反射:可高对比度观察Descemet膜前的混浊。
直接照明:微小沉积物容易漏诊,因此联合后照法很重要。

角膜面粉状变性(cornea farinata)是指在角膜基质最深层、紧贴Descemet膜前方出现细微粉尘状混浊的表现1)。由瑞士眼科医生Arthur Vogt首次描述,也称为“面粉状角膜”。
双眼发病,随年龄增长缓慢进展。由于不影响视力,临床意义有限。被归类为变性而非角膜营养不良。40岁以下罕见。活体共聚焦显微镜(IVCM)可见角膜深层基质角膜细胞胞质内高反射微粒1)。
由STS基因(Xp22.31)突变引起的X连锁鱼鳞病(XLI)患者也出现类似的角膜深层混浊2,3)。50%的患者和25%的女性携带者中可见,从成年早期出现2)。这种情况并非年龄变化,而是由类固醇硫酸酯酶缺乏导致硫酸胆固醇蓄积所致3)。
角膜面粉状变性通常不需要治疗。由于无症状且不影响视力,仅需观察随访。但需与呈现类似角膜深层混浊的Fuchs角膜内皮营养不良等疾病鉴别。Fuchs伴有角膜内皮细胞密度降低,而角膜面粉状变性的角膜内皮正常。
角膜面粉状变性通常无症状。不会引起视力下降、眼痛、异物感或畏光。多数情况下在裂隙灯检查中偶然发现。
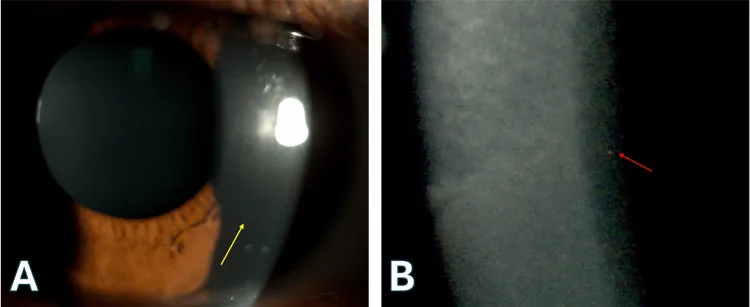
裂隙灯显微镜下,通过后照法或镜面反射可见角膜后表面有细微的灰白色至黄褐色颗粒状沉积物。混浊密集分布于角膜中央至旁中央区,周边部减少。单个沉积物极小,直接裂隙光照射时容易漏诊。
混浊弥漫均匀分布于Descemet膜前方的角膜基质。Descemet膜、角膜上皮和内皮细胞层均无异常。角膜厚度在正常范围内。镜面显微镜检查显示角膜内皮细胞形态和密度均正常。
最大的风险因素是年龄增长。多见于老年人,进展缓慢,但几乎不会引起临床问题。40岁以下发病的报道很少见。
STS基因(Xp22.31)突变导致的类固醇硫酸酯酶缺乏会引起X连锁鱼鳞病(XLI)。XLI患者角膜基质深层积聚胆固醇硫酸酯,出现类似角膜粉样变性的混浊。STS基因至少报道了6种不同的突变,突变类型不同导致类固醇硫酸酯酶的表达和功能各异,从而表现出多种表型。
裂隙灯显微镜检查
后照法:显示角膜后表面细微颗粒状沉积物的最基本方法。
镜面反射:可高对比度观察Descemet膜前的混浊。
直接照明:微小沉积物容易漏诊,因此联合后照法很重要。
角膜内皮镜
角膜内皮评估:确认内皮细胞的形态和密度正常。
与Fuchs内皮营养不良鉴别:Fuchs营养不良可见角膜小滴和内皮细胞密度降低,而本病内皮正常。
共焦显微镜
深层观察:在Descemet膜前的角膜基质细胞内可见高反射微粒。
鉴别诊断:有助于与类似的角膜营养不良和变性进行鉴别。
| 疾病 | 混浊特征 | 角膜内皮 |
|---|---|---|
| 角膜粉状变性 | 微细粉尘状、深层 | 正常 |
| Fuchs角膜内皮营养不良 | 角膜小滴、深层 | 异常 |
| 前Descemet膜角膜营养不良 | 多形性混浊、深层 | 正常 |
其他鉴别诊断包括斑点状角膜营养不良、深部丝状营养不良和后部点状营养不良。这些疾病均表现为角膜深层混浊,但混浊的形态和分布不同。
仅通过裂隙灯显微镜有时难以与Fuchs角膜内皮营养不良鉴别,需要进行角膜内皮镜(specular microscopy)检查。角膜粉样变性(角膜小麦粉状变性)中角膜内皮未见异常。
角膜粉样变性和Fuchs角膜内皮营养不良均在角膜深层有表现,但决定性区别在于角膜内皮的状态。角膜粉样变性中,角膜内皮镜显示角膜内皮细胞的形态和密度正常,而Fuchs则表现为Descemet膜上的赘疣(guttae)和内皮细胞密度降低。Fuchs进展可导致角膜水肿和大疱性角膜病变,但角膜粉样变性不影响视力。
角膜粉样变性无需治疗。由于不影响视力且无自觉症状,仅需随访观察。
伴有X连锁鱼鳞病时,也无需针对角膜表现进行治疗。以皮肤科管理为主。
由于该病是基于变性和遗传基础的疾病,目前尚无一级预防方法。
随着年龄增长,Descemet膜正前方的角膜基质细胞(keratocyte)胞质内积聚脂褐素样包涵体。组织病理学上表现为含有脂褐素样包涵体的胞质内空泡,有时导致角膜基质细胞异常肥大。
脂褐素是细胞内氧化应激导致的脂质过氧化产物,随年龄增长而积聚。选择性积聚于角膜基质深层角膜基质细胞的机制尚未完全阐明。
STS基因突变导致的类固醇硫酸酯酶缺乏会引起胆固醇硫酸酯代谢障碍。积聚的胆固醇硫酸酯沉积于角膜基质细胞内,呈现与年龄相关性角膜粉样变性类似的粉尘状混浊。STS定位于细胞内质网,可能与组织病理学所见脂褐素样沉积物的形成有关。
XLI中的角膜沉积物往往比年龄相关性变化出现得更早,且分布更广泛。有观点指出XLI与年龄相关性角膜粉样变性可能具有共同的病理生理基础,但详细机制仍需进一步研究3)。