โรคมูคอร์ไมโคซิสของเบ้าตาเป็นการติดเชื้อราที่ร้ายแรงจากอันดับ Mucorales ซึ่งลุกลามอย่างรวดเร็วจากโพรงจมูกไปยังเบ้าตา และสมอง ชนิดจมูก-เบ้าตา -สมอง (ROCM) รุนแรงที่สุด อัตราตายหากไม่รักษาสูงถึง 79%
โรคเบาหวาน (โดยเฉพาะภาวะกรดคีโตนจากเบาหวาน) เป็นปัจจัยเสี่ยงสำคัญที่สุด พบใน 58.9–86.7% ของผู้ป่วย
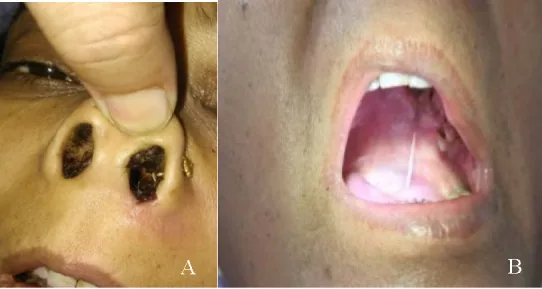
เนื้อเยื่อบุโพรงจมูกตายสีดำ (black eschar) เป็นสัญญาณเริ่มต้นที่จำเพาะ ต้องไม่พลาด
ความรุนแรงของการลุกลามเข้าสู่เบ้าตา ประเมินโดยการจำแนกของ Chandler (กลุ่ม 1–5) กลุ่ม 3 ขึ้นไปมักต้องผ่าตัด
การวินิจฉัยแน่นอนอาศัยการตัดชิ้นเนื้อและเพาะเชื้อ แต่การหาลำดับดีเอ็นเอเมตาจีโนมยุคถัดไป (mNGS) มีประโยชน์ในกรณีที่วิธีปกติให้ผลลบ
การรักษาหลักคือ amphotericin B แบบไลโปโซม (L-AMB) และควรทราบว่า voriconazole ไม่ได้ผลกับโรคมูคอร์ไมโคซิส
การวินิจฉัยล่าช้าอันตรายถึงชีวิต หากล่าช้าเกิน 6 วัน อัตราตายเพิ่มขึ้นประมาณ 2 เท่า
โรคมูคอร์ไมโคซิสของเบ้าตา (Orbital Mucormycosis) คือการติดเชื้อราที่ลุกลามซึ่งเกิดจากราอันดับ Mucorales แทรกซึมเข้าเนื้อเยื่อเบ้าตา จากโพรงจมูกและไซนัส ชนิดจมูก-เบ้าตา -สมอง (ROCM) สำคัญที่สุด สกุล Rhizopus (โดยเฉพาะ Rhizopus oryzae) พบประมาณ 85–90% ของกรณีจมูก-สมอง เดิมเรียกว่า zygomycosis ของเบ้าตา
รา Mucorales มีการแทรกซึมเนื้อเยื่อสูง แม้รอยโรคเล็กที่ปลายเบ้าตา ก็อาจทำให้เกิดความผิดปกติของการเคลื่อนไหวตาที่ไม่สามารถฟื้นคืนและการสูญเสียการมองเห็น อุบัติการณ์โดยประมาณต่อปีคือ 1.7 ต่อล้านคน 8) ในอินเดียรายงานสูงกว่าประเทศพัฒนาแล้ว 80 เท่า 9) ในยุโรปรายงาน 0.2–3 ต่อล้านคน 4) อัตราตายรวมเกิน 50% ไม่รักษา 79% รักษาประมาณ 40.5% การเกี่ยวข้องกับระบบประสาทส่วนกลางในผู้ป่วยเบาหวานที่ควบคุมน้ำตาลไม่ดีสูงถึง 33–49% 8)
Q
โรคมูคอร์ไมโคซิสของเบ้าตา (ชนิดจมูก-เบ้าตา-สมอง) พบบ่อยแค่ไหน?
A
อัตราการเกิดโรคโดยประมาณต่อปีคือ 1.7 ต่อล้านคน 8) ในอินเดีย มีรายงานอัตราการเกิดสูงกว่าประเทศที่พัฒนาแล้วถึง 80 เท่า โดยมีความแตกต่างในแต่ละภูมิภาคอย่างมาก ความเสี่ยงในการเกิดโรคเพิ่มขึ้นอย่างมีนัยสำคัญในผู้ป่วยโรคเบาหวาน มะเร็งเม็ดเลือด หรือภาวะภูมิคุ้มกันบกพร่อง ตั้งแต่การระบาดของโควิด-19 จำนวนผู้ป่วยเพิ่มขึ้นอย่างรวดเร็ว โดยเฉพาะในอินเดีย 6)
โรคมูคอร์ไมโคซิสของเบ้าตาจำแนกตามขอบเขตการลุกลามออกเป็น 3 ชนิดดังต่อไปนี้
ชนิดจำกัดเฉพาะเบ้าตา : การลุกลามจากโพรงอากาศข้างจมูกเข้าสู่เบ้าตา (ระยะแรกสุด)ชนิดจมูก-เบ้าตา : การลุกลามเข้าไปในโพรงจมูก โพรงอากาศข้างจมูก และเบ้าตา ชนิดจมูก-เบ้าตา -สมอง (ROCM) : การลุกลามเข้าไปในโพรงจมูก โพรงอากาศข้างจมูก เบ้าตา และภายในกะโหลกศีรษะ (รุนแรงที่สุด)
ความรุนแรงของการแพร่กระจายของการอักเสบเข้าสู่เบ้าตา ประเมินโดยใช้การจำแนกตามแชนด์เลอร์
การจำแนกตามแชนด์เลอร์ พยาธิสภาพ กลุ่ม 1 การอักเสบก่อนผนังกั้น (รอบเบ้าตา ) กลุ่ม 2 การอักเสบแทรกซึมภายในเบ้าตา กลุ่ม 3 ฝีใต้เยื่อหุ้มกระดูก กลุ่ม 4 ฝีในเบ้าตา กลุ่ม 5 ลิ่มเลือดในโพรงเลือดดำคาเวอร์นัส
ในกลุ่ม 3 ขึ้นไป ควรพิจารณาการผ่าตัดรักษาอย่างจริงจัง และกลุ่ม 5 แสดงถึงการลุกลามเข้าสู่กะโหลกศีรษะที่รุนแรงที่สุด
สะเก็ดดำเนื้อตาย (black eschar) ที่โพรงจมูกส่วนหน้าและเนื้อตายของเยื่อบุเพดานปาก Diaconescu DL, Diaconescu MR, Dumitrescu GF, et al. Rhinocerebral Mucormycosis—A Sight-Threatening Emergency. Rom J Ophthalmol. 2021 Oct-Dec; 65(4):339-353. Figure 1. PM
CI D: PMC8764427. License: CC BY.
(A) สะเก็ดดำเนื้อตาย (black eschar) ติดอยู่ที่โพรงจมูกส่วนหน้าซ้าย (B) ภาพถ่ายทางคลินิกแสดงรอยโรคเนื้อตายที่เพดานแข็ง สอดคล้องกับ black eschar ซึ่งเป็นลักษณะเฉพาะของระยะไซนัสที่กล่าวถึงในหัวข้อ “2. อาการหลักและอาการแสดงทางคลินิก”
อาการไซนัสอักเสบ: คัดจมูก น้ำมูกไหล เลือดกำเดาไหล
ปวดศีรษะ (ปวดใบหน้า ปวดบริเวณหน้าผาก)
การมองเห็น ลดลงจนถึงสูญเสียการมองเห็น เห็นภาพซ้อน จมูกอักเสบ หนังตาตก ข้างเดียว หนังตาบวม (อาการเริ่มแรก)
อ่อนเพลียและมีไข้
อาจแย่ลงอย่างรวดเร็วภายใน 1-2 วัน
อาการแสดงทางตาและทางระบบที่จำเพาะจะปรากฏตามระยะของโรคที่ดำเนินไป
ระยะไซนัส (ระยะเริ่มต้น)
เนื้อตายดำ/สะเก็ดดำ (black eschar) : ลักษณะเฉพาะที่พบในเยื่อบุไซนัส กังหันจมูก และเพดานปาก
การเกี่ยวข้องของไซนัสแม็กซิลลารีและเอทมอยด์ : ตำแหน่งที่พบบ่อยที่สุด
เนื้อตายที่ไม่มีภาวะเลือดคั่งเป็นลักษณะเฉพาะ ซึ่งแตกต่างจากการติดเชื้อทั่วไป
ระยะลุกลามเข้าสู่วงโคจร
ตาโปน (proptosis) : พบได้ 64-83% ของผู้ป่วย
อัมพาตกล้ามเนื้อนอกลูกตา จนถึงลูกตาค้าง (frozen globe) : อาการแสดงทางตาที่พบบ่อยที่สุด
หนังตาตก หนังตาบวม หนังตาเน่า
ระยะลุกลามเข้าสู่สมอง
กลุ่มอาการยอดเบ้าตา (OAS) : ร่วมกับลูกตาค้าง บ่งชี้การเกี่ยวข้องของเส้นประสาทสมองเป็นวงกว้าง อัตราตายสูง
ลิ่มเลือดในโพรงเลือดดำคาเวอร์นัส (cavernous sinus thrombosis) : เนื่องจากการไหลเวียนเลือดดำผิดปกติ
หลอดเลือดแดงจอประสาทตา ส่วนกลางอุดตัน (CRAO ) : พบจุดแดงเชอร์รี ่ (cherry-red spot) ที่จอตา
ใน ROCM ที่เกี่ยวข้องกับ COVID-19 ทุกรายพบ CRAO ภาวะตายื่น และกล้ามเนื้อตาอัมพาตทั้งหมด การพยากรณ์โรคแย่มาก (ผู้ป่วยทุกรายเสียชีวิต) 3) .
เชื้อราในอันดับ Mucorales โดยเฉพาะ Rhizopus oryzae เป็นสาเหตุหลัก เป็นราสายใยที่ไม่มีผนังกั้น (aseptate) เจริญเติบโตเร็ว พบมากในเขตร้อนและกึ่งร้อน เข้าสู่ร่างกายโดยการสูดดมสปอร์
เบาหวาน (โดยเฉพาะภาวะกรดคีโตนจากเบาหวาน) : ปัจจัยเสี่ยงสูงสุด (58.9–86.7%)มะเร็งทางโลหิตวิทยา (เช่น มะเร็งเม็ดเลือดขาวชนิดเฉียบพลันไมอีลอยด์) และภาวะนิวโทรพีเนีย
ประวัติการปลูกถ่ายไตและการรักษาด้วยยากดภูมิคุ้มกัน
การติดเชื้อเอชไอวี โรคไตเรื้อรัง และภาวะทุพโภชนาการ
โรคฮีโมโครมาโทซิสและการรักษาด้วยเดเฟอรอกซามีน
การติดเชื้อ COVID-19 : ความเสี่ยงเพิ่มขึ้นโดยเฉพาะเมื่อใช้สเตียรอยด์ หรือมีเบาหวานร่วม 6) 7) การนอน ICU เป็นเวลานานและการใช้ยาทางหลอดเลือดดำ
การให้ยาโวริโคนาโซลเพื่อป้องกัน (อาจกระตุ้นการเจริญเกินของเชื้อรา Mucorales) 4)
Q
การติดเชื้อ COVID-19 ทำให้เสี่ยงต่อโรคมูคอร์ไมโคซิสมากขึ้นหรือไม่?
A
ผู้ป่วยโรคมูคอร์ไมโคซิสบริเวณจมูก-เบ้าตา -สมองหลังติดเชื้อ COVID-19 เพิ่มขึ้นทั่วโลก โดยเฉพาะในอินเดียมีรายงาน 2,826 รายในปี 2021 6) เชื่อว่าพายุไซโตไคน์จาก COVID-19 ความผิดปกติของภูมิคุ้มกัน การใช้สเตียรอยด์ และน้ำตาลในเลือดสูง ส่งเสริมการเจริญเติบโตของเชื้อราแบบเสริมฤทธิ์กัน
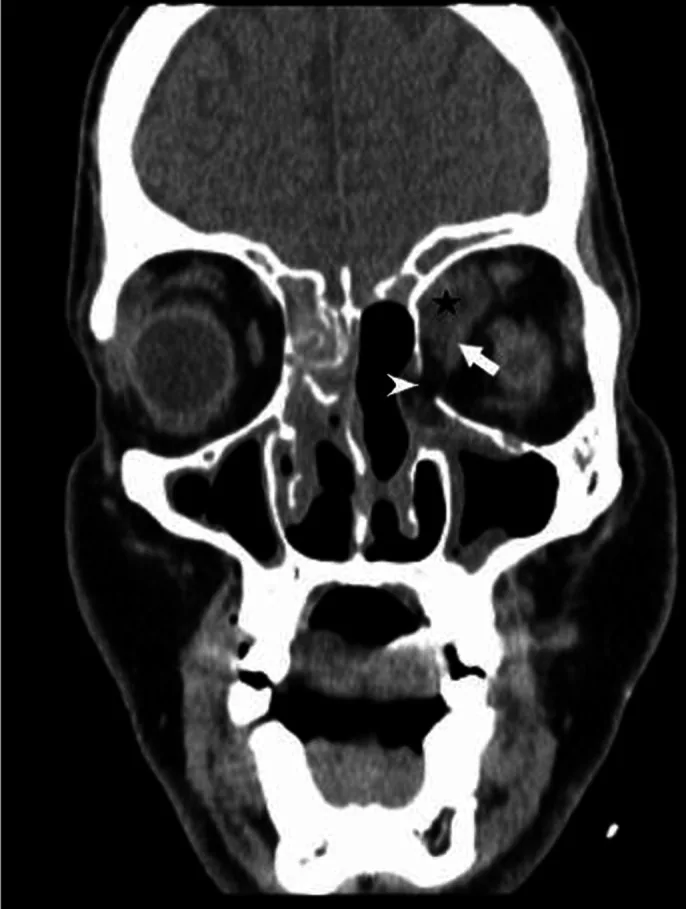
ภาพ CT scan โพรงอากาศข้างจมูกในโรคมูคอร์ไมโคซิส: การกร่อนของผนังกระดูกและการลุกลามของเนื้อเยื่ออ่อนเข้าสู่เบ้าตา Alghamdi AA, Alhazmi AS, Alsubhi FS, et al. Rhino-orbital-cerebral mucormycosis: A case report. BJR Case Rep. 2022 Mar 9; 7(6):20210111. Figure 4. PM
CI D: PMC8906162. License: CC BY.
ภาพ CT scan โพรงอากาศข้างจมูกแบบไม่ฉีดสีในแนวโคโรนัล พบความขุ่นในโพรงอากาศเอทมอยด์และแม็กซิลลารี การกร่อนของผนังกระดูก (arrowhead) และการแทรกซึมของเนื้อเยื่ออ่อนเข้าไปในเบ้าตา จนถึงกล้ามเนื้อเรกตัสมีเดียลิส (arrow) โดยสูญเสียชั้นไขมัน ภาพนี้สอดคล้องกับลักษณะ CT (การกร่อนกระดูก การลุกลามเข้าสู่เบ้าตา ) ที่กล่าวถึงในหัวข้อ “4. การวินิจฉัยและวิธีการตรวจ”
CT : มีประโยชน์ในการประเมินการกร่อนของผนังกระดูกโพรงอากาศและความขุ่นภายในโพรง ตำแหน่งที่พบบ่อยที่สุดคือโพรงอากาศแม็กซิลลารีและเอทมอยด์ ควรทำ CT แบบฉีดสี ในระยะแรกมักไม่พบความผิดปกติ ดังนั้นการตรวจซ้ำจึงสำคัญ โดยเฉพาะสังเกตสัญญาณของไซนัสอักเสบใกล้รอยโรค (เยื่อบุโพรงหนา, ความขุ่น)MRI :
ภาพ T1: รอยโรคสัญญาณเท่ากัน
ภาพ T2: สัญญาณต่ำ (สะท้อนเนื้อตาย)
สัญญาณกังหันดำ (Black Turbinate sign) : ในภาพ T1 ฉีดสี กังหันจมูกไม่ได้รับการเพิ่มสัญญาณ สะท้อนเนื้อตายและเป็นลักษณะเฉพาะ 5) การเกี่ยวข้องกับโพรงเลือดดำคาเวอร์นัส : ไม่มีการเพิ่มสัญญาณ
การตรวจพบจุดขาดเลือดในสมองที่พบบ่อยในสมองกลีบหน้าและเบซัลแกงเกลีย 5)
การตัดชิ้นเนื้อและการเพาะเชื้อเป็นมาตรฐานทองคำสำหรับการวินิจฉัยที่แน่นอน ในการตรวจทางจุลพยาธิวิทยา จะใช้การย้อม H&E, PAS และ GMS และลักษณะที่พบได้แก่ เส้นใยรากว้างคล้ายริบบิ้น ไม่มีผนังกั้น แตกแขนงเป็นมุมฉาก (90 องศา) การบุกรุกหลอดเลือด การเกิดลิ่มเลือด และเนื้อตาย 2) การระบุชนิดของเชื้อราด้วยการเพาะเชื้อก็มีความสำคัญต่อการเลือกใช้ยา แต่อัตราการเพาะเชื้อให้ผลบวกต่ำ การวินิจฉัยที่แน่นอนขึ้นอยู่กับการพิสูจน์เชื้อราจากการตรวจทางจุลพยาธิวิทยาหรือการเพาะเชื้อ
สามารถตรวจพบลำดับดีเอ็นเอของสกุล Rhizopus ในน้ำไขสันหลัง มีรายงานผลบวกในทั้ง 7 ราย (การเพาะเชื้อให้ผลลบทั้งหมด) มีประโยชน์อย่างยิ่งเมื่อวิธีการแบบดั้งเดิมให้ผลลบ
ลักษณะของวิธีการวินิจฉัยแสดงไว้ด้านล่าง
วิธีการตรวจ ลักษณะ ข้อควรระวัง การตัดชิ้นเนื้อ + การเพาะเชื้อ มาตรฐานทองคำสำหรับการวินิจฉัยที่แน่นอน อัตราการเพาะเชื้อให้ผลบวกต่ำ mNGS (น้ำไขสันหลัง) สามารถตรวจพบได้แม้ในกรณีที่เพาะเชื้อให้ผลลบ ต้องใช้สถานที่เฉพาะทาง β-D-กลูแคน และ GM เครื่องหมายเชื้อราประจำ ความไวต่อ Mucorales ต่ำ ไม่เหมาะสำหรับการวินิจฉัย
โรคแอสเปอร์จิลโลซิส (สำคัญที่สุด): เส้นใยรามีผนังกั้นและแตกแขนงเป็นมุม 45 องศาเป็นจุดที่ใช้แยกเซลลูไลติสของเบ้าตา (จากแบคทีเรีย)โรคแกรนูโลมาโทซิสกับโพลีแองจิอักเสบ (GP A)
การรักษาพื้นฐานคือการใช้ยาต้านเชื้อราร่วมกับการผ่าตัดตัดเนื้อตาย และควรทำการรักษาในแผนกอายุรกรรมเพื่อการจัดการทั้งระบบ การซึมผ่านของยาต้านเชื้อราเข้าไปในเนื้อเยื่อที่ตายแล้วไม่ดี ดังนั้นจึงจำเป็นต้องใช้ร่วมกับการผ่าตัด
ยา ตำแหน่ง ขนาดและวิธีใช้ แอมโฟเทอริซิน บี แบบไลโปโซม (L-AMB) ทางเลือกแรก ปกติ 5-7.5 มก./กก./วัน; กรณีที่มีการลุกลามถึงระบบประสาทส่วนกลาง 10 มก./กก./วัน โพซาโคนาโซล การรักษาแบบลดระดับหรือกู้ชีพ อัตราการตอบสนอง 60-70%2) ไอซาวูโคนาโซล การรักษาทางเลือก (ทนต่อยาได้ดี) 7) ขนาดยาเริ่มต้น 200 มก. แล้วตามด้วย 200 มก./วัน (รับประทาน) โวริโคนาโซล ไม่ได้ผลต่อโรคมูคอร์ไมโคซิส ไม่สามารถใช้ได้ (จุดแตกต่างสำคัญกับโรคแอสเปอร์จิลโลซิส)
ทางเลือกแรก: แอมโฟเทอริซิน บี ชนิดไลโปโซม (L-AMB) 2)
ขนาดปกติ: 5-7.5 มก./กก./วัน
กรณีที่มีการลุกลามถึงระบบประสาทส่วนกลาง: 10 มก./กก./วัน 1)
ระยะเวลาให้ยา: 3-36 เดือน (ขึ้นอยู่กับการดีขึ้นทางคลินิกและภาพถ่ายรังสี)
แอมโฟเทอริซิน บี ดีออกซีโคเลต มีพิษต่อไตสูงมาก จึงควรเลือกใช้สูตรไลโปโซม
โพซาโคนาโซล : การรักษาแบบ step-down หรือ salvage. อัตราการตอบสนอง 60-70% 2) .
ไอซาวูโคนาโซล : มีประสิทธิภาพเป็นทางเลือก ทนต่อยาได้ดี 7) . ขนาดยาเริ่มต้น 200 มก. แล้วตามด้วย 200 มก./วัน (รับประทาน).
การรักษาแบบผสม : การใช้แอมโฟเทอริซินร่วมกับแคสโปฟังจินมีรายงานว่าให้ผลลัพธ์ที่ดีกว่าการใช้ยาเดี่ยว แต่ฤทธิ์ในหลอดทดลองของเอไคโนแคนดินต่อเชื้อราในอันดับ Mucorales ต่ำ และไม่มีหลักฐานที่ชัดเจน 2) .
การผ่าตัดตัดเนื้อเยื่อที่ตายแล้วเป็นสิ่งจำเป็น ต้องตัดจนกว่าจะมีเลือดออกปกติ และแนะนำอย่างยิ่งให้ยืนยันขอบเขตการตัดทางพยาธิวิทยา การผ่าตัดไซนัสผ่านกล้องแบบส่องกล้องเพื่อการทำงาน (FES S) เป็นวิธีการผ่าตัดมาตรฐาน และอาจต้องผ่าตัดหลายครั้ง 4) การรักษาทางโสต ศอ นาสิกสำหรับไซนัสมักจำเป็นในผู้ใหญ่ โดยเฉพาะเมื่อมีการมองเห็น ลดลง การลดความดันในเบ้าตา เป็นสิ่งสำคัญ ในกรณีที่เกี่ยวข้องกับเบ้าตา อย่างกว้างขวาง อาจต้องผ่าตัดเอาสิ่งในเบ้าตา ออกพร้อมกับการเอาส่วนกระดูกออก
อัตราการเสียชีวิตของการใช้ยาต้านเชื้อราร่วมกับการผ่าตัดคือ 18.5% ในขณะที่การใช้ยาต้านเชื้อราเพียงอย่างเดียวคือ 60% ซึ่งสูงกว่าอย่างมีนัยสำคัญ 2)
การฉีด amphotericin B เข้าช่อง retrobulbar และ intravitreal (ขนาด intravitreal: 10 mcg/0.1 mL) 1)
การบำบัดด้วยออกซิเจนความดันสูง : ฤทธิ์ต้านเชื้อราและส่งเสริมการสร้างหลอดเลือดใหม่ในบริเวณที่ขาดเลือด 1)
การควบคุมระดับน้ำตาลในเลือดในผู้ป่วยเบาหวานและการแก้ไขภาวะกรดคีโตนจากเบาหวาน 7)
การแก้ไขภาวะกดภูมิคุ้มกัน (ลดยาภูมิคุ้มกันให้มากที่สุดเท่าที่เป็นไปได้)
การวินิจฉัยล่าช้าเกิน 6 วันเพิ่มอัตราการเสียชีวิตใน 30 วันจาก 35% เป็น 66% เพิ่มขึ้นประมาณสองเท่า หากสงสัย ให้เริ่มการรักษาทันที 6)
ยาตัวแรกสำหรับ mucormycosis คือ amphotericin B แบบ liposomal ส่วน voriconazole ไม่ได้ผลกับ mucormycosis บางครั้งอาจแยกจาก aspergillosis ได้ยาก แต่การระบุเชื้อก่อโรคมีความสำคัญอย่างยิ่งต่อการเลือกการรักษา
เนื่องจากการซึมผ่านของยาต้านเชื้อราไปยังเนื้อเยื่อที่ตายได้ไม่ดี การรักษาด้วยยาต้านเชื้อราเพียงอย่างเดียวจึงหายได้ยาก การใช้ร่วมกับการผ่าตัดตัดเนื้อเยื่อเป็นสิ่งจำเป็น
แม้จะใช้ยาในรูปแบบ liposomal ก็ต้องระวังพิษต่อไตและติดตามการทำงานของไตอย่างสม่ำเสมอ
Q
การรักษาใช้เวลานานเท่าใด?
A
ระยะเวลาในการให้ amphotericin B แบบ liposomal อยู่ระหว่าง 3 ถึง 36 เดือน ปรับตามการตอบสนองทางคลินิกและภาพถ่ายรังสีเป็นรายบุคคล 2) ในกรณีรุนแรงหรือมีการลุกลามไปยังสมอง มักต้องใช้ระยะเวลานานขึ้น การผ่าตัดตัดเนื้อเยื่ออาจต้องทำหลายครั้งเช่นกัน
Q
โวริโคนาโซลไม่ได้ผลต่อโรคมูคอร์มิโคซิสใช่หรือไม่?
A
โวริโคนาโซลเป็นยาต้านเชื้อราที่มีประสิทธิภาพสำหรับโรคแอสเปอร์จิลโลซิส แต่ไม่ได้ผลต่อโรคมูคอร์มิโคซิส (Mucorales) เนื่องจากทั้งสองโรคอาจแสดงอาการและอาการแสดงที่คล้ายคลึงกัน การระบุเชื้อก่อโรคจึงมีความสำคัญอย่างยิ่งต่อการเลือกการรักษา มีรายงานกรณีการติดเชื้อมูคอร์มิโคซิสแบบ breakthrough ระหว่างการให้โวริโคนาโซล 4) ดังนั้นจึงจำเป็นต้องระบุเชื้อราให้แน่ชัด
การสูดดมสปอร์ทำให้เกิดการเจริญเติบโตในโพรงอากาศข้างจมูก จากนั้นไปถึงเบ้าตา โดยการแทรกซึมโดยตรงหรือผ่านทางท่อน้ำตา จากเบ้าตา ไปยังสมองผ่านทางปลายเบ้าตา โพรงเลือดดำคาเวอร์นัส แผ่นคริบริฟอร์ม และหลอดเลือด
กลไกการแพร่กระจายหลักคือการบุกรุกหลอดเลือด (angioinvasion) โดยเจาะผ่านเซลล์บุผนังหลอดเลือดและโปรตีนเมทริกซ์นอกเซลล์ GRP 78 (glucose-regulated protein) มีส่วนร่วมในกระบวนการเจาะนี้ การดำเนินโรคเป็นไปตามเส้นทาง: การบุกรุกหลอดเลือด → การเกิดลิ่มเลือด → ภาวะขาดเลือด → เนื้อตายจากการขาดเลือด ส่งผลให้เกิดเนื้อตายโดยไม่มีภาวะเลือดคั่ง
ภายใต้สภาวะที่เป็นกรด ธาตุเหล็กจะถูกปลดปล่อยจากทรานสเฟอร์ริน และเชื้อรา Mucorales ใช้ธาตุเหล็กอิสระเพื่อเพิ่มจำนวนอย่างรวดเร็ว กลไกที่คล้ายกันนี้ยังเกิดขึ้นในภาวะธาตุเหล็กเกิน (hemochromatosis, การให้เลือดซ้ำๆ, การรักษาด้วย desferrioxamine)
พายุไซโตไคน์ (การเพิ่มขึ้นของ IL-1, IL-2, IL-6, TNF -α), การลดลงของการแสดงออกของ IFN-γ ในเซลล์ T CD4+, การใช้สเตียรอยด์ และยากดภูมิคุ้มกัน และการซ้อนทับของสภาพแวดล้อมที่ขาดออกซิเจน + น้ำตาลในเลือดสูง + เป็นกรด + ระดับธาตุเหล็กสูง ทำให้เกิดสภาพแวดล้อมที่เหมาะสำหรับการงอกของสปอร์เชื้อรา 7)
การอุดตันของหลอดเลือดแดงจอประสาทตา ส่วนกลาง : การอุดตันของหลอดเลือดโดยตรงหรือเส้นเลือดอุดตันจากการบุกรุกหลอดเลือดของเชื้อรา 3) ภาวะขาดเลือดของเส้นประสาทตา : การอุดตันของหลอดเลือดที่ปลายเบ้าตา ลิ่มเลือดในโพรงเลือดดำคาเวอร์นัส : การไหลเวียนเลือดดำบกพร่อง
Yang และคณะ (2026) รายงานผู้ป่วย ROCM 7 รายที่มีอาการเริ่มต้นเป็นภาวะสมองขาดเลือด 5) ตรวจพบ Rhizopus ในน้ำไขสันหลังด้วย mNGS ในทุกราย แต่การเพาะเชื้อให้ผลลบทั้งหมด ค่ามัธยฐานของเวลาจนถึงการวินิจฉัยคือ 5 วัน ผู้รอดชีวิตเพียงรายเดียวได้รับการวินิจฉัยภายใน 2 วัน (อัตราการเสียชีวิต 85.7%) mNGS เป็นเครื่องมือที่มีแนวโน้มสำหรับการวินิจฉัย ROCM ตั้งแต่เนิ่นๆ และมีคุณค่าโดยเฉพาะเมื่อการเพาะเชื้อและเครื่องหมายในซีรัมแบบดั้งเดิมให้ผลลบ
Q
การตรวจ mNGS มีประโยชน์ในสถานการณ์ใดบ้าง?
A
mNGS (การหาลำดับรุ่นถัดไปแบบเมทาจีโนมิกส์) มีประโยชน์เมื่อ β-D-glucan และ galactomannan มีความไวต่ำ และการเพาะเชื้อไม่สามารถระบุเชื้อก่อโรคได้ โดยเฉพาะใน ROCM ที่ไม่ปกติซึ่งมีอาการเริ่มต้นเป็นภาวะสมองขาดเลือด mNGS ของน้ำไขสันหลังอาจเป็นวิธีการวินิจฉัยเพียงวิธีเดียว 5)
หลังจากการเพิ่มขึ้นทั่วโลกของ ROCM ที่เกิดร่วมกับ COVID-19 Ostovan และคณะ (2021) รายงานว่าผู้ป่วยทุกรายที่มีประวัติใช้เครื่องช่วยหายใจเสียชีวิต 6) ในอินเดีย Sen และคณะ (2021) รายงานผู้ป่วย ROCM ที่เกี่ยวข้องกับ COVID-19 จำนวน 2,826 ราย ซึ่งเป็นที่สนใจในฐานะภาวะแทรกซ้อนร้ายแรงใหม่ในการระบาดใหญ่
Al Reesi และคณะ (2023) รายงานกรณีเด็กที่มีโรคไตเรื้อรังเฉียบพลันและภาวะทุพโภชนาการ ซึ่งหายขาดด้วยการรักษาเชิงรุกโดยใช้ amphotericin B liposomal (5→9 มก./กก./วัน) + posaconazole + การผ่าตัดหลายครั้ง 2) การวินิจฉัยตั้งแต่เนิ่นๆ ภายใน 24 ชั่วโมงและการรักษาเชิงรุกถือเป็นกุญแจสำคัญสู่ผลลัพธ์ที่ดี
Benlamkaddem S, Zdaik G, Doughmi D, et al. Rhino-Orbital Cerebral Mucormycosis: A Fatal Evolution. Cureus. 2023.
Al Reesi M, Al Muqbali T, Al Ajmi A, et al. Successful Management of Rhino-Orbital-Cerebral Mucormycosis in a Child with Acute-on-Chronic Kidney Disease and Malnutrition. Sultan Qaboos Univ Med J. 2023.
Kamath GM, Jeganathan S, Salim S, et al. Case series of central retinal artery occlusion in COVID-19-associated rhino-orbital-cerebral mucormycosis. Indian J Ophthalmol. 2023.
Siriwardena P, Wariyapperuma U, Nanayakkara P, et al. Rhino-orbital-cerebral mucormycosis in acute myeloid leukemia patients: a case series from Sri Lanka. BMC Infect Dis. 2024.
Yang F, Yang C, Li H, et al. Metagenomic next-generation sequencing in diagnosing rhino-orbital-cerebral mucormycosis presenting as cerebral infarction: a case series and diagnostic analysis of seven patients. Front Fungal Biol. 2026.
Ostovan VR, Rezapanah S, Behzadi Z, et al. Coronavirus disease (COVID-19) complicated by rhino-orbital-cerebral mucormycosis presenting with neurovascular thrombosis: a case report and review of literature. J Neurovirol. 2021.
Ponce-Rosas L, Gonzales-Zamora J, Diaz-Reyes N, et al. Rhino-Orbital-Cerebral Mucormycosis in a Post-COVID-19 Patient from Peru. Case Rep Infect Dis. 2022.
Alanazi RF, Almalki A, Alkhaibary A, et al. Rhino-Orbital-Cerebral Mucormycosis: A Rare Complication of Uncontrolled Diabetes. Case Rep Surg. 2022.
Mokhtar EA, Fatima Q, Akbar S, et al. Rhino-Orbital Cerebral Mucormycosis Causing Temporomandibular Joint Ankylosis: A Case Series of Two Patients. Cureus. 2023.