จุดแดงเชอร์รี ่เป็นลักษณะที่พบในจอประสาทตา ส่วนหลัง โดยที่รอยบุ๋มจอประสาทตา ปรากฏเป็นสีแดงท่ามกลางความขุ่นของจอประสาทตา สาเหตุที่พบบ่อยที่สุดคือการอุดตันของหลอดเลือดแดงจอประสาทตา ส่วนกลาง (CRAO ) ซึ่งพบได้ประมาณ 90% ของผู้ป่วยเมื่อวินิจฉัยครั้งแรก
CRAO เป็นภาวะฉุกเฉินที่เทียบเท่ากับโรคหลอดเลือดสมอง และความเสียหายของจอประสาทตา ที่ไม่สามารถฟื้นคืนได้จะเกิดขึ้นประมาณ 4 ชั่วโมงหลังจากเริ่มมีอาการในเด็ก โรคสะสมในไลโซโซมทางเมตาบอลิก (เช่น โรคเทย์-แซคส์, โรคเซียลิโดซิส) เป็นสาเหตุหลัก
ไม่มีการรักษาเฉียบพลันที่ได้มาตรฐาน อาจลองนวดลูกตา การเจาะช่องหน้าม่านตา และการตัดแก้วตา
ผู้ป่วย CRAO มีความเสี่ยงต่อโรคหลอดเลือดสมอง (12.9%) และกล้ามเนื้อหัวใจตาย (3.7%) หลังเข้ารับการรักษาในโรงพยาบาล จึงจำเป็นต้องตรวจร่างกายอย่างละเอียด
มีความแตกต่างทางเชื้อชาติ ในคนผิวขาวจะมีสีแดงสด ส่วนในคนที่ไม่ใช่ผิวขาวอาจมีสีน้ำตาลถึงดำ
จุดแดงเชอร์รี ่ (cherry-red spot; CRS ) เป็นลักษณะที่พบในจอประสาทตา ส่วนหลัง ตั้งชื่อตามลักษณะของรอยบุ๋มจอประสาทตา ที่ปรากฏเป็นสีแดงท่ามกลางความขุ่นของจอประสาทตา คล้ายผลเชอร์รี่สีแดง ในภาษาญี่ปุ่นเรียกว่า “ซากุระโคฮัน” (เม็ดเลือดแดงซากุระ)
ลักษณะนี้ถูกบรรยายครั้งแรกในปี ค.ศ. 1887 โดย Bernard Sachs ในฐานะลักษณะจอประสาทตา ของ “ภาวะสมองเสื่อมตาบอดในครอบครัว” (ปัจจุบันคือโรคเทย์-แซคส์) ปัจจุบันเป็นที่รู้จักอย่างกว้างขวางในฐานะสัญญาณทางคลินิกที่สำคัญซึ่งปรากฏในโรคต่างๆ เช่น CRAO และโรคสะสมในไลโซโซมต่างๆ
อุบัติการณ์ของ CRAO ประมาณ 1 ต่อ 100,000 คน 1) 1-2% ของผู้ป่วย CRAO เป็นสองข้าง ซึ่งบ่งชี้ถึงภาวะหลอดเลือดอักเสบ เช่น หลอดเลือดแดงอักเสบชนิดเซลล์ยักษ์ 10) นอกจากนี้ ประมาณ 60% ของการอุดตันของหลอดเลือดแดงจักษุก็พบ CRS เช่นกัน 9)
ลักษณะที่ปรากฏแตกต่างกันตามเชื้อชาติ ในคนผิวขาวจะมีสีแดงสด แต่ในคนที่ไม่ใช่ผิวขาวอาจมีสีน้ำตาลหรือดำ เนื่องจากความแตกต่างของปริมาณเม็ดสีในคอรอยด์ มีการเสนอคำศัพท์ทางเลือก “รอยขาวรอบรอยบุ๋มจอประสาทตา ” ด้วย
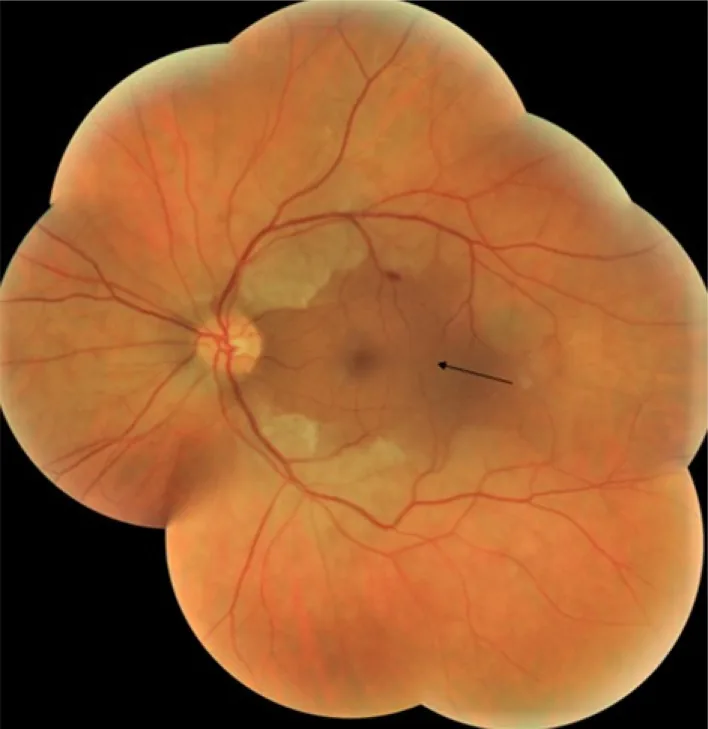
ภาพจุดแดงเชอร์รี่ Anis Mahmoud; Fatma Abid; Molka Khairallah; Fatma Sakji; Hassen Ibn Hadj Amor; Hala Attia. Case Report: Central retinal artery occlusion following sildenafil intake. F1000Res. 2022 Jun 1; 11:600 Figure 1. PM
CI D: PMC9490277. License: CC BY.
ภาพถ่ายจอประสาทตา พื้นฐานรวมของตาซ้ายแสดงให้เห็นจอประสาทตา ขาวขุ่น ยกเว้นบริเวณที่หลอดเลือดแดงซิลิโอเรตินาเลี้ยง (ลูกศรดำ)
จุดแดงเชอร์รี ่ (CRS ) ไม่ใช่โรคเดียว แต่เป็นอาการแสดงทางคลินิกที่เกิดจากภาวะทางพยาธิวิทยาที่แตกต่างกันหลายอย่าง สาเหตุแบ่งออกเป็น 4 กลุ่มใหญ่ ได้แก่ “หลอดเลือด” “โรคสะสมทางเมตาบอลิก” “ยา/สารพิษ” และ “การบาดเจ็บ/อื่นๆ”
หลอดเลือด (CRAO)
CRAO ชนิดไม่เกิดจากหลอดเลือดแดงอักเสบCRAO ทั้งหมด ชนิดของลิ่มเลือดอุดตัน: ลิ่มเลือดคอเลสเตอรอล 74%, ลิ่มเลือดเกล็ดเลือด-ไฟบริน 15.5%, ลิ่มเลือดแคลเซียม 10.5%2) โรคหลอดเลือดแดงคาโรติดพบร่วมในมากกว่า 70% ของกรณี (การศึกษา EAGLE)1)
CRAO ชนิดเกิดจากหลอดเลือดแดงอักเสบCRAO ทั้งสองข้าง ต้องแยกโรคนี้เสมอ10)
CRAO จากเยื่อบุหัวใจอักเสบติดเชื้อ9)
โรคสะสมทางเมตาบอลิก
โรคเทย์-แซคส์ : ขาดเอนไซม์เฮกโซซามินิเดส A ความถี่ของการพบ CRS 75-90%
GM1 gangliosidosis ชนิดที่ 1 : ขาดเอนไซม์ β-กาแลกโตซิเดส ความถี่ของการพบ CRS ประมาณ 50%
Sialidosis ชนิดที่ 1 : ขาดเอนไซม์นิวรามินิเดส (NEU1) พบ CRS ในเกือบทุกกรณี3) 5) อย่างไรก็ตาม ในกรณีที่มีอัลลีลคู่ของ NEU1 ที่กลายพันธุ์แบบไม่รุนแรง ก็มีรายงานว่าไม่มี CRS เช่นกัน5)
ยา/สารพิษ
ยายับยั้ง PDE5 (ซิลเดนาฟิล ฯลฯ) : มีรายงานผู้ป่วย CRAO หลังจากรับประทานซิลเดนาฟิลเกินขนาด 100 มก. × 2 เม็ด6) นอกจากนี้ FDA ยังมีรายงานการอุดตันของหลอดเลือดตาที่เกี่ยวข้องกับยายับยั้ง PDE5 สะสมจำนวนมาก
อื่นๆ : พิษจากควินิน, พิษจากคาร์บอนมอนอกไซด์ (CO) ฯลฯ
การบาดเจ็บ/อื่นๆ
Commotio retinae (จอประสาทตากระเทือน ) : หลังจากการฟกช้ำลูกตา จะเกิดความขุ่นของจอประสาทตา ที่ขั้วหลัง ทำให้เกิด CRS ปลอม
CRAO หลังวัคซีน COVID-19CRAO รายแรกของโลกหลังการฉีดวัคซีน Covaxin (วัคซีนเชื้อตายที่ผลิตในอินเดีย)8)
ภาวะพาหะของโรคเม็ดเลือดแดงรูปเคียว + เบาหวาน : การเกิดรูปเคียวของเม็ดเลือดแดงจากภาวะเครียดออกซิเดชัน อาจทำให้เกิดการอุดตันของหลอดเลือดแดงจอประสาทตา ส่วนกลาง 1)
สรุปความถี่ของการพบจุดแดงเชอร์รี ่ตามโรคสะสมทางเมตาบอลิก
ชื่อโรค เอนไซม์ที่บกพร่อง ความถี่ของ CRS โรคเทย์-แซคส์ เฮกโซซามินิเดส A 75-90% โรค GM1 แกงกลิโอซิโดซิสชนิดที่ 1 บีตา-กาแลกโตซิเดส ประมาณ 50% โรคไซอาลิโดซิสชนิดที่ 1 นิวรามินิเดส (NEU1) เกือบทุกกรณี
Q
จุดแดงเชอร์รี่สามารถเกิดขึ้นในเด็กได้หรือไม่?
A
ในเด็ก สาเหตุหลักคือโรคสะสมในไลโซโซม ในโรค Tay-Sachs พบ CRS ได้ 75-90% ของผู้ป่วย 5) เมื่อพบ CRS ในเด็กร่วมกับอาการทางระบบประสาท เช่น กล้ามเนื้อกระตุก (myoclonus) การเคลื่อนไหวไม่ประสานกัน (ataxia) และอาการชัก จำเป็นต้องตรวจหาโรคสะสมทางเมตาบอลิก
ในกรณี CRAO (จากหลอดเลือด):
การสูญเสียการมองเห็น เฉียบพลันในตาข้างเดียว: การมองเห็น ลดลงอย่างรวดเร็วโดยไม่เจ็บปวดภายในไม่กี่วินาที โดยปกติจะลดลงต่ำกว่า 0.1ภาวะตามัวชั่วคราว (amaurosis fugax): อาจมีอาการตามัวชั่วคราว เป็นนาทีก่อนเกิดอาการ
ในกรณีโรคสะสมในไลโซโซม:
กล้ามเนื้อกระตุก (myoclonus): การหดตัวของกล้ามเนื้อโดยไม่ตั้งใจ 3) การเคลื่อนไหวไม่ประสานกันและอาการชัก: อาการทางระบบประสาทรวมถึงอาการของสมองน้อยร่วมกับอาการทางตา 3)
การตรวจพบในจอตา:
จุดแดงเชอร์รี ่ (CRS ):รอยบุ๋มจอตา ใน CRAO พบได้ประมาณ 90% ของผู้ป่วยเมื่อวินิจฉัยครั้งแรกหลอดเลือดแดงจอตาตีบ: การตีบแคบของหลอดเลือดแดงจอตา 1) 4) 8) การขาดตอนของเลือด (boxcarring): การไหลเวียนเลือดในหลอดเลือดแดงจอตาขาดตอน ดูเป็นลูกปัด 4) 10) การมองเห็น สิ่งอุดตัน (แผ่น Hollenhorst):Roth spot : จุดเลือดออกที่มีจุดศูนย์กลางสีขาว ซึ่งพบในเยื่อบุหัวใจอักเสบติดเชื้อ2)
อาการทางจักษุอื่นๆ :
RAPD (Relative Afferent Pupillary Defect)เส้นประสาทตา ในตาข้างที่ได้รับผลกระทบ1) 2) 4)
ผลการตรวจทางภาพ :
OCT จอประสาทตา ชั้นในมีการสะท้อนแสงสูงและหนาตัวขึ้น1) 2) 6) 8) ระยะเรื้อรัง: ชั้นจอประสาทตา ชั้นในบางลงและฝ่อ1) 7) OCTA (Optical Coherence Tomography Angiography)6) FA (Fluorescein Angiography)1)
การตรวจทางจักษุ
การตรวจอวัยวะภายในลูกตา : ยืนยัน CRS ภายใต้การขยายม่านตา และประเมินหลอดเลือดแดงจอประสาทตา ตรวจสอบว่ามีสิ่งอุดตันหรือไม่
การประเมิน RAPD : การทดสอบด้วยไฟฉายสวิงเพื่อยืนยันความผิดปกติของรูม่านตา ชนิดอวัยวะนำเข้า
การวัดการมองเห็น และลานสายตา : เพื่อประเมินขอบเขตและความรุนแรงของการอุดตัน
การตรวจทางภาพ
OCT จอประสาทตา ชั้นใน ในโรคสะสมในไลโซโซม อาจตรวจพบการเปลี่ยนแปลงได้เร็วกว่าการตรวจอวัยวะภายในลูกตาทั่วไป5)
OCTA 6)
การตรวจฟลูออเรสซีน แองจิโอกราฟี (FA ) : ยืนยันรูปแบบการเติมเลือดของหลอดเลือดแดงที่ล่าช้า1) การเรืองแสงอัตโนมัติ (FAF ) มีประโยชน์ในการประเมินโรคสะสมในไลโซโซม5)
การตรวจร่างกายทั่วร่างกาย
การตรวจคลื่นเสียงสะท้อนหัวใจ (TEE) : การตรวจคลื่นเสียงสะท้อนหัวใจผ่านหลอดอาหารมีความไว 91-100% เหนือกว่าการตรวจผ่านผนังทรวงอก (TTE) ซึ่งมีความไว 44-63%2)
การตรวจคลื่นเสียงหลอดเลือดแดงคาโรติด : ประเมินการตีบและคราบพลัคของหลอดเลือดแดงคาโรติด4)
CTA/MRI (สมอง) : ยืนยันภาวะสมองขาดเลือดที่เกิดขึ้นพร้อมกัน4)
การตรวจระบบการแข็งตัวของเลือดและการแยกฮีโมโกลบินด้วยไฟฟ้า : ประเมินภาวะลิ่มเลือดอุดตันง่ายและภาวะพาหะของโรคเม็ดเลือดแดงรูปเคียว 1)
หากสงสัยโรคสะสมทางเมตาบอลิก :
การตรวจยีน NEU1 : ยืนยันจีโนไทป์ของโรคไซอะลิโดซิส5) การวัดกิจกรรมของเอนไซม์ : วัดกิจกรรมของเอนไซม์ไลโซโซมแต่ละชนิดเพื่อระบุชนิดของโรคสะสม3)
Q
จุดแดงเชอร์รี่เป็นภาวะฉุกเฉินหรือไม่?
A
ในกรณีหลอดเลือดแดงจอประสาทตา ส่วนกลางอุดตัน (CRAO ) ถือเป็นภาวะฉุกเฉินที่เทียบเท่ากับโรคหลอดเลือดสมอง ความเสียหายของจอประสาทตา ที่ไม่สามารถฟื้นคืนได้เกิดขึ้นประมาณ 4 ชั่วโมงหลังเริ่มมีอาการ7) และผู้ป่วยใน 12.9% มีโรคหลอดเลือดสมอง 3.7% มีกล้ามเนื้อหัวใจตาย4) เมื่อสังเกตเห็นอาการ จำเป็นต้องไปพบจักษุแพทย์หรืออายุรแพทย์ระบบประสาทฉุกเฉินทันที
ปัจจุบันยังไม่มีการรักษามาตรฐานที่พิสูจน์ประสิทธิภาพสำหรับ CRAO 9) มีการลองรักษาดังต่อไปนี้ แต่หลักฐานยังจำกัด
มีเพียงประมาณ 22% ของผู้ที่ไม่ได้รับการรักษาที่ดีขึ้นเองหลังจากเกิด CRAO 7) เวลาที่ประมาณว่าจะเกิดความเสียหายของจอประสาทตา ที่ไม่สามารถกลับคืนได้คือประมาณ 4 ชั่วโมง 7)
สรุปการรักษาที่ลองในระยะเฉียบพลัน
การรักษา วิธีการเฉพาะ หลักฐาน การนวดลูกตา การกดเป็นระยะด้วยนิ้ว ยังไม่เป็นที่ยอมรับ 9) การเจาะช่องหน้าม่านตา ลดความดันลูกตา โดยการระบายของเหลวในช่องหน้าม่านตา ยังไม่เป็นที่ยอมรับ 9) การตัดแก้วตา ลดความดันลูกตา + เพิ่มความดันหลอดเลือดแดง ระดับรายงานผู้ป่วย 7)
เกี่ยวกับการตัดแก้วตา ได้มีการรายงานเทคนิคที่รวมการลดความดันลูกตา ลงต่ำกว่า 3 มิลลิเมตรปรอท ร่วมกับการเพิ่มความดันหลอดเลือดแดงโดยการฉีดอะดรีนาลีน 0.1 มิลลิกรัมทางหลอดเลือดดำ Okonkwo และคณะได้ทำเทคนิคนี้ในผู้ป่วย CRAO ที่ไม่ใช่ชนิดหลอดเลือดแดงอักเสบ 2 ราย และรายงานการมองเห็น ดีขึ้นเป็น 6/60 และ 6/36+1 ตามลำดับ 7)
การบาดเจ็บจากการขาดเลือด-กลับมาเลือดไหล (IRI) เชื่อว่าเกิดขึ้นประมาณ 7 วันหลังจาก CRAO 7)
การป้องกันทุติยภูมิ :
ยาต้านเกล็ดเลือดและสแตติน : ให้แอสไพริน 150 มก./วัน + อะทอร์วาสแตติน 20 มก./คืน เป็นการป้องกันทุติยภูมิ 4)
CRAO ชนิดหลอดเลือดแดงอักเสบ (สงสัย GCA)สเตียรอยด์ ขนาดสูงทางหลอดเลือดดำอย่างเร่งด่วน 2) CRAO จากเยื่อบุหัวใจอักเสบติดเชื้อ2) 9) โรคสะสมทางเมตาบอลิก : ใช้ clonazepam, sodium valproate และ levetiracetam เพื่อควบคุมอาการกล้ามเนื้อกระตุก 5)
Q
การรักษา CRAO ช่วยให้การมองเห็นดีขึ้นหรือไม่?
A
ไม่มีการรักษาที่ได้มาตรฐาน และแม้ไม่ได้รับการรักษา ประมาณ 22% ของผู้ป่วยจะดีขึ้นเอง 7) 9) รายงานผู้ป่วยที่ได้รับการตัดแก้วตาบันทึกการมองเห็น ดีขึ้นเป็น 6/60 และ 6/36+1 7) แต่ไม่มีการทดลองเปรียบเทียบขนาดใหญ่ การตอบสนองตั้งแต่เนิ่นๆ หลังเริ่มมีอาการและการจัดการภาวะแทรกซ้อนทางระบบเป็นสิ่งสำคัญ
ในบริเวณจอตา ชั้นเซลล์ปมประสาทก่อตัวเป็นโครงสร้างหนาหลายชั้น เมื่อการไหลเวียนเลือดไปยังจอตาชั้นในหยุดชะงักเนื่องจากการอุดตันของหลอดเลือดแดงจอตาส่วนกลาง เซลล์ปมประสาทจะขาดเลือดและบวมอย่างรวดเร็ว และจอตาที่ขั้วหลังจะขุ่นเป็นสีขาวขุ่น
ในทางกลับกัน ชั้นเซลล์ประสาทปมประสาทไม่มีอยู่ในโฟวีโอลา (foveola) ดังนั้น โฟวีโอลาจึงได้รับสารอาหารโดยตรงจากการไหลเวียนของคอรอยด์ และคงความโปร่งใสไว้ ผลที่ได้คือ สีแดงของคอรอยด์ ปรากฏขึ้นที่โฟวีโอลาท่ามกลางบริเวณรอบข้างที่ขุ่นมัว—นี่คือสาเหตุของการเกิดจุดแดงเชอร์รี (CRS )
ใน 15–25% ของดวงตา มีหลอดเลือดแดงซิลิโอเรตินัล (cilioretinal artery) หลอดเลือดแดงนี้แตกแขนงมาจากการไหลเวียนของคอรอยด์ ซึ่งเป็นอิสระจากหลอดเลือดแดงจอประสาทตา ส่วนกลาง (CRA) ดังนั้น การมองเห็น ส่วนกลางอาจถูกสงวนไว้ในกรณีที่มีการอุดตันของหลอดเลือดแดงจอประสาทตา ส่วนกลาง (CRAO ) 10)
จอประสาทตา สามารถทนต่อภาวะขาดเลือดได้ประมาณ 97 นาที แต่ความเสียหายที่ไม่สามารถกลับคืนได้จะเกิดขึ้นหลังจาก 4 ชั่วโมง 7) การบาดเจ็บจากภาวะขาดเลือด-กลับมาเลี้ยงเลือดอีกครั้ง (IRI) เชื่อว่าเกิดขึ้นประมาณ 7 วันหลังจาก CRAO 7)
เนื่องจากการขาดเอนไซม์ในไลโซโซม ไขมันที่ยังไม่ถูกย่อยสลาย (เช่น แกงกลิโอไซด์, ไกลโคโปรตีนที่มีกรดเซียลิก) จึงสะสมภายในเซลล์ประสาทปมประสาท การสะสมนี้ทำให้ตัวเซลล์บวมขึ้น ทำให้ชั้นเซลล์ประสาทปมประสาทในบริเวณจอประสาทตา ส่วนกลาง (macula) ขุ่นมัว เนื่องจากไม่มีเซลล์ประสาทปมประสาทในโฟวีโอลา CRS จึงปรากฏขึ้นด้วยกลไกเดียวกับ CRAO
ในโรคเซียลิโดซิส (sialidosis) การกลายพันธุ์ของยีน NEU1 ทำให้เกิดการขาดนิวรามินิเดส (neuraminidase) และการสะสมของไกลโคโปรตีนที่มีกรดเซียลิก 3) 5) CRS อาจปรากฏขึ้นช้าเมื่อการสะสมเพิ่มขึ้น และในทางกลับกัน CRS จะไม่ชัดเจนเมื่อเซลล์ประสาทปมประสาทตายมากขึ้น 5) หากมีการกลายพันธุ์แบบไม่รุนแรงของ NEU1 ในทั้งสองอัลลีล CRS อาจไม่ปรากฏ 5)
สารยับยั้ง PDE5 จะเพิ่ม cGMP ซึ่งอาจทำให้การไหลเวียนเลือดในสมอง (CBF) ลดลงเนื่องจากความดันโลหิตทั่วร่างกายลดลง 6) นอกจากนี้ การเพิ่มขึ้นของ cGMP ในระยะยาวเชื่อว่าเปลี่ยนแปลงการซึมผ่านของเยื่อบุผนังหลอดเลือดและส่งเสริมการเกาะตัวของเกล็ดเลือดและการเกิดลิ่มเลือด 6)
Q
ในโรคเซียลิโดซิส จุดแดงเชอร์รีอาจไม่ปรากฏหรือไม่?
A
มีรายงานว่า CRS ไม่ปรากฏเมื่อมีการกลายพันธุ์แบบไม่รุนแรงของ NEU1 ในทั้งสองอัลลีล 5) แม้ในกรณีที่ CRS ไม่ชัดเจน OCT และการเรืองแสงอัตโนมัติ (FAF ) อาจตรวจพบความผิดปกติได้ไวขึ้น 5) ไม่ควรตัดโรคสะสมสารออกเพียงเพราะไม่มี CRS
Q
ลักษณะของจุดแดงเชอร์รีแตกต่างกันตามเชื้อชาติหรือไม่?
A
ในคนผิวขาว จะปรากฏเป็นสีแดงสด แต่ในคนที่ไม่ใช่ผิวขาว (เอเชีย แอฟริกา ฯลฯ) อาจมีลักษณะเป็นสีน้ำตาลถึงดำ ทั้งนี้เนื่องจากความแตกต่างของปริมาณเม็ดสีในคอรอยด์ และต้องใช้ความระมัดระวังในการตีความผลการตรวจ
เนื้อหาต่อไปนี้อยู่ในขั้นตอนการวิจัยหรือการทดลองทางคลินิกในปัจจุบัน และไม่ใช่การรักษามาตรฐานที่สามารถรับได้ในโรงพยาบาลทั่วไป เป็นข้อมูลอ้างอิงสำหรับผู้เชี่ยวชาญเกี่ยวกับการพัฒนาทางการแพทย์ในอนาคต
มีการรายงานการรักษาทางศัลยกรรม CRAO ที่ผสมผสานการตัดวุ้นตา กับการจัดการความดันลูกตา และความดันหลอดเลือดแดง
Okonkwo และคณะ (2021) รายงานผู้ป่วย CRAO ชนิดไม่ใช่หลอดเลือดแดงอักเสบ 2 รายที่ได้รับการตัดวุ้นตา (ลดความดันลูกตาต่ำ กว่า 3 มิลลิเมตรปรอท + เพิ่มความดันหลอดเลือดแดงด้วยการฉีดอะดรีนาลีน 0.1 มิลลิกรัมทางหลอดเลือดดำ) โดยมีการมองเห็น ดีขึ้นเป็น 6/60 และ 6/36+1 ตามลำดับ 7) เชื่อว่ายิ่งระยะเวลาตั้งแต่เริ่มมีอาการสั้นลง โอกาสฟื้นฟูการมองเห็น ก็จะสูงขึ้น
AHA/ASA ในแนวทางปฏิบัติปี 2021 แนะนำให้ปฏิบัติต่อ CRAO เสมือนโรคหลอดเลือดสมอง และตรวจทางระบบประสาทภายใน 72 ชั่วโมง
Zhong Yang และคณะ (2024) รายงานผู้ป่วย CRAO 1 รายที่มีภาวะสมองขาดเลือดร่วมด้วย และแสดงให้เห็นว่าความเสี่ยงโรคหลอดเลือดสมองหลังเข้ารับการรักษาในผู้ป่วย CRAO อยู่ที่ 12.9% ความเสี่ยงกล้ามเนื้อหัวใจตาย 3.7% และความเสี่ยงรวมของเหตุการณ์หัวใจและหลอดเลือด 19% 4) จำเป็นต้องมีความร่วมมือระหว่างทีมโรคหลอดเลือดสมองเฉพาะทางและจักษุวิทยา
Thakar และคณะ (2022) รายงานผู้ป่วยรายแรกของโลกที่เป็น CRAO หลังการฉีดวัคซีน Covaxin (วัคซีน COVID-19 ชนิดเชื้อตาย) 8) กรณีนี้ได้รับความสนใจในฐานะภาวะแทรกซ้อนทางหลอดเลือดที่เกี่ยวข้องกับวัคซีน และการชี้แจงความสัมพันธ์เชิงสาเหตุเป็นความท้าทายในอนาคต
Sahoo และคณะ (2023) ระบุการกลายพันธุ์ใหม่ของ NEU1 (c.544T>A, p.Y182N) ในโรคไซอะลิโดซิส และรายงานลักษณะทางคลินิกที่มีจุดแดงเชอร์รี และกล้ามเนื้อกระตุกเป็นอาการหลัก 3) Neeraja และคณะ (2021) รายงานผู้ป่วยไซอะลิโดซิสชนิดที่ 1 ที่มีการกลายพันธุ์ NEU1 เล็กน้อยซึ่งไม่มีจุดแดงเชอร์รี และแสดงให้เห็นว่า OCT และการเรืองแสงอัตโนมัติมีประโยชน์ในการวินิจฉัย 5) การวิเคราะห์ความสัมพันธ์ระหว่างจีโนไทป์และฟีโนไทป์กำลังก้าวหน้า
Semidey VA, Nortley E, Semidey AL, et al. Central retinal artery occlusion in a young patient with sickle cell trait. Cureus. 2023;15(2):e34865.
Chawla H, Garg U, Gupta A, et al. Central retinal artery occlusion with intracranial hemorrhage secondary to Streptococcus gordonii endocarditis. Case Rep Ophthalmol Med. 2023;2023:9268480.
Sahoo LK, Mohapatra S, Jena RK, et al. Novel NEU1 variant in sialidosis presenting with cherry-red spot. Neurology. 2023;101(19):861-862.
Zhong Yang L, Yaqoob T, Tan X, et al. Central retinal artery occlusion with concurrent ischemic stroke: a case report. Cureus. 2024;16(2):e53577.
Neeraja K, Rukmini AV, Pal PK, et al. Sialidosis type I without cherry red spot: a diagnostic challenge. J Mov Disord. 2021;14(1):65-69.
Abrishami M, Poorzand H, Shoeibi N, et al. Central retinal artery occlusion associated with sildenafil overdose. Case Rep Ophthalmol Med. 2021;2021:2006271.
Okonkwo ON, Hassan AO , Alaribe I, et al. Vitrectomy for nonarteritic central retinal artery occlusion. Taiwan J Ophthalmol. 2021;11(3):305-311.
Thakar M, Bharti N, Chandravanshi LP. Central retinal artery occlusion after Covaxin vaccination: a case report. Indian J Ophthalmol. 2022;70(10):3716-3718.
Mohamed M, Alsawidi K, Elhousseini Z, et al. Bilateral central retinal artery occlusion in infective endocarditis. J VitreoRetinal Dis. 2021;5(3):261-265.
American Academy of Ophthalmology. Retinal and ophthalmic artery occlusions preferred practice pattern. AAO ; 2024.
ถาม AI เกี่ยวกับบทความนี้
คัดลอกข้อความบทความแล้ววางในผู้ช่วย AI ที่คุณต้องการใช้
เปิดผู้ช่วย AI ด้านล่าง แล้ววางข้อความที่คัดลอกลงในช่องแชต