血管性(CRAO)

櫻桃紅點
一目瞭然的要點
Section titled “一目瞭然的要點”1. 什麼是櫻桃紅點?
Section titled “1. 什麼是櫻桃紅點?”櫻桃紅點(cherry-red spot; CRS)是後極部眼底所見之一。在視網膜白濁的混濁中,僅中心窩部分呈紅色調,外觀類似櫻桃的紅色果實,因而得名。日語中也稱為「桜実紅斑」。
此所見於1887年由Bernard Sachs首次描述為「家族性黑蒙性白痴」(現稱泰-薩克斯病)的眼底所見。目前被廣泛認為是出現在CRAO及各種溶酶體儲積症等多種疾病中的臨床重要徵象。
CRAO的發生率約為每10萬人1例1)。1-2%的CRAO為雙側性,提示巨細胞動脈炎(GCA)等血管炎10)。此外,約60%的眼動脈阻塞(OAO)也出現CRS9)。
外觀因種族而異:白人呈鮮紅色,非白人可能呈棕色或黑色調。這是由於脈絡膜色素量的差異。也有人提出替代術語「中心凹周圍白斑」。
2. 呈現櫻桃紅點的疾病和原因
Section titled “2. 呈現櫻桃紅點的疾病和原因”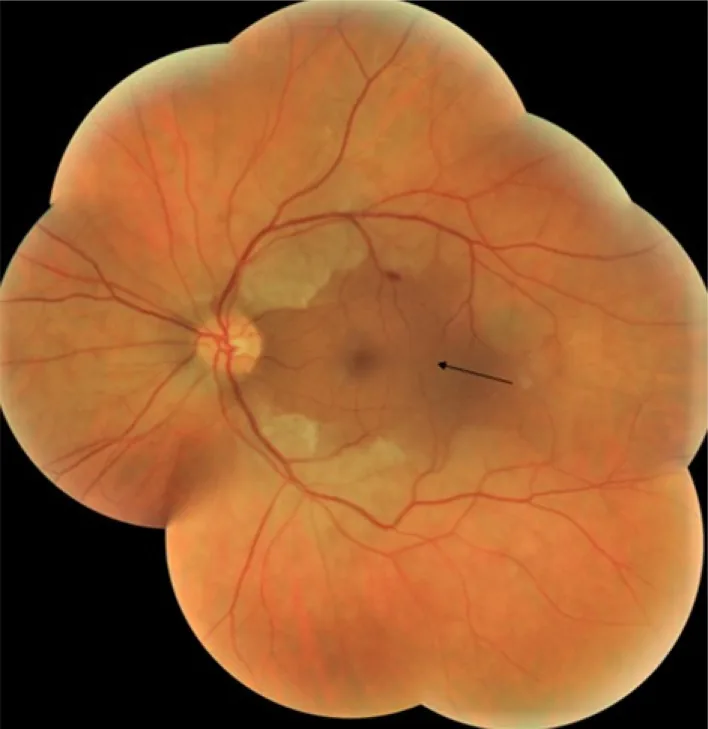
CRS不是單一疾病,而是由多種不同病理狀態引起的臨床徵兆。原因大致分為四類:「血管性」、「代謝性儲積症」、「藥物/毒性」和「外傷/其他」。
代謝性儲積症
泰-薩克斯病:己糖胺酶A缺乏。CRS出現頻率75-90%。
GM1神經節苷脂儲積症1型:β-半乳糖苷酶缺乏。CRS出現頻率約50%。
唾液酸儲積症1型:神經氨酸酶(NEU1)缺乏。幾乎所有病例都出現CRS 3)5)。但NEU1輕度突變純合子也有CRS缺失的報導 5)。
藥物/毒性
PDE5抑制劑(西地那非等):有報導過量服用西地那非100mg×2錠後發生CRAO的病例 6)。FDA也累積了大量與PDE5抑制劑相關的眼血管阻塞報告。
其他:奎寧中毒、一氧化碳(CO)中毒等。
外傷/其他
總結不同代謝性儲積症的CRS出現頻率。
| 疾病名稱 | 缺陷酶 | CRS頻率 |
|---|---|---|
| 泰-薩克斯病 | 己糖胺酶A | 75~90% |
| GM1神經節苷脂儲積症1型 | β-半乳糖苷酶 | 約50% |
| 唾液酸儲積症1型 | 神經氨酸酶(NEU1) | 幾乎所有病例 |
在兒童中,溶酶體儲積症是主要原因。在泰-薩克斯病中,75-90%的病例出現CRS 5)。當兒童出現CRS並伴有肌陣攣、運動失調和痙攣等神經症狀時,需要進行代謝性儲積症的檢查。
3. 主要症狀和臨床所見
Section titled “3. 主要症狀和臨床所見”CRAO(血管性)病例:
- 急性單眼視力下降: 數秒內發生的無痛性急劇視力下降,通常降至0.1以下。
- 一過性黑蒙(amaurosis fugax): 發病前可能出現持續數分鐘的一過性視力喪失。
溶酶體儲積症病例:
- 肌陣攣: 不自主的肌肉收縮發作 3)。
- 運動失調和痙攣: 包括小腦症狀在內的神經學表現與眼部症狀並存 3)。
眼底所見:
- 櫻桃紅點(CRS): 後極部視網膜白濁(混濁)與中心凹紅色調形成對比。在CRAO中,初診時約90%可見。
- 視網膜動脈變細: 視網膜動脈狹窄 1)4)8)。
- 血流中斷(boxcarring): 視網膜動脈內血流中斷,呈串珠狀外觀 4)10)。
- 可見栓子(霍倫霍斯特斑): 可能可見膽固醇栓子(20-40%)。
- Roth斑:感染性心內膜炎引起的白色中心出血斑2)。
其他眼科表現:
- RAPD(相對傳入性瞳孔反應缺陷):反映患眼視神經損傷1)2)4)。
影像學檢查所見:
- OCT:急性期內層視網膜高反射和增厚1)2)6)8)。慢性期內層視網膜變薄和萎縮1)7)。
- OCTA(光學同調斷層掃描血管成像):表層和深層毛細血管叢血流消失6)。
- FA(螢光素眼底血管造影):動脈充盈延遲1)。
4. 診斷和檢查方法
Section titled “4. 診斷和檢查方法”眼科檢查
影像學檢查
OCT:評估急性期內層視網膜高反射和慢性期變薄。在溶酶體貯積症中,可能比常規眼底檢查更早發現早期變化5)。
OCTA:非侵入性評估血流消失區域6)。
FA:確認動脈充盈延遲模式1)。自體螢光(FAF)有助於評估溶酶體儲積症5)。
全身檢查
心臟超音波(TEE):經食道心臟超音波敏感度為91-100%。優於經胸心臟超音波(TTE),後者敏感度為44-63%2)。
頸動脈超音波:評估頸動脈狹窄和斑塊4)。
CTA/MRI(腦):確認同時存在的腦梗塞4)。
凝血功能檢查和Hb電泳:評估血栓形成傾向和鐮狀細胞特質1)。
如果懷疑代謝性儲積症:
- NEU1基因檢測:確認唾液酸儲積症的基因型5)。
- 酶活性測定:測量各溶酶體酶的活性,以確定儲積症的類型3)。
在CRAO中,這是與中風同等的緊急情況。不可逆的視網膜損傷在發病後約4小時發生7),住院患者中12.9%合併中風,3.7%合併心肌梗塞4)。一旦發現症狀,需要立即到眼科和神經內科急診就診。
5. 標準治療方法
Section titled “5. 標準治療方法”CRAO的急性期治療
Section titled “CRAO的急性期治療”目前,對於CRAO尚無已確立有效性的標準治療方法9)。以下治療方法可嘗試,但證據均有限。
CRAO發病後,未經治療的患者中僅約22%會自然改善7)。發生不可逆視網膜損傷的時間約為4小時7)。
急性期嘗試的治療方法總結如下。
| 治療方法 | 具體方法 | 證據 |
|---|---|---|
| 眼球按摩 | 指壓間歇加壓 | 未確立9) |
| 前房穿刺 | 通過排出房水降低眼壓 | 未確立9) |
| 玻璃體切除術 | 降低眼壓+升高動脈壓 | 病例報告等級7) |
關於玻璃體切除術,已有報告一種術式,將眼壓降至3 mmHg以下,同時靜脈注射0.1 mg腎上腺素以升高動脈壓。Okonkwo等人對兩例非動脈炎性CRAO患者施行此術式,報告視力分別改善至6/60和6/36+1 7)。
缺血再灌注損傷(IRI)被認為發生在CRAO後約7天 7)。
次級預防:
- 抗血小板藥與史他汀:阿斯匹靈150 mg/日加上阿托伐他汀20 mg/晚用於次級預防 4)。
- 動脈炎性CRAO(疑似GCA):緊急開始大劑量靜脈類固醇治療 2)。
- 感染性心內膜炎引起的CRAO:基礎治療為6週抗生素;若贅生物超過15 mm,考慮瓣膜置換術 2)9)。
- 代謝性儲積症:使用克羅那西泮、丙戊酸鈉和左乙拉西坦控制肌陣攣 5)。
沒有確立的治療方法,約22%的未治療病例會自然改善 7)9)。玻璃體切除術的病例報告記錄了視力恢復至6/60或6/36+1 7),但缺乏大規模比較試驗。發病後的早期處理和全身併發症的管理很重要。
6. 病理生理學與詳細發病機制
Section titled “6. 病理生理學與詳細發病機制”CRAO中的櫻桃紅斑
Section titled “CRAO中的櫻桃紅斑”在黃斑部,神經節細胞層形成多層堆積的厚結構。視網膜中央動脈(CRA)閉塞導致內層視網膜血流中斷時,神經節細胞迅速缺血並腫脹,後極部視網膜呈現乳白色混濁。
在中心凹(foveola)處,沒有神經節細胞層。因此,中心凹直接從脈絡膜循環獲得營養並保持透明。結果,在周圍混濁的視網膜中,中心凹的紅色(脈絡膜的紅色)色調浮現出來——這就是櫻桃紅點的成因。
15%至25%的眼睛存在睫狀視網膜動脈。該動脈從脈絡膜循環獨立於中央視網膜動脈分支,因此在CRAO時,中心視力有時得以保留10)。
視網膜可耐受約97分鐘的缺血,但超過4小時則發生不可逆損傷7)。缺血再灌注損傷(IRI)被認為發生在CRAO後約7天7)。
代謝性儲積症中的櫻桃紅點
Section titled “代謝性儲積症中的櫻桃紅點”由於溶酶體酶缺陷,未降解的脂質(如神經節苷脂、唾液酸化糖蛋白等)在神經節細胞內積聚。這種積聚使細胞體腫脹,導致黃斑部神經節細胞層混濁。由於中心凹沒有神經節細胞,因此與CRAO相同的機制出現櫻桃紅點。
在唾液酸沉積症中,NEU1基因突變導致神經氨酸酶缺乏,唾液酸化糖蛋白積聚3)5)。櫻桃紅點可能隨著積聚量增加而延遲出現,反之,隨著神經節細胞死亡進展,櫻桃紅點變得不明顯5)。如果兩個等位基因均存在NEU1輕症突變,則可能缺乏櫻桃紅點5)。
藥物性(如西地那非等)CRAO
Section titled “藥物性(如西地那非等)CRAO”PDE5抑制劑升高cGMP,可能因全身血壓下降導致腦血流(CBF)減少6)。此外,長期cGMP升高被認為會改變內皮通透性,促進血小板黏附和血栓形成6)。
據報導,當NEU1基因的兩個等位基因均存在輕症突變時,可能缺乏櫻桃紅點5)。即使在櫻桃紅點不明顯的病例中,OCT或自體螢光(FAF)也可能更敏感地檢測到異常5)。不能僅因缺乏櫻桃紅點就排除儲積症。
在白人中,它呈現鮮紅色,但在非白人(如亞洲人、非洲人等)中,可能呈現棕色至黑色調。這是由於脈絡膜色素量的差異,解讀時需注意。
7. 最新研究與未來展望(研究階段報告)
Section titled “7. 最新研究與未來展望(研究階段報告)”CRAO外科治療的發展
Section titled “CRAO外科治療的發展”已有報告將玻璃體切除術與眼壓及動脈壓操作相結合的外科CRAO治療。
Okonkwo等人(2021)對兩例非動脈炎性CRAO患者進行玻璃體切除術(將眼壓降至3 mmHg以下,並靜脈注射0.1 mg腎上腺素升高動脈壓),報告視力分別改善至6/60和6/36+1 7)。一般認為發病後時間越短,視功能恢復的可能性越大。
CRAO的腦中風同等管理
Section titled “CRAO的腦中風同等管理”AHA/ASA在2021年指南中建議將CRAO視為腦中風同等對待,並在72小時內進行神經學檢查。
Zhong Yang等人(2024)報告了一例CRAO合併同時性腦梗塞的病例,顯示CRAO患者入院後中風風險為12.9%,心肌梗塞風險為3.7%,總心血管事件風險為19% 4)。需要中風專科團隊與眼科的協作。
COVID-19疫苗後CRAO
Section titled “COVID-19疫苗後CRAO”Thakar等人(2022)報告了全球首例接種Covaxin(滅活COVID-19疫苗)後發生CRAO的病例 8)。這作為疫苗相關的血管併發症受到關注,闡明因果關係是未來的課題。
唾液酸儲積症的基因型-表現型相關性
Section titled “唾液酸儲積症的基因型-表現型相關性”Sahoo等人(2023)在唾液酸儲積症中鑑定出一種新的NEU1突變(c.544T>A, p.Y182N),並報告了以櫻桃紅斑和肌陣攣為主要特徵的臨床表現 3)。Neeraja等人(2021)報告了一例攜帶NEU1輕症突變的1型唾液酸儲積症患者缺乏櫻桃紅斑,顯示OCT和自體螢光對診斷有用 5)。基因型與表現型的相關性分析正在進展中。
8. 參考文獻
Section titled “8. 參考文獻”- Semidey VA, Nortley E, Semidey AL, et al. Central retinal artery occlusion in a young patient with sickle cell trait. Cureus. 2023;15(2):e34865.
- Chawla H, Garg U, Gupta A, et al. Central retinal artery occlusion with intracranial hemorrhage secondary to Streptococcus gordonii endocarditis. Case Rep Ophthalmol Med. 2023;2023:9268480.
- Sahoo LK, Mohapatra S, Jena RK, et al. Novel NEU1 variant in sialidosis presenting with cherry-red spot. Neurology. 2023;101(19):861-862.
- Zhong Yang L, Yaqoob T, Tan X, et al. Central retinal artery occlusion with concurrent ischemic stroke: a case report. Cureus. 2024;16(2):e53577.
- Neeraja K, Rukmini AV, Pal PK, et al. Sialidosis type I without cherry red spot: a diagnostic challenge. J Mov Disord. 2021;14(1):65-69.
- Abrishami M, Poorzand H, Shoeibi N, et al. Central retinal artery occlusion associated with sildenafil overdose. Case Rep Ophthalmol Med. 2021;2021:2006271.
- Okonkwo ON, Hassan AO, Alaribe I, et al. Vitrectomy for nonarteritic central retinal artery occlusion. Taiwan J Ophthalmol. 2021;11(3):305-311.
- Thakar M, Bharti N, Chandravanshi LP. Central retinal artery occlusion after Covaxin vaccination: a case report. Indian J Ophthalmol. 2022;70(10):3716-3718.
- Mohamed M, Alsawidi K, Elhousseini Z, et al. Bilateral central retinal artery occlusion in infective endocarditis. J VitreoRetinal Dis. 2021;5(3):261-265.
- American Academy of Ophthalmology. Retinal and ophthalmic artery occlusions preferred practice pattern. AAO; 2024.
