혈관성 (CRAO)

체리 레드 스팟
한눈에 보는 포인트
섹션 제목: “한눈에 보는 포인트”1. 체리-레드 스팟이란?
섹션 제목: “1. 체리-레드 스팟이란?”체리-레드 스팟(cherry-red spot; CRS)은 후극부 안저 소견 중 하나이다. 망막이 백탁된 혼탁 속에서 중심와(foveola) 부분만 붉은 색조로 떠오르는 모양이 체리의 붉은 열매와 닮아 명명되었다. 일본어로는 ‘사쿠라지츠 코우한(벚꽃 열매 홍반)‘이라고도 불린다.
이 소견은 1887년 Bernard Sachs가 ‘가족성 흑내성 백치’(현재의 테이-삭스병)의 안저 소견으로 처음 기술했다. 현재는 CRAO 및 다양한 리소좀 축적 질환 등 여러 질환에서 나타나는 임상적으로 중요한 징후로 널리 인식되고 있다.
CRAO의 발생률은 10만 명당 약 1명으로 알려져 있다1). CRAO의 1~2%는 양측성이며, 이 경우 거대세포동맥염(GCA) 등의 혈관염을 시사한다10). 또한 안동맥폐쇄(OAO)의 약 60%에서도 CRS가 나타난다9).
인종에 따라 모양이 달라 백인에서는 선명한 적색을 띠지만, 비백인에서는 갈색이나 흑색조가 될 수 있다. 이는 맥락막의 색소량 차이에 기인한다. 대체 용어로 ‘중심와주위 백색 반점(perifoveal white patch)‘도 제안되었다.
2. 체리-레드 스팟을 나타내는 질환과 원인
섹션 제목: “2. 체리-레드 스팟을 나타내는 질환과 원인”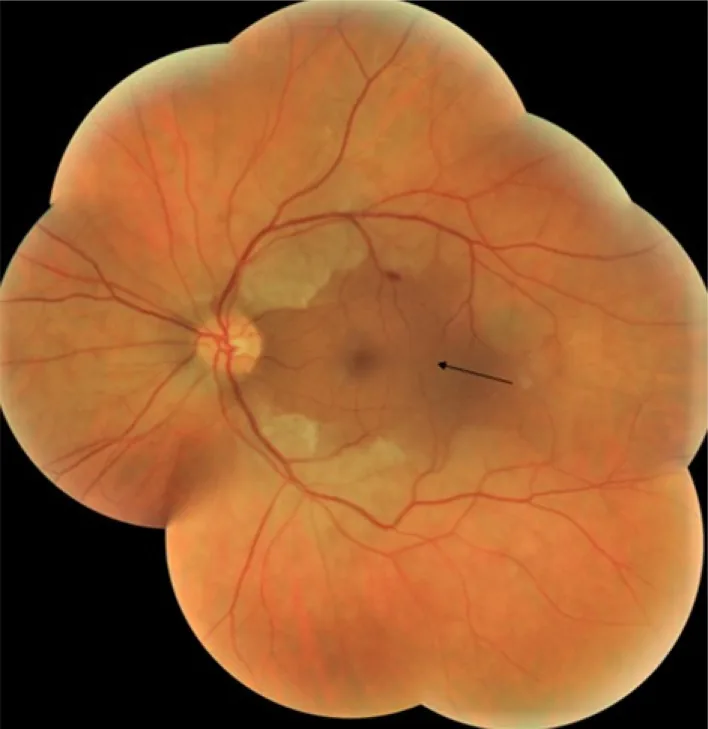
CRS는 단일 질환이 아니라 여러 다른 병태에서 발생하는 임상 징후입니다. 원인은 크게 “혈관성”, “대사성 축적 질환”, “약물/독성”, “외상/기타”의 4군으로 분류됩니다.
대사성 축적 질환
테이-삭스병: 헥소사미니다제 A 결핍. CRS 출현 빈도 75~90%.
GM1 강글리오시드증 1형: β-갈락토시다제 결핍. CRS 출현 빈도 약 50%.
시알리도시스 1형: 뉴라미니다제(NEU1) 결핍. 거의 모든 예에서 CRS가 나타납니다 3)5). 그러나 NEU1의 경증 변이 동형접합에서는 CRS가 없는 경우도 보고되었습니다 5).
약물/독성
PDE5 억제제(실데나필 등): 실데나필 100mg 2정 과량 복용 후 CRAO가 발생한 증례 보고가 있습니다 6). FDA에도 PDE5 억제제 관련 안혈관 폐쇄 보고가 다수 축적되어 있습니다.
기타: 퀴닌 중독, 일산화탄소(CO) 중독 등.
외상/기타
대사성 축적 질환별 CRS 출현 빈도를 요약합니다.
| 질환명 | 결핍 효소 | CRS 빈도 |
|---|---|---|
| 테이-삭스병 | 헥소사미니다제 A | 75~90% |
| GM1 강글리오시드증 1형 | β-갈락토시다제 | 약 50% |
| 시알리도시스 1형 | 뉴라미니다제 (NEU1) | 거의 모든 증례 |
소아에서는 리소좀 축적 질환이 주요 원인입니다. 테이-삭스병에서는 75-90%의 증례에서 CRS가 나타납니다 5). 소아에서 CRS가 근경련, 운동실조, 경련 등의 신경 증상과 함께 나타나는 경우 대사성 축적 질환에 대한 정밀 검사가 필요합니다.
3. 주요 증상 및 임상 소견
섹션 제목: “3. 주요 증상 및 임상 소견”자각 증상
섹션 제목: “자각 증상”CRAO(혈관성)의 경우:
- 급성 단안 시력 저하: 수초 내에 발생하는 통증 없는 급격한 시력 저하. 일반적으로 0.1 미만으로 떨어집니다.
- 일과성 흑암시(amaurosis fugax): 발병 전에 수분간의 일과성 시력 소실이 선행될 수 있습니다.
리소좀 축적 질환의 경우:
- 근경련: 불수의적 근수축 발작 3).
- 운동실조 및 경련: 소뇌 증상을 포함한 신경학적 소견이 안구 증상과 공존합니다 3).
임상 소견
섹션 제목: “임상 소견”안저 소견:
- 체리-레드 스팟(CRS): 후극부 망막 백탁(혼탁)과 중심와의 붉은 색조의 대비. CRAO에서는 초진 시 약 90%에서 관찰됩니다.
- 망막 동맥 세선화: 망막 동맥의 협소화 1)4)8).
- 혈류 단절(boxcarring): 망막 동맥 내 혈류가 단절되어 염주 모양으로 보이는 소견 4)10).
- 색전의 시인(홀렌호르스트 플라크): 콜레스테롤 색전이 관찰되는 경우가 있습니다(20-40%).
- Roth 반점: 감염성 심내막염에서 나타나는 흰색 중심 출혈반2).
기타 안과적 소견:
- RAPD (상대적 구심성 동공 반응 장애): 환안의 시신경 손상을 반영1)2)4).
영상 검사 소견:
- OCT: 급성기에는 내층 망막의 고반사 및 비후1)2)6)8). 만성기에는 내층 망막의 얇아짐 및 위축1)7).
- OCTA (광간섭단층혈관조영술): 표층 및 심층 모세혈관총의 혈류 소실6).
- FA (형광안저혈관조영술): 동맥 충만 지연1).
4. 진단 및 검사 방법
섹션 제목: “4. 진단 및 검사 방법”안과적 검사
안저 검사: 산동 하에서 CRS 확인 및 망막 동맥 평가. 색전 유무 확인.
RAPD 평가: 스윙 라이트 테스트를 통한 구심성 동공 장애 확인.
시력 및 시야 측정: 폐쇄의 범위와 중증도 파악.
영상 검사
OCT: 급성기 내층 망막 고반사와 만성기 얇아짐 평가. 리소좀 축적 질환에서는 일반 안저 검사보다 조기 변화를 더 일찍 포착할 수 있음5).
OCTA: 비침습적으로 혈류 소실 영역 파악6).
FA: 동맥 충만 지연 패턴 확인1). 자가형광(FAF)은 리소좀 축적 질환 평가에 유용함5).
전신 검사
심장 초음파(TEE): 경식도 심초음파의 민감도는 91100%입니다. 경흉부 심초음파(TTE)의 민감도 4463%와 비교하여 우수함2).
경동맥 초음파: 경동맥 협착 및 플라크 평가4).
CTA/MRI(뇌): 동시 뇌경색 확인4).
응고 검사 및 Hb 전기영동: 혈전 소인 및 겸상 적혈구 형질 평가1).
대사성 축적 질환이 의심되는 경우:
- NEU1 유전자 검사: 시알리도증의 유전자형 확정5).
- 효소 활성 측정: 각 리소좀 효소의 활성을 측정하여 축적 질환의 종류를 확정함3).
CRAO의 경우 뇌졸중과 동등한 응급 상황입니다. 비가역적 망막 손상은 발병 후 약 4시간 후에 발생하며7), 입원 환자의 12.9%가 뇌졸중, 3.7%가 심근경색을 동반합니다4). 증상이 발견되는 즉시 안과 및 신경과 응급 진료가 필요합니다.
5. 표준 치료법
섹션 제목: “5. 표준 치료법”CRAO의 급성기 치료
섹션 제목: “CRAO의 급성기 치료”현재 CRAO에 대해 효과가 입증된 표준 치료는 존재하지 않습니다9). 다음 치료법이 시도될 수 있으나, 각각의 근거는 제한적입니다.
CRAO 발병 후 자연 회복되는 경우는 치료하지 않은 환자의 약 22%에 불과합니다7). 비가역적 망막 손상이 발생하기까지의 시간은 약 4시간으로 알려져 있습니다7).
급성기에 시도되는 치료법을 요약합니다.
| 치료법 | 구체적인 방법 | 근거 |
|---|---|---|
| 안구 마사지 | 지압에 의한 간헐적 가압 | 확립되지 않음9) |
| 전방 천자 | 방수 배출을 통한 안압 하강 | 확립되지 않음9) |
| 유리체 절제술 | 안압 하강 + 동맥압 상승 | 증례 보고 수준7) |
유리체절제술에 관해서는 안압을 3mmHg 미만으로 낮추면서 아드레날린 0.1mg 정맥주사로 동맥압을 상승시키는 수술법이 보고되었습니다. Okonkwo 등은 비동맥염성 CRAO 2예에 이 수술법을 시행하여 각각 시력 6/60 및 6/36+1로의 개선을 보고했습니다 7).
허혈 재관류 손상(IRI)은 CRAO 후 약 7일에 발생하는 것으로 알려져 있습니다 7).
이차 예방:
- 항혈소판제 및 스타틴: 아스피린 150mg/일 및 아토르바스타틴 20mg/야간 투여가 이차 예방으로 시행됩니다 4).
원인별 치료
섹션 제목: “원인별 치료”- 동맥염성 CRAO (GCA 의심): 응급으로 고용량 스테로이드 정맥내 투여를 시작합니다 2).
- 감염성 심내막염 유래 CRAO: 항생제 6주 투여를 기본으로 하며, 사마귀가 15mm 초과 시 판막 치환술을 고려합니다 2)9).
- 대사성 축적 질환: 근경련 관리에 클로나제팜, 발프로산나트륨, 레베티라세탐이 사용됩니다 5).
확립된 치료법은 없으며, 무치료 예에서도 약 22%가 자연 호전됩니다 7)9). 유리체절제술의 증례 보고에서는 시력 6/60 또는 6/36+1로의 회복이 기록되었지만 7), 대규모 비교 시험은 없습니다. 발병 후 조기 대응과 전신 합병증 관리가 중요합니다.
6. 병태생리학 및 상세 발병 기전
섹션 제목: “6. 병태생리학 및 상세 발병 기전”CRAO에서의 체리-레드 스팟
섹션 제목: “CRAO에서의 체리-레드 스팟”황반부에서는 신경절 세포층이 여러 층으로 쌓인 두꺼운 구조를 이루고 있습니다. 망막중심동맥(CRA)의 폐쇄로 내층 망막으로의 혈류가 차단되면 신경절 세포가 급속히 허혈 및 세포 종창을 일으켜 후극부 망막이 유백색으로 혼탁해집니다.
중심와(foveola)에는 신경절세포층이 존재하지 않습니다. 따라서 중심와는 맥락막 순환으로부터 직접 영양을 공급받아 투명성을 유지합니다. 결과적으로, 혼탁해진 주변부 속에서 중심와의 붉은색(맥락막의 붉은색)이 두드러져 보이게 됩니다——이것이 체리적점의 원인입니다.
15~25%의 눈에는 섬모체망막동맥이 존재합니다. 이 동맥은 중심망막동맥과 독립적으로 맥락막 순환에서 분지하므로, CRAO 시에도 중심 시력이 보존되는 경우가 있습니다10).
망막은 약 97분간의 허혈을 견딜 수 있지만, 4시간을 초과하면 비가역적 손상이 발생합니다7). 허혈-재관류 손상(IRI)은 CRAO 후 약 7일에 발생하는 것으로 알려져 있습니다7).
대사성 축적질환에서의 체리적점
섹션 제목: “대사성 축적질환에서의 체리적점”리소좀 효소 결핍으로 인해 분해되지 않은 지질(강글리오사이드, 시알산화 당단백 등)이 신경절세포 내에 축적됩니다. 이 축적이 세포체를 팽창시켜 황반부의 신경절세포층이 혼탁해집니다. 중심와에는 신경절세포가 없기 때문에 CRAO와 동일한 기전으로 체리적점이 나타납니다.
시알리도시스에서는 NEU1 유전자의 돌연변이로 인해 뉴라미니다제가 결핍되어 시알산화 당단백이 축적됩니다3)5). 체리적점은 축적량이 증가함에 따라 늦게 나타나는 경우가 있으며, 반대로 신경절세포 사멸이 진행되면 체리적점이 불명확해집니다5). NEU1의 경증 돌연변이가 양쪽 대립유전자에 존재하는 경우 체리적점이 없을 수 있습니다5).
약물 유발성(실데나필 등) CRAO
섹션 제목: “약물 유발성(실데나필 등) CRAO”PDE5 억제제는 cGMP를 상승시켜 전신 혈압 저하로 인한 뇌혈류(CBF) 감소를 초래할 수 있습니다6). 또한 장기적인 cGMP 상승은 내피 투과성을 변화시키고 혈소판 부착 및 혈전 형성을 촉진하는 것으로 알려져 있습니다6).
백인에서는 선명한 붉은색으로 인식되지만, 비백인(아시아인, 아프리카계 등)에서는 갈색에서 검은색조로 보일 수 있습니다. 이는 맥락막 색소량의 차이에 의한 것이며, 소견 해석에 주의가 필요합니다.
7. 최신 연구와 향후 전망(연구 단계 보고)
섹션 제목: “7. 최신 연구와 향후 전망(연구 단계 보고)”CRAO의 외과적 치료 발전
섹션 제목: “CRAO의 외과적 치료 발전”유리체절제술과 안압 및 동맥압 조작을 결합한 외과적 CRAO 치료가 보고되었습니다.
Okonkwo 등(2021)은 비동맥염성 CRAO 2예에 유리체절제술(안압 3 mmHg 미만으로 감소 + 아드레날린 0.1 mg 정맥주사로 동맥압 상승)을 시행하여 각각 시력 6/60, 6/36+1로의 개선을 보고했습니다 7). 발병 후 시간이 짧을수록 시기능 회복 가능성이 높은 것으로 생각됩니다.
CRAO의 뇌졸중 동등 관리
섹션 제목: “CRAO의 뇌졸중 동등 관리”AHA/ASA는 2021년 가이드라인에서 CRAO를 뇌졸중과 동등하게 취급하고 72시간 이내 신경학적 정밀검사를 권장합니다.
Zhong Yang 등(2024)은 CRAO와 동시 뇌경색이 합병된 1예를 보고하고, CRAO 환자의 입원 후 뇌졸중 위험 12.9%, 심근경색 위험 3.7%, 총 심혈관 사건 위험 19%를 제시했습니다 4). 뇌졸중 전문팀과 안과의 협력이 요구됩니다.
COVID-19 백신 후 CRAO
섹션 제목: “COVID-19 백신 후 CRAO”Thakar 등(2022)은 Covaxin(불활성화 COVID-19 백신) 접종 후 CRAO가 발생한 세계 최초의 증례를 보고했습니다 8). 백신 관련 혈관 합병증으로 주목받고 있으며, 인과관계 규명이 향후 과제입니다.
시알리도시스의 유전자형-표현형 상관관계
섹션 제목: “시알리도시스의 유전자형-표현형 상관관계”Sahoo 등(2023)은 시알리도시스에서 새로운 NEU1 돌연변이(c.544T>A, p.Y182N)를 동정하고, CRS와 근간대경련을 주증상으로 하는 임상상을 보고했습니다 3). Neeraja 등(2021)은 NEU1 경증 돌연변이를 가진 시알리도시스 1형 예에서 CRS가 결여된 증례를 보고하고, OCT와 자가형광이 진단에 유용함을 보여주었습니다 5). 유전자형과 표현형의 상관관계 분석이 진행 중입니다.
8. 참고문헌
섹션 제목: “8. 참고문헌”- Semidey VA, Nortley E, Semidey AL, et al. Central retinal artery occlusion in a young patient with sickle cell trait. Cureus. 2023;15(2):e34865.
- Chawla H, Garg U, Gupta A, et al. Central retinal artery occlusion with intracranial hemorrhage secondary to Streptococcus gordonii endocarditis. Case Rep Ophthalmol Med. 2023;2023:9268480.
- Sahoo LK, Mohapatra S, Jena RK, et al. Novel NEU1 variant in sialidosis presenting with cherry-red spot. Neurology. 2023;101(19):861-862.
- Zhong Yang L, Yaqoob T, Tan X, et al. Central retinal artery occlusion with concurrent ischemic stroke: a case report. Cureus. 2024;16(2):e53577.
- Neeraja K, Rukmini AV, Pal PK, et al. Sialidosis type I without cherry red spot: a diagnostic challenge. J Mov Disord. 2021;14(1):65-69.
- Abrishami M, Poorzand H, Shoeibi N, et al. Central retinal artery occlusion associated with sildenafil overdose. Case Rep Ophthalmol Med. 2021;2021:2006271.
- Okonkwo ON, Hassan AO, Alaribe I, et al. Vitrectomy for nonarteritic central retinal artery occlusion. Taiwan J Ophthalmol. 2021;11(3):305-311.
- Thakar M, Bharti N, Chandravanshi LP. Central retinal artery occlusion after Covaxin vaccination: a case report. Indian J Ophthalmol. 2022;70(10):3716-3718.
- Mohamed M, Alsawidi K, Elhousseini Z, et al. Bilateral central retinal artery occlusion in infective endocarditis. J VitreoRetinal Dis. 2021;5(3):261-265.
- American Academy of Ophthalmology. Retinal and ophthalmic artery occlusions preferred practice pattern. AAO; 2024.
