مرحلة الجيوب الأنفية (المرحلة المبكرة)
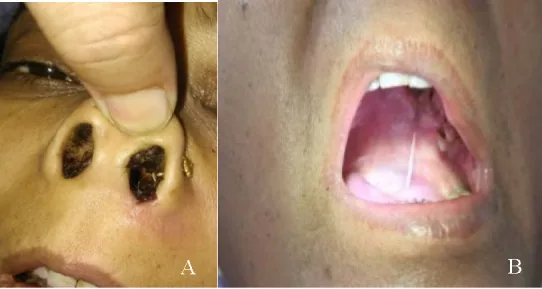
الندبة السوداء (black eschar): علامة مميزة تظهر على الغشاء المخاطي للجيوب الأنفية والمحارات والحنك.
إصابة الجيب الفكي والغربالي: أكثر المناطق إصابة.
يتميز النخر بغياب الاحمرار، على عكس العدوى النمطية.

داء الغشاء المخاطي المداري (Orbital Mucormycosis) هو عدوى فطرية غازية تسببها فطريات من رتبة Mucorales تغزو أنسجة الحجاج من تجويف الأنف والجيوب الأنفية. النوع الأنفي الحجاجي الدماغي (rhino-orbital-cerebral mucormycosis; ROCM) هو الأهم، حيث يشكل جنس Rhizopus (خاصة Rhizopus oryzae) حوالي 85-90% من الحالات الأنفية الدماغية. كان يُسمى سابقًا داء الزيجوميكوز المداري (orbital zygomycosis).
فطريات Mucorales شديدة الارتشاح في الأنسجة، وحتى الآفات الصغيرة التي تصيب قمة الحجاج يمكن أن تسبب اضطرابات حركة العين لا رجعة فيها وفقدان البصر. يقدر معدل الإصابة السنوي بـ 1.7 لكل مليون شخص 8)، وفي الهند يُبلغ عن معدل إصابة أعلى بـ 80 مرة من الدول المتقدمة 9). في أوروبا، يُبلغ عن 0.2-3 لكل مليون شخص 4). يتجاوز معدل الوفيات الإجمالي 50%، ويصل إلى 79% دون علاج وحوالي 40.5% مع العلاج. تصل نسبة إصابة الجهاز العصبي المركزي لدى مرضى السكري ذوي التحكم الضعيف في سكر الدم إلى 33-49% 8).
يبلغ معدل الإصابة السنوي المقدر 1.7 لكل مليون شخص 8). في الهند، تم الإبلاغ عن معدل إصابة أعلى بـ 80 مرة من الدول المتقدمة، مع اختلافات إقليمية كبيرة. يزداد خطر الإصابة بشكل ملحوظ لدى المرضى الذين يعانون من داء السكري أو الأورام الخبيثة الدموية أو نقص المناعة. منذ جائحة كوفيد-19، زادت الحالات بشكل حاد، خاصة في الهند 6).
يصنف داء الموكور الحجاجي حسب مدى الانتشار إلى ثلاثة أنواع التالية.
يتم تقييم شدة انتشار الالتهاب إلى الحجاج باستخدام تصنيف تشاندلر.
| تصنيف تشاندلر | الحالة المرضية |
|---|---|
| المجموعة 1 | التهاب أمام الحاجز (حول الحجاج) |
| المجموعة 2 | التهاب ارتشاحي داخل الحجاج |
| المجموعة 3 | خراج تحت السمحاق |
| المجموعة 4 | خراج داخل الحجاج |
| المجموعة 5 | تخثر الجيب الكهفي |
في المجموعة 3 وما فوق، يجب النظر بنشاط في التدخل الجراحي، وتمثل المجموعة 5 أشد حالات الامتداد داخل الجمجمة.
قد يتدهور بسرعة خلال يوم إلى يومين.
تظهر علامات عينية وجهازية مميزة مع تقدم المرض.
مرحلة الجيوب الأنفية (المرحلة المبكرة)
الندبة السوداء (black eschar): علامة مميزة تظهر على الغشاء المخاطي للجيوب الأنفية والمحارات والحنك.
إصابة الجيب الفكي والغربالي: أكثر المناطق إصابة.
يتميز النخر بغياب الاحمرار، على عكس العدوى النمطية.
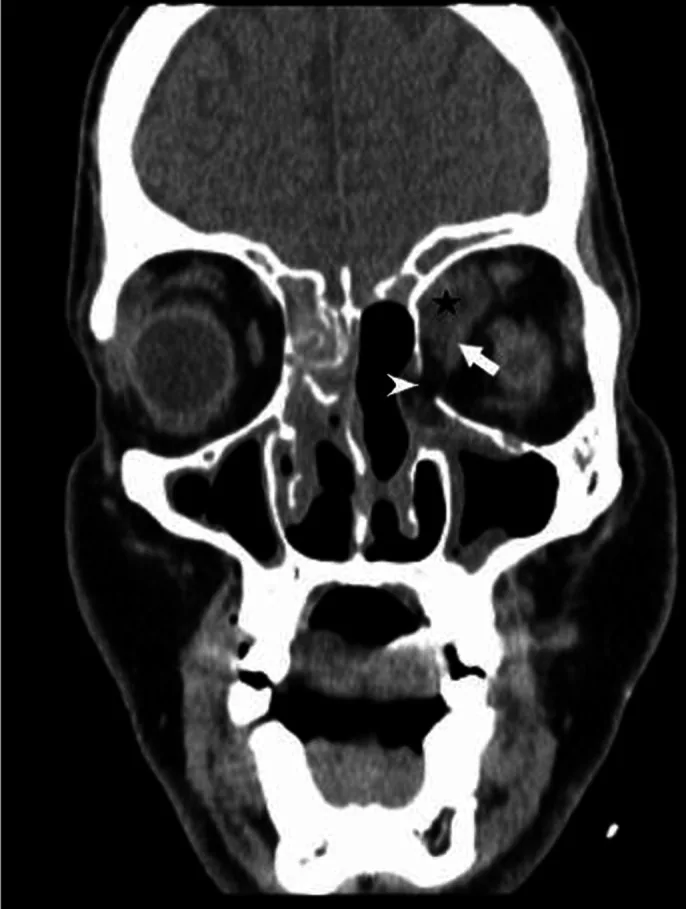
مرحلة الامتداد المداري
جحوظ العين: يُبلغ عنه في 64-83% من الحالات.
شلل العضلات خارج المقلة إلى تصلب المقلة (frozen globe): أكثر العلامات العينية شيوعًا.
تدلي الجفن، وذمة الجفن، غرغرينا الجفن: تعكس تقدم الالتهاب والنخر.
مرحلة الامتداد الدماغي
متلازمة قمة الحجاج (OAS): مع تصلب المقلة، تشير إلى إصابة واسعة للأعصاب القحفية. معدل وفيات مرتفع.
خثار الجيب الكهفي: بسبب ضعف التصريف الوريدي.
انسداد الشريان الشبكي المركزي (CRAO): بقعة حمراء كرزية في قاع العين.
في حالات ROCM المرتبطة بـCOVID-19، لوحظ وجود CRAO وجحوظ العين وشلل العضلات العينية الكامل في جميع الحالات، وكان التشخيص سيئًا للغاية (جميع الحالات توفيت) 3).
الفطريات من رتبة Mucorales، خاصة Rhizopus oryzae، هي المسبب الرئيسي. وهي فطريات خيطية سريعة النمو غير مقسمة (aseptate)، تنتشر بكثرة في المناطق الاستوائية وشبه الاستوائية. تدخل الجسم عن طريق استنشاق الجراثيم.
لقد زادت حالات داء الفطريات المخاطية المداري الأنفي بعد كوفيد-19 بشكل كبير عالميًا، وخاصة في الهند حيث تم الإبلاغ عن 2,826 حالة في عام 2021 6). يُعتقد أن عاصفة السيتوكينات الناتجة عن كوفيد-19، واضطراب المناعة، واستخدام الستيرويدات، وارتفاع سكر الدم تعزز بشكل تآزري نمو الفطريات.
الخزعة والزراعة هما المعيار الذهبي للتشخيص النهائي. في علم الأمراض النسيجي، تُستخدم صبغات H&E وPAS وGMS، وتتمثل النتائج المميزة في خيوط فطرية عريضة شبيهة بالأشرطة غير محجوبة تتفرع بزاوية قائمة (90 درجة)، بالإضافة إلى الغزو الوعائي والتخثر والنخر 2). تحديد نوع الفطر عن طريق الزراعة مهم أيضًا لاختيار العلاج، لكن معدل إيجابية الزراعة منخفض. يعتمد التشخيص النهائي على إثبات وجود الفطر عن طريق الفحص النسيجي أو الزراعة.
يمكن اكتشاف تسلسلات الحمض النووي لجنس Rhizopus في السائل النخاعي. تم الإبلاغ عن إيجابية في جميع الحالات السبع (بينما كانت الزراعة سلبية في جميع الحالات)، وهو مفيد بشكل خاص عندما تكون الطرق التقليدية سلبية.
فيما يلي خصائص طرق التشخيص:
| طريقة الفحص | الخصائص | ملاحظات |
|---|---|---|
| الخزعة + الزراعة | المعيار الذهبي للتشخيص النهائي | معدل إيجابية الزراعة منخفض |
| mNGS (السائل النخاعي) | يمكن الكشف حتى في حالات الزراعة السلبية | يتطلب مرافق متخصصة |
| β-D-جلوكان و GM | علامات فطرية روتينية | حساسية منخفضة تجاه Mucorales، غير مناسب للتشخيص |
العلاج الأساسي هو الجمع بين مضادات الفطريات والتنضير الجراحي، ويُفضل العلاج في قسم الباطنة للإدارة الشاملة. نظرًا لضعف اختراق مضادات الفطريات للأنسجة الميتة، فإن الجمع مع العلاج الجراحي ضروري.
| الدواء | الموقع | الجرعة وطريقة الاستخدام |
|---|---|---|
| أمفوتيريسين ب الشحمي (L-AMB) | الخط الأول | عادة 5-7.5 ملغم/كغم/يوم؛ في حالات إصابة الجهاز العصبي المركزي 10 ملغم/كغم/يوم |
| بوساكونازول | العلاج التنحي أو الإنقاذي | معدل الاستجابة 60-70%2) |
| إيزافوكونازول | علاج بديل (تحمّل جيد) 7) | جرعة تحميل 200 ملغ ثم 200 ملغ/يوم (عن طريق الفم) |
| فوريكونازول | غير فعال ضد داء الفطريات المخاطية | غير قابل للاستخدام (نقطة اختلاف حاسمة مع داء الرشاشيات) |
الخيار الأول: أمفوتيريسين ب الشحمي (L-AMB) 2)
بوساكونازول: علاج تنحي أو إنقاذي. نسبة الاستجابة 60-70% 2).
إيزافوكونازول: فعال كعلاج بديل، تحمّل جيد 7). جرعة تحميل 200 ملغ ثم 200 ملغ/يوم (عن طريق الفم).
العلاج المركب: أفادت بعض التقارير أن الجمع بين أمفوتيريسين وكاسبوفونجين يؤدي إلى نتائج أفضل من العلاج الأحادي، لكن النشاط المختبري للإكينوكاندينات ضد الفطريات المخاطية منخفض، ولا توجد أدلة قوية 2).
التنظير الجراحي للأنسجة الميتة ضروري. يجب الاستئصال حتى الحصول على نزيف طبيعي، ويوصى بشدة بتأكيد هوامش الاستئصال مرضياً. الجراحة بالمنظار الوظيفي للجيوب الأنفية (FESS) هي الطريقة الجراحية القياسية، وقد تكون هناك حاجة لعمليات متعددة 4). غالباً ما تكون معالجة الجيوب الأنفية من قبل أخصائي الأنف والأذن والحنجرة ضرورية لدى البالغين، ومن المهم تقليل الضغط داخل الحجاج خاصة عند حدوث انخفاض في الرؤية. في الحالات الواسعة التي تشمل الحجاج، قد يلزم استئصال محتويات الحجاج مع إزالة العظام.
معدل الوفيات عند الجمع بين مضادات الفطريات والجراحة هو 18.5%، بينما يصل إلى 60% عند استخدام مضادات الفطريات وحدها، وهو أعلى بكثير 2).
مدة إعطاء الأمفوتريسين ب الشحمي تتراوح بين 3 و36 شهراً، ويتم تعديلها بشكل فردي حسب التحسن السريري والتصويري 2). في الحالات الشديدة أو التي تمتد إلى الدماغ، غالباً ما تكون هناك حاجة لفترة أطول. قد تكون هناك حاجة أيضاً لعمليات تنظير جراحي متعددة.
فوريكونازول هو دواء مضاد للفطريات فعال ضد داء الرشاشيات، لكنه غير فعال ضد داء الموكور (Mucorales). نظرًا لأن كلاهما قد يظهران أعراضًا وعلامات متشابهة، فإن تحديد العامل المسبب مهم جدًا لاختيار العلاج. تم الإبلاغ عن حالات عدوى اختراقية للموكور أثناء تناول فوريكونازول 4)، مما يستلزم تحديدًا دقيقًا للفطر.
يؤدي استنشاق الجراثيم إلى تكاثرها داخل الجيوب الأنفية، ثم تصل إلى الحجاج إما عن طريق الارتشاح المباشر أو عبر القناة الأنفية الدمعية. من الحجاج إلى الدماغ، تدخل عبر قمة الحجاج والجيب الكهفي والصفيحة المصفوية والأوعية الدموية.
آلية الانتشار الرئيسية هي غزو الأوعية الدموية (angioinvasion)، حيث تخترق الخلايا البطانية لجدار الوعاء وبروتينات المصفوفة خارج الخلية. يشارك بروتين GRP78 (بروتين تنظيم الجلوكوز) في عملية الاختراق هذه. يتطور المسار: غزو الأوعية → تخثر → نقص تروية → نخر إقفاري، مما يؤدي إلى نخر بدون احتقان.
تحت الظروف الحمضية، يتم تحرير الحديد من الترانسفيرين، وتستخدم فطريات الموكوراليس الحديد الحر للتكاثر بسرعة. تعمل آلية مماثلة أيضًا في حالات فرط الحديد (داء ترسب الأصبغة الدموية، نقل الدم المتكرر، العلاج بديسفيريوكسامين).
عاصفة السيتوكينات (ارتفاع IL-1 وIL-2 وIL-6 وTNF-α)، وانخفاض تعبير IFN-γ في الخلايا التائية CD4+، واستخدام الستيرويدات والأدوية المعدلة للمناعة، وتداخل نقص الأكسجة + ارتفاع السكر + البيئة الحمضية + ارتفاع الحديد يوفر بيئة مثالية لإنبات الجراثيم الفطرية 7).
أبلغ يانغ وآخرون (2026) عن 7 حالات من داء الغشاء المخاطي المداري الجيبي (ROCM) ظهرت أعراضها الأولية كاحتشاء دماغي 5). تم اكتشاف جنس الرايزوبس في السائل النخاعي بواسطة mNGS في جميع الحالات، لكن الزرع كان سلبيًا في جميع الحالات. كان متوسط الوقت حتى التشخيص 5 أيام، والمريض الوحيد الناجي تم تشخيصه في يومين (معدل الوفيات 85.7%). يُعتبر mNGS أداة واعدة للتشخيص المبكر لـ ROCM، وله قيمة خاصة عندما تكون الزراعة والعلامات المصلية التقليدية سلبية.
يكون mNGS (تسلسل الجيل التالي للميتاجينوم) مفيدًا عندما يكون β-D-glucan و galactomannan ضعيفي الحساسية، وعندما يفشل الزرع في تحديد العامل المسبب. خاصة في حالات ROCM غير النمطية التي تظهر أعراضها الأولية كاحتشاء دماغي، يمكن أن يكون mNGS للسائل النخاعي وسيلة التشخيص الوحيدة 5).
نظرًا للزيادة العالمية في ROCM المصاحب لكوفيد-19، أبلغ أوستوفان وآخرون (2021) عن وفاة جميع المرضى الذين لديهم تاريخ من التهوية الميكانيكية 6). في الهند، أبلغ سين وآخرون (2021) عن 2,826 حالة من ROCM المرتبط بكوفيد-19، مما يلفت الانتباه كمضاعفات خطيرة جديدة في الجائحة.
أبلغ آل ريسي وآخرون (2023) عن حالة طفل يعاني من مرض الكلى المزمن الحاد وسوء التغذية، تم شفاؤه بالعلاج المكثف باستخدام الأمفوتريسين B الليبوزومي (5→9 ملغم/كغم/يوم) + بوساكونازول + عمليات جراحية متعددة 2). يُعتبر التشخيص المبكر خلال 24 ساعة والعلاج المكثف مفتاح النتائج الجيدة.