โรคเมือกอร์มิโคซิสชนิดไรโน-ออร์บิทัล-ซีรีบรัล (ROCM) คือการติดเชื้อราในอันดับ Mucorales ที่รุนแรงและเป็นอันตรายถึงชีวิต โดยเชื้อจะแพร่กระจายอย่างรวดเร็วจากโพรงจมูกไปยังเบ้าตา และสมอง อัตราการเสียชีวิตหากไม่ได้รับการรักษาสูงถึง 79%
โรคเบาหวาน (โดยเฉพาะภาวะกรดคีโตนจากเบาหวาน) เป็นปัจจัยเสี่ยงที่สำคัญที่สุด โดยพบในผู้ป่วย 58.9–86.7% ของกรณี
เนื้อเยื่อบุโพรงจมูกที่ตายเป็นสีดำ (black eschar) เป็นลักษณะสำคัญในระยะแรกที่ไม่ควรมองข้าม
การวินิจฉัยที่แน่นอนโดยหลักแล้วต้องอาศัยการตรวจชิ้นเนื้อและการเพาะเชื้อ แต่ mNGS (การหาลำดับรุ่นต่อไปแบบเมตาจีโนม) มีประโยชน์ในกรณีที่ผลการตรวจด้วยวิธีดั้งเดิมเป็นลบ
การรักษาหลักคือการใช้ยาต้านเชื้อรา liposomal amphotericin B ร่วมกับการผ่าตัดเนื้อเยื่อที่ตายแล้วออก
ความล่าช้าในการวินิจฉัยเป็นอันตรายถึงชีวิต โดยความล่าช้ามากกว่า 6 วันจะทำให้อัตราการเสียชีวิตเพิ่มขึ้นประมาณ 2 เท่า
โรคมิวคอร์ไมโคซิสชนิดไรโน-ออร์บิทัล-ซีรีบรัล (rhino-orbital-cerebral mucormycosis ; ROCM) คือการติดเชื้อราที่รุกรานจากเชื้อราในอันดับ Mucorales โดยเฉพาะ Rhizopus oryzae โรคนี้เริ่มต้นจากไซนัสพารานาซัลแล้วลุกลามอย่างรวดเร็วไปยังเบ้าตา และสมอง เป็นโรคที่ร้ายแรงถึงชีวิต เดิมเคยเรียกว่า orbital zygomycosis Gregory เป็นผู้บรรยายโรคนี้ครั้งแรกในปี ค.ศ. 19431)
สกุล Rhizopus คิดเป็นประมาณ 85-90% ของผู้ป่วยโรคสมองจากเชื้อราในโพรงจมูก อัตราการเกิดโรคโดยประมาณคือ 1.7 ต่อล้านคนต่อปี8) ในอินเดียมีรายงานอัตราการเกิดโรคสูงกว่าประเทศที่พัฒนาแล้วถึง 80 เท่า9) ในยุโรปมีรายงาน 0.2-3 ต่อล้านคน4) อัตราการเสียชีวิตโดยรวมมากกว่า 50% โดยไม่ได้รับการรักษาคือ 79% และเมื่อได้รับการรักษาประมาณ 40.5% การมีส่วนร่วมของระบบประสาทส่วนกลางในผู้ป่วยเบาหวานที่ควบคุมระดับน้ำตาลได้ไม่ดีสูงถึง 33-49%8)
แม้จะพบได้น้อย แต่อัตราการเสียชีวิตสูง โดยเฉพาะในชนิดรุกรานของเชื้อราที่โพรงไซนัส มีรายงานอัตราการเสียชีวิตสูงถึง 94% หลังการระบาดของ COVID-19 จำนวนผู้ป่วยเพิ่มขึ้นอย่างรวดเร็ว โดยเฉพาะในอินเดีย 6)
Q
โรคมิวคอร์ไมโคซิสชนิดโพรงจมูก-เบ้าตา-สมองเกิดขึ้นบ่อยแค่ไหน?
A
อัตราการเกิดโรคโดยประมาณต่อปีคือ 1.7 ต่อประชากร 1 ล้านคน8) ในอินเดีย มีรายงานอัตราการเกิดโรคสูงกว่าประเทศที่พัฒนาแล้วถึง 80 เท่า ซึ่งแสดงให้เห็นถึงความแตกต่างในแต่ละภูมิภาคอย่างมาก ในกลุ่มผู้ป่วยที่เป็นโรคเบาหวาน มะเร็งเม็ดเลือดขาว หรือมีภาวะภูมิคุ้มกันบกพร่อง ความเสี่ยงในการเกิดโรคจะเพิ่มขึ้นอย่างมีนัยสำคัญ
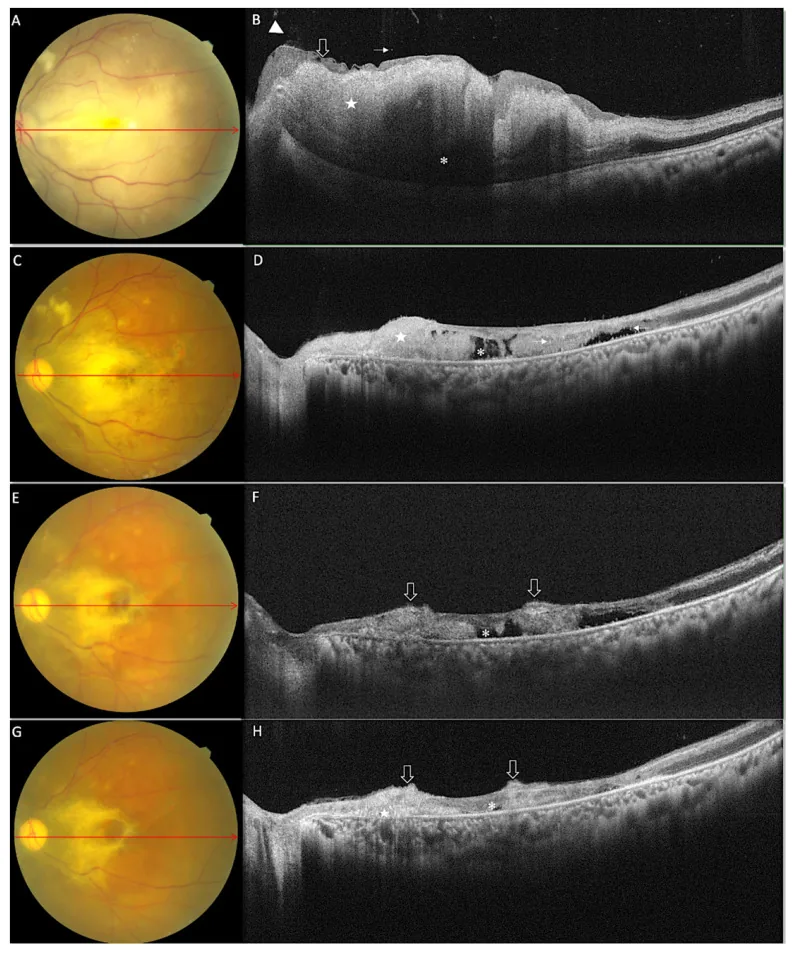
ภาพจอประสาทตาและ OCT ของโรค mucormycosis ชนิด rhino-orbital-cerebral Spectral Domain Optical Coherence Tomography Findings in Vision-Threatening Rhino-Orbital Cerebral Mucor Mycosis—A Prospective Analysis. Diagnostics (Basel). 2022 Dec 8; 12(12):3098. Figure 1. PM
CI D: PMC9777225. License: CC BY.
ภาพถ่ายจอประสาทตา ต่อเนื่องและภาพ SD-OCT ของกรณีตัวอย่าง (กรณีที่ 5) ที่จุดเริ่มต้น (A) ภาพถ่ายจอประสาทตา แสดงให้เห็นการขาวของจอประสาทตา แบบกระจายพร้อมรอยพับของจานประสาทตา -จุดรับภาพ, การแบ่งส่วนของหลอดเลือดแบบ boxcar, ไม่มี cherry red spot (B) ภาพตัด SD-OCT ที่สอดคล้องกันแสดงให้เห็นการหนาตัวของจอประสาทตา แบบกระจาย, การสะท้อนแสงที่เพิ่มขึ้นของจอประสาทตา ชั้นใน (ดาวสีขาว) พร้อมเอฟเฟกต์เงาบนจอประสาทตา ชั้นนอก (ดอกจันสีขาว) นอกจากนี้ยังพบรอยพับของจอประสาทตา , การหลุดของเยื่อหุ้มชั้นใน (ILM ) (ลูกศรว่าง), หมอกในน้ำวุ้นตา และเซลล์ในน้ำวุ้นตา (หัวลูกศร) ที่สามสัปดาห์ (C) ภาพถ่ายจอประสาทตา แสดงให้เห็นการลดลงของบริเวณที่จอประสาทตา ขาวแบบกระจาย, มีจุดสำลีและเลือดออกเล็กน้อย (D) บน SD-OCT พบการหยุดชะงักของทุกชั้นจอประสาทตา (ดาวสีขาว) ร่วมกับช่องว่างที่ไม่มีแสง
อาการของไซนัสอักเสบ: คัดจมูก น้ำมูกไหล เลือดกำเดาไหล
ปวดศีรษะ (ปวดใบหน้า ปวดบริเวณหน้าผาก)
การมองเห็น ลดลงจนถึงสูญเสียการมองเห็น ภาพซ้อน โรคจมูกอักเสบ หนังตาตก ข้างเดียว หนังตาบวม (อาการเริ่มแรก)
อ่อนเพลีย มีไข้
อาจแย่ลงอย่างรวดเร็วภายใน 1-2 วัน
เมื่อโรคดำเนินไป จะพบลักษณะเฉพาะทางจักษุวิทยาและทางระบบร่างกายตามระยะของโรค
ระยะไซนัส (ระยะเริ่มต้น)
เนื้อตายสีดำและสะเก็ดดำ (black eschar) : เป็นลักษณะเฉพาะที่พบในเยื่อบุโพรงจมูก, กังหันจมูก, และเยื่อบุเพดานปาก
การมีส่วนร่วมของโพรงอากาศขากรรไกรบนและโพรงอากาศเอทมอยด์ : เป็นตำแหน่งที่เกี่ยวข้องบ่อยที่สุด
ลักษณะเด่นคือเนื้อตายที่ไม่มีอาการตาแดง ซึ่งแตกต่างจากการติดเชื้อทั่วไป
ระยะลุกลามเข้าสู่วงโคจรตา
ตาโปน (Proptosis) : พบได้ 64–83% ของผู้ป่วย
กล้ามเนื้อตาภายนอกเป็นอัมพาตจนถึงลูกตาถูกตรึง (frozen globe) : สัญญาณทางตาที่พบได้บ่อยที่สุด
หนังตาตก หนังตาบวม หนังตาเน่า
ระยะลุกลามของสมอง
กลุ่มอาการปลายเบ้าตา (Orbital Apex Syndrome - OAS)
ภาวะลิ่มเลือดอุดตันในโพรงเลือดดำโพรงกระดูกสันหลังส่วนคอ (Cavernous Sinus Thrombosis) : เกิดจากการไหลเวียนเลือดดำผิดปกติ
ภาวะหลอดเลือดแดงจอตาส่วนกลางอุดตัน (CRAO ) : พบจุดแดงเชอร์รี (cherry-red spot) ที่จอตา
ในผู้ป่วย COVID-19 ที่เกี่ยวข้องกับ ROCM ทุกรายพบ CRAO ร่วมกับตาโปนและกล้ามเนื้อตาอัมพาตสมบูรณ์ และการพยากรณ์โรคแย่มาก (ผู้ป่วยทุกรายเสียชีวิต) 3)
เชื้อราในอันดับ Mucorales โดยเฉพาะ Rhizopus oryzae เป็นสาเหตุหลัก เป็นราเส้นใยที่ไม่มีผนังกั้น (aseptate) เจริญเติบโตเร็ว พบมากในเขตร้อนและกึ่งร้อน การติดเชื้อเกิดจากการสูดดมสปอร์
โรคเบาหวาน (โดยเฉพาะภาวะกรดคีโตนจากเบาหวาน) : ปัจจัยเสี่ยงที่สำคัญที่สุด (58.9–86.7%)มะเร็งเม็ดเลือดขาวชนิดร้าย (เช่น acute myeloid leukemia) · ภาวะนิวโทรพีเนีย
ประวัติการปลูกถ่ายไตและการใช้ยากดภูมิคุ้มกัน
การติดเชื้อเอชไอวี โรคไตเรื้อรัง ภาวะทุพโภชนาการ
ภาวะฮีโมโครมาโทซิสและการรักษาด้วยเดเฟอริอกซามีน
การติดเชื้อ COVID-19 : ความเสี่ยงเพิ่มขึ้นโดยเฉพาะในผู้ที่ใช้สเตียรอยด์ หรือมีโรคเบาหวานร่วม6) 7) การพักรักษาตัวใน ICU เป็นเวลานาน การใช้ยาทางหลอดเลือดดำ
การให้ยาโวริโคนาโซลเพื่อป้องกัน (อาจกระตุ้นให้เชื้อรา Mucorales เจริญมากเกินไป) 4)
Q
การติดเชื้อ COVID-19 ทำให้เสี่ยงต่อโรคมูคอร์ไมโคซิสมากขึ้นหรือไม่?
A
จำนวนผู้ป่วยโรค ROCM หลังติดเชื้อ COVID-19 เพิ่มขึ้นอย่างรวดเร็วทั่วโลก โดยเฉพาะในอินเดียมีรายงาน 2,826 รายในปี 2021 6) เชื่อว่าพายุไซโตไคน์ ความผิดปกติของภูมิคุ้มกัน การใช้สเตียรอยด์ และภาวะน้ำตาลในเลือดสูงจาก COVID-19 ส่งเสริมการเจริญเติบโตของเชื้อราอย่างสัมพันธ์กัน
CT :มีประโยชน์ในการประเมินการกัดกร่อนของกระดูกผนังไซนัสและความขุ่นภายในโพรงไซนัส ตำแหน่งที่พบบ่อยที่สุดคือไซนัสบนขากรรไกรและไซนัสเอทมอยด์ ควรทำ CT ด้วยการฉีดสารทึบรังสี ในระยะแรกอาจไม่พบความผิดปกติในหลายกรณี ดังนั้นการตรวจภาพซ้ำจึงมีความสำคัญMRI :
T1-weighted image: รอยโรคที่มีสัญญาณเท่ากัน
ภาพ T2-weighted: สัญญาณต่ำ (สะท้อนเนื้อตาย)
สัญญาณ Turbinate ดำ : การตรวจพบว่าเยื่อบุโพรงจมูกไม่มีการเพิ่มความเข้มของสัญญาณในการตรวจ MRI ด้วยสารทึบแสง T1 ซึ่งบ่งชี้ถึงเนื้อตายและเป็นลักษณะเฉพาะ5) การมีส่วนร่วมของโพรงเลือดดำในสมอง (Cavernous sinus): การไม่มีการเพิ่มความเข้มของสารทึบรังสี
การตรวจหาจุด infarct ในสมองที่มักเกิดในสมองส่วนหน้าและ basal ganglia 5)
การตรวจชิ้นเนื้อและการเพาะเชื้อเป็นมาตรฐานทองคำสำหรับการวินิจฉัยที่แน่นอน ในการตรวจทางพยาธิวิทยาเนื้อเยื่อจะใช้การย้อม H&E การย้อม PAS และการย้อม GMS โดยลักษณะที่พบได้คือเส้นใยเชื้อรารูปริบบิ้นกว้างไม่มีผนังกั้นที่แตกแขนงเป็นมุมฉาก (90 องศา) การบุกรุกหลอดเลือด การเกิดลิ่มเลือด และเนื้อตาย 2) การระบุชนิดของเชื้อราด้วยการเพาะเชื้อมีความสำคัญต่อการเลือกใช้ยา แต่ผลเพาะเชื้อเป็นบวกมีอัตราต่ำ การวินิจฉัยที่แน่นอนทำได้โดยการตรวจทางพยาธิวิทยาหรือการเพาะเชื้อที่พิสูจน์ว่ามีเชื้อรา
สามารถตรวจพบลำดับดีเอ็นเอของเชื้อรา Rhizopus ในน้ำไขสันหลังได้ มีรายงานผลบวกในทุกรายจากทั้งหมด 7 ราย (การเพาะเชื้อให้ผลลบทั้งหมด) ซึ่งมีประโยชน์อย่างยิ่งเมื่อวิธีการตรวจแบบดั้งเดิมให้ผลลบ
ลักษณะเฉพาะของวิธีการวินิจฉัยแสดงดังต่อไปนี้
วิธีการตรวจ ลักษณะเด่น ข้อควรระวัง การตรวจชิ้นเนื้อ + การเพาะเชื้อ มาตรฐานทองคำสำหรับการวินิจฉัยที่แน่นอน อัตราการเพาะเชื้อให้ผลบวกต่ำ mNGS (น้ำไขสันหลัง) ตรวจพบได้แม้ในกรณีที่เพาะเชื้อให้ผลลบ ต้องใช้สถานพยาบาลเฉพาะทาง β-D-กลูแคน · จีเอ็ม เครื่องหมายเชื้อราทั่วไป มีความไวต่อ Mucorales ต่ำ ไม่เหมาะสำหรับการวินิจฉัย
โรคแอสเปอร์จิลโลซิส (สำคัญที่สุด): จุดสังเกตคือเส้นใยที่มีผนังกั้นและแตกแขนงเป็นมุม 45 องศาเซลลูไลติสในเบ้าตา
แกรนูโลมาโตซิสกับโพลีแองจิอักเสบ (GP A)
การรักษาหลักคือการใช้ยาต้านเชื้อราร่วมกับการผ่าตัดตัดเนื้อเยื่อที่ตายแล้ว และควรทำการรักษาในแผนกอายุรกรรมที่สามารถดูแลผู้ป่วยแบบองค์รวมได้ เนื่องจากการซึมผ่านของยาต้านเชื้อราเข้าไปในเนื้อเยื่อที่ตายแล้วนั้นไม่ดี จึงจำเป็นต้องใช้ร่วมกับการผ่าตัดรักษา
ทางเลือกแรก: ลิโปโซมอลแอมโฟเทอริซินบี (L-AMB) 2)
ขนาดปกติ: 5–7.5 มก./กก./วัน
กรณีที่มีการบุกรุกของ CNS: 10 มก./กก./วัน1)
ระยะเวลาการให้ยา: 3–36 เดือน (ขึ้นอยู่กับการปรับปรุงทางคลินิกและภาพถ่ายรังสี)
แอมโฟเทอริซินบีดีออกซีโคเลตมีความเป็นพิษต่อไตสูงมาก ควรเลือกใช้สูตรไลโปโซมเป็นอันดับแรก
โพซาโคนาโซล : การบำบัดแบบลดขั้นหรือการบำบัดกู้ชีพ อัตราการตอบสนอง 60–70%2)
ไอซาวูโคนาโซล : มีประสิทธิภาพเป็นทางเลือกทดแทน ทนต่อยาได้ดี7) หลังจากให้ยาโหลด 200 มก. แล้วให้ 200 มก./วัน (สามารถรับประทานได้)
การรักษาแบบผสมผสาน : มีรายงานว่าการใช้แอมโฟเทอริซินร่วมกับแคสโปฟังกินให้ผลลัพธ์ที่ดีกว่าการใช้ยาเดี่ยว แต่เอคิโนแคนดินมีฤทธิ์ในหลอดทดลองต่อเชื้อราในกลุ่ม Mucorales ต่ำ และยังไม่มีหลักฐานที่ชัดเจน2)
การตัดเนื้อเยื่อที่ตายแล้วออกด้วยวิธีผ่าตัดเป็นสิ่งจำเป็น ควรตัดจนกว่าจะมีเลือดออกปกติ และแนะนำอย่างยิ่งให้ตรวจทางพยาธิวิทยาที่ขอบตัด การผ่าตัดไซนัสด้วยกล้องแบบส่องกล้องเพื่อการทำงาน (FES S) เป็นวิธีมาตรฐาน และอาจต้องผ่าตัดหลายครั้ง4) ในกรณีที่มีการเกี่ยวข้องกับเบ้าตา อย่างกว้างขวาง อาจต้องผ่าตัดเอาสิ่งในเบ้าตา ออกพร้อมกับการตัดกระดูก
อัตราการเสียชีวิตของการใช้ยาต้านเชื้อราร่วมกับการผ่าตัดอยู่ที่ 18.5% ในขณะที่การใช้ยาต้านเชื้อราเพียงอย่างเดียวสูงถึง 60% ซึ่งสูงกว่าอย่างมีนัยสำคัญ2)
การฉีดแอมโฟเทอริซินบีหลังลูกตาและในน้ำวุ้นตา (การให้ในน้ำวุ้นตา : 10 ไมโครกรัม/0.1 มล.) 1)
การบำบัดด้วยออกซิเจนความดันสูง : มีฤทธิ์ต้านเชื้อราและส่งเสริมการสร้างหลอดเลือดใหม่ในบริเวณที่ขาดเลือด1)
การควบคุมระดับน้ำตาลในเลือดในผู้ป่วยเบาหวานและการแก้ไขภาวะกรดคีโตนจากเบาหวาน7)
การแก้ไขภาวะภูมิคุ้มกันบกพร่อง (ลดขนาดยาภูมิคุ้มกันให้มากที่สุดเท่าที่เป็นไปได้)
การวินิจฉัยที่ล่าช้าเกิน 6 วันจะทำให้อัตราการเสียชีวิตภายใน 30 วันเพิ่มขึ้นประมาณ 2 เท่า จาก 35% เป็น 66% หากสงสัย ควรเริ่มการรักษาทันที6)
เนื่องจากยาต้านเชื้อราแทรกซึมเข้าไปในเนื้อเยื่อที่ตายแล้วได้ไม่ดี การรักษาด้วยยาต้านเชื้อราเพียงอย่างเดียวจึงยากที่จะหายขาด จำเป็นต้องใช้ร่วมกับการผ่าตัดล้างเนื้อเยื่อที่ตายแล้ว (debridement)
แม้จะใช้ยาสูตรไลโปโซม ก็ต้องระวังพิษต่อไต และติดตามการทำงานของไตอย่างสม่ำเสมอ
Q
การรักษาต้องใช้ระยะเวลานานเท่าใด?
A
ระยะเวลาในการให้ยา liposomal amphotericin B มีความกว้างตั้งแต่ 3 ถึง 36 เดือน โดยปรับตามการตอบสนองทางคลินิกและภาพถ่ายรังสีเป็นรายบุคคล2) ในกรณีที่รุนแรงหรือมีการลุกลามไปยังสมอง มักต้องใช้ระยะเวลาในการรักษาที่ยาวนานขึ้น การผ่าตัดล้างแผล (surgical debridement) อาจต้องทำหลายครั้งเช่นกัน
สปอร์ที่สูดเข้าไปจะเจริญเติบโตในโพรงไซนัส และเข้าสู่เบ้าตา โดยการแพร่กระจายโดยตรงหรือผ่านทางท่อน้ำตา จากเบ้าตา ไปยังสมองจะบุกรุกผ่านทางปลายเบ้าตา โพรงเลือดดำคาเวอร์นัส แผ่นคริบริฟอร์ม และหลอดเลือด
กลไกการแพร่กระจายหลักคือการบุกรุกหลอดเลือด (angioinvasion) ซึ่งทะลุผ่านเซลล์บุผนังหลอดเลือดและโปรตีนเมทริกซ์นอกเซลล์ GRP 78 (glucose-regulated protein 78) มีส่วนร่วมในกระบวนการทะลุผ่านนี้ การดำเนินไปตามเส้นทาง การบุกรุกหลอดเลือด → การเกิดลิ่มเลือด → การขาดเลือด → เนื้อตายจากการขาดเลือด ทำให้เกิดเนื้อตายที่ไม่มีเลือดคั่ง
ภายใต้สภาวะที่เป็นกรด เหล็กจะถูกปลดปล่อยจากทรานสเฟอร์ริน และเชื้อรา Mucorales จะใช้เหล็กอิสระนี้เพื่อเจริญเติบโตอย่างรวดเร็ว กลไกเดียวกันนี้ยังเกิดขึ้นในภาวะเหล็กเกิน (เช่น ฮีโมโครมาโทซิส การรับเลือดบ่อยครั้ง การรักษาด้วยเดสเฟอริออกซามีน)
พายุไซโตไคน์ (การเพิ่มขึ้นของ IL-1, IL-2, IL-6, TNF -α เป็นต้น), การแสดงออกของ IFN-γ ใน CD4+ T cells ที่ลดลง, การใช้สเตียรอยด์ และยาปรับภูมิคุ้มกัน, ภาวะขาดออกซิเจนร่วมกับน้ำตาลในเลือดสูง, สภาพแวดล้อมที่เป็นกรด และระดับธาตุเหล็กสูงที่ซ้อนทับกัน ทำให้เกิดสภาพแวดล้อมที่เหมาะสมต่อการงอกของสปอร์เชื้อรา7)
การอุดตันของหลอดเลือดแดงจอประสาทตา ส่วนกลาง : การอุดตันหรือเส้นเลือดอุดตันโดยตรงจากการบุกรุกของเชื้อราในหลอดเลือด3) เส้นประสาทตา ขาดเลือดเบ้าตา ลิ่มเลือดอุดตันในโพรงเลือดดำคาเวอร์นัส (Cavernous sinus thrombosis) : การไหลเวียนเลือดดำกลับผิดปกติ
เนื้อหาต่อไปนี้อยู่ในขั้นตอนการวิจัยหรือการทดลองทางคลินิก และไม่ใช่การรักษามาตรฐานที่สามารถรับได้ในโรงพยาบาลทั่วไป เป็นข้อมูลอ้างอิงสำหรับผู้เชี่ยวชาญเกี่ยวกับการพัฒนาทางการแพทย์ในอนาคต
Yang et al. (2026) รายงานผู้ป่วย ROCM จำนวน 7 รายที่มีอาการเริ่มต้นเป็นโรคหลอดเลือดสมองตีบ5) ผู้ป่วยทุกรายตรวจพบเชื้อ Rhizopus ในน้ำไขสันหลังด้วยวิธี mNGS แต่การเพาะเชื้อให้ผลลบทั้งหมด ค่ามัธยฐานของเวลาจนถึงการวินิจฉัยคือ 5 วัน ผู้รอดชีวิตเพียงรายเดียวได้รับการวินิจฉัยภายใน 2 วัน (อัตราการเสียชีวิต 85.7%) mNGS เป็นเครื่องมือที่มีแนวโน้มดีสำหรับการวินิจฉัย ROCM ตั้งแต่ระยะแรก โดยเฉพาะอย่างยิ่งเมื่อการเพาะเชื้อและเครื่องหมายทางซีรั่มแบบดั้งเดิมให้ผลลบ
Q
การตรวจ mNGS มีประโยชน์ในสถานการณ์ใดบ้าง?
A
mNGS (การหาลำดับเมตาจีโนมยุคถัดไป) มีประโยชน์ในกรณีที่ β-D-glucan และ galactomannan มีความไวต่ำ และไม่สามารถระบุเชื้อก่อโรคได้จากการเพาะเชื้อ โดยเฉพาะใน ROCM ที่ผิดปกติซึ่งมีภาวะสมองขาดเลือดเป็นอาการเริ่มแรก mNGS ในน้ำไขสันหลังอาจเป็นวิธีการวินิจฉัยเพียงวิธีเดียว5)
เนื่องจากการเพิ่มขึ้นอย่างรวดเร็วของ ROCM ที่เกี่ยวข้องกับ COVID-19 ทั่วโลก Ostovan et al. (2021) รายงานว่าผู้ป่วยทุกคนที่มีประวัติการใช้เครื่องช่วยหายใจเสียชีวิตทั้งหมด 6) ในอินเดีย Sen และคณะ (2021) รายงานผู้ป่วย ROCM ที่เกี่ยวข้องกับ COVID-19 จำนวน 2,826 ราย ซึ่งได้รับความสนใจในฐานะภาวะแทรกซ้อนรุนแรงใหม่ในช่วงการแพร่ระบาด
Al Reesi et al. (2023) รายงานกรณีเด็กที่มีภาวะไตเรื้อรังเฉียบพลันและทุพโภชนาการ ซึ่งได้รับการรักษาจนหายขาดด้วยการรักษาเชิงรุกโดยใช้ liposomal amphotericin B (5→9 มก./กก./วัน) ร่วมกับ posaconazole และการผ่าตัดหลายครั้ง2) การวินิจฉัยตั้งแต่เนิ่นๆ ภายใน 24 ชั่วโมงและการรักษาเชิงรุกเป็นกุญแจสำคัญสู่ผลลัพธ์ที่ดี
Benlamkaddem S, Zdaik G, Doughmi D, et al. Rhino-Orbital Cerebral Mucormycosis: A Fatal Evolution. Cureus. 2023.
Al Reesi M, Al Muqbali T, Al Ajmi A, et al. Successful Management of Rhino-Orbital-Cerebral Mucormycosis in a Child with Acute-on-Chronic Kidney Disease and Malnutrition. Sultan Qaboos Univ Med J. 2023.
Kamath GM, Jeganathan S, Salim S, et al. Case series of central retinal artery occlusion in COVID-19-associated rhino-orbital-cerebral mucormycosis . Indian J Ophthalmol. 2023.
Siriwardena P, Wariyapperuma U, Nanayakkara P, et al. Rhino-orbital-cerebral mucormycosis in acute myeloid leukemia patients: a case series from Sri Lanka. BMC Infect Dis. 2024.
Yang F, Yang C, Li H, et al. Metagenomic next-generation sequencing in diagnosing rhino-orbital-cerebral mucormycosis presenting as cerebral infarction: a case series and diagnostic analysis of seven patients. Front Fungal Biol. 2026.
Ostovan VR, Rezapanah S, Behzadi Z, et al. Coronavirus disease (COVID-19) complicated by rhino-orbital-cerebral mucormycosis presenting with neurovascular thrombosis: a case report and review of literature. J Neurovirol. 2021.
Ponce-Rosas L, Gonzales-Zamora J, Diaz-Reyes N, et al. Rhino-Orbital-Cerebral Mucormycosis in a Post-COVID-19 Patient from Peru. Case Rep Infect Dis. 2022.
Alanazi RF, Almalki A, Alkhaibary A, et al. Rhino-Orbital-Cerebral Mucormycosis: A Rare Complication of Uncontrolled Diabetes. Case Rep Surg. 2022.
Mokhtar EA, Fatima Q, Akbar S, et al. Rhino-Orbital Cerebral Mucormycosis Causing Temporomandibular Joint Ankylosis: A Case Series of Two Patients. Cureus. 2023.
ถาม AI เกี่ยวกับบทความนี้
คัดลอกข้อความบทความแล้ววางในผู้ช่วย AI ที่คุณต้องการใช้
เปิดผู้ช่วย AI ด้านล่าง แล้ววางข้อความที่คัดลอกลงในช่องแชต