Prevalenza ed epidemiologia
Età e sesso prevalenti : età media 30,6 anni, femmine 62,3%, per lo più unilaterale
Coinvolgimento bilaterale : 9,8% raro
Tasso di recidiva : 3% raro

L’epitelite pigmentaria retinica acuta (Acute Retinal Pigment Epitheliitis; ARPE) è una rara malattia infiammatoria retinica idiopatica e autolimitante, descritta per la prima volta nel 1972 da Alex E. Krill e August F. Deutman1, 2, 4). È anche chiamata “malattia di Krill” dal nome dello scopritore. È classificata tra le sindromi dei punti bianchi.
Colpisce prevalentemente giovani adulti sani, con un’età media di 30,6 ± 10,7 anni (range 16-55 anni) e una predominanza femminile (62,3%)2). Si manifesta principalmente in modo unilaterale, con coinvolgimento bilaterale solo nel 9,8% dei casi. Le recidive sono rare (3%)2).
Un’associazione con infezione virale è riportata nel 25,9% dei casi2). Possono precedere sintomi simil-influenzali. Per quanto riguarda i farmaci, sono stati riportati casi dopo somministrazione di agonisti del recettore D2 della dopamina (bromocriptina, cabergolina) o bisfosfonati per via endovenosa1). Sono stati segnalati anche casi dopo vaccinazione anti-COVID-19 e antinfluenzale4).
Il concetto se l’ARPE sia una malattia indipendente o un tipo di altra malattia come MEWDS, pachicoroide, AMN, ecc., è ancora in discussione 1).
È una malattia estremamente rara. Anche nelle revisioni della letteratura, solo 29 articoli e 61 casi sono stati riportati, e l’incidenza esatta è sconosciuta. Ogni volta che viene segnalato un caso raro, il concetto di malattia viene rivisto.
L’esordio è acuto e presenta i seguenti sintomi.
Prevalenza ed epidemiologia
Età e sesso prevalenti : età media 30,6 anni, femmine 62,3%, per lo più unilaterale
Coinvolgimento bilaterale : 9,8% raro
Tasso di recidiva : 3% raro
Principali sintomi soggettivi
Visione offuscata e metamorfopsia : esordio acuto caratteristico
Scotoma centrale : corrisponde a lesione maculare
Discromatopsia : blu → verde, giallo → beige, rosso → grigio
Prognosi visiva
Acuità visiva iniziale : ≈20/40 (acuità corretta)
Acuità visiva finale : ≈20/20
Tasso di recupero completo : circa l’89% raggiunge 20/20 entro 2 mesi
Non si osservano anomalie del segmento anteriore né segni di infiammazione intraoculare4). All’esame del fondo oculare, si notano sottili macchie pigmentate circondate da un alone ipopigmentato giallo-biancastro nella regione maculare2, 4). L’aspetto caratteristico è un nucleo scuro centrale con un alone grigio-biancastro periferico.
L’acuità visiva iniziale è di circa 20/40 e, nella maggior parte dei casi, l’acuità visiva finale si ripristina a circa 20/202). Gli esami elettrofisiologici mostrano una riduzione dell’ampiezza dell’onda P50 del pERG e una riduzione della densità di risposta del mfERG, che riflettono una disfunzione maculare1).
Circa l’89% dei casi recupera 20/20 entro 2 mesi. Tuttavia, sono stati riportati recuperi incompleti in casi con rottura della zona ellissoidale (EZ) alla OCT persistente per oltre 12 mesi o in lesioni estese che raggiungono lo strato nucleare esterno (ONL) (vedere Reperti OCT).
La causa dell’ARPE è sconosciuta e la maggior parte dei casi è considerata idiopatica2). I fattori di rischio attualmente noti sono i seguenti.
Infezione virale (più comune) È stata riportata un’associazione con infezione virale nel 25,9% dei casi2). Sintomi simil-influenzali possono precedere l’insorgenza della malattia.
Dopo la vaccinazione È stato riportato un caso con insorgenza 31 giorni dopo la seconda dose del vaccino COVID-19. In questo caso, si sono verificati febbre lieve (37,3–37,5 °C) e dolori articolari per 2 giorni dopo la vaccinazione, e il vaccino antinfluenzale era stato somministrato 5 giorni prima 4). Bolletta et al. hanno riportato casi di infiammazione oculare 28–30 giorni dopo il vaccino COVID-19 4).
Farmacologico Sono stati riportati casi durante il trattamento dell’iperprolattinemia con agonisti del recettore D2 della dopamina (bromocriptina, cabergolina) 1). Esistono anche casi dopo somministrazione endovenosa di bifosfonati 1).
Sono stati riportati casi dopo vaccinazione anti-COVID-19 o antinfluenzale 4). La reazione immunitaria scatenata dalla vaccinazione potrebbe essere un fattore scatenante, ma la relazione causale non è ancora stabilita.
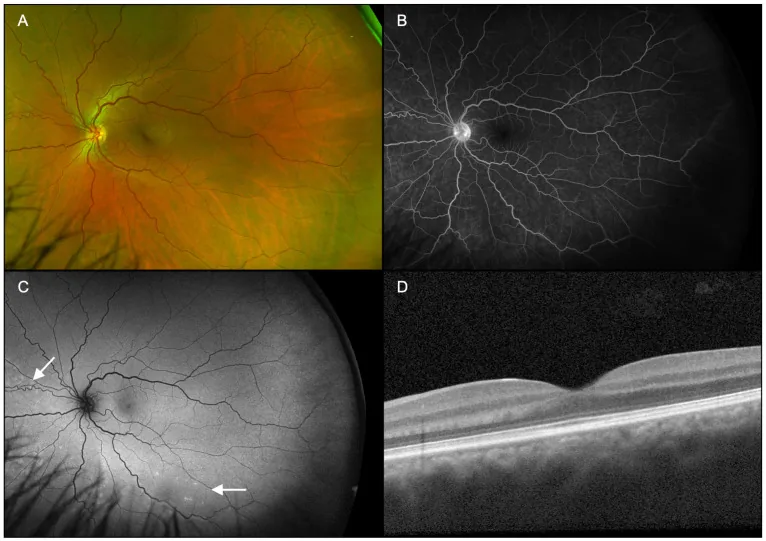
La diagnosi di ARPE si basa su una combinazione di più esami di imaging. Di seguito sono riportati i reperti caratteristici di ciascun esame.
L’OCT (tomografia a coerenza ottica) è lo strumento più importante per la diagnosi e il follow-up.
La frequenza di coinvolgimento di ogni strato retinico e la durata della guarigione sono mostrate di seguito.
| Strato coinvolto | Frequenza | Durata della guarigione |
|---|---|---|
| IZ (giunzione segmento interno/esterno) | 100% | 9,1±8,3 settimane |
| EZ (zona ellissoide) | 95,6% | 7,2±5,2 settimane |
| ELM (membrana limitante esterna) | 35,6% | 5,1±4,8 settimane |
I principali reperti sono i seguenti.
I reperti caratteristici di ciascuna modalità di imaging sono mostrati di seguito.
| Esame | Reperto caratteristico | Tasso di positività |
|---|---|---|
| FA | Iperfluorescenza da trasmissione, senza perdita | 83,6% |
| ICGA | Alone iperfluorescente a coccarda | 84,6% |
| Autofluorescenza del fondo oculare | Lieve iperfluorescenza della lesione | 40% |
È importante la diagnosi differenziale con le seguenti malattie 3, 4).
L’ARPE è una malattia autolimitante, con un miglioramento spontaneo previsto in 6-12 settimane. In linea di principio non è necessario alcun trattamento attivo 2).
L’osservazione è la base Molti rapporti mostrano un recupero visivo spontaneo senza trattamento. Nel caso di Kilic (2021), l’acuità visiva è tornata a 20/20 dopo un mese senza trattamento 1). Nel caso di ARPE post-vaccino di Sasajima et al. (2022), l’acuità visiva è tornata a 1,5 (equivalente a 20/13) dopo 5 settimane senza trattamento 4).
Efficacia degli steroidi non stabilita Sebbene esistano segnalazioni di casi di recupero dopo 6 mesi con steroidi orali 3), ci sono anche segnalazioni che il gruppo trattato con steroidi recuperi più lentamente del gruppo non trattato. La decisione di trattare e l’osservazione sono le linee guida di base.
In linea di principio non è necessario alcun trattamento e la guarigione spontanea avviene in 6-12 settimane. Non ci sono prove che la somministrazione di steroidi acceleri il recupero, anzi, alcuni rapporti suggeriscono un possibile ritardo. Si raccomanda un monitoraggio regolare con OCT.
La fisiopatologia dell’ARPE non è completamente compresa, ma sono state proposte diverse ipotesi.
Ipotesi del deficit di MerTK
Disturbo della fagocitosi dei POS: Deficit di MerTK → Accumulo di POS → Iperriflettività degli strati esterni → Degenerazione dei fotorecettori
Tre fasi del disturbo: Riconoscimento e legame (αvβ5 + MFG-E8), internalizzazione (attivazione di MerTK), digestione lisosomiale
Malattie correlate: Le mutazioni di MerTK causano retinite pigmentosa nell’uomo.
Ipotesi dell'ischemia coroidale
Risultati OCTA: Presenza di flow void nella coriocapillare.
Somiglianza con APMPPE: Ischemia coroidale primaria → danno secondario dei fotorecettori e dello strato delle fibre di Henle.
Comparsa di ASHH: L’iperriflettività dello strato delle fibre di Henle suggerisce un’associazione con l’ischemia coroidale.
Ipotesi del disturbo del ritmo circadiano
Alterazione del sistema dopaminergico: Gli agonisti del recettore D2 potrebbero indurre ARPE.
Anomalia dello shedding dei POS: L’orologio circadiano retinico controlla lo shedding dei dischi dei POS.
Stimolazione del recettore D2: Inibizione delle giunzioni gap cono-bastoncello → ridotta sensibilità alla luce dei fotorecettori.
La fagocitosi dei segmenti esterni dei fotorecettori (POS) da parte dell’RPE procede in tre fasi2).
Si ritiene che un deficit acuto e transitorio di MerTK sia centrale nella patogenesi dell’ARPE2). Le mutazioni di MerTK causano retinite pigmentosa nell’uomo, suggerendo una continuità patologica con l’ARPE.
I flow void della coriocapillare all’OCTA suggeriscono un meccanismo simile all’APMPPE 3). È stato proposto un meccanismo in cui l’ischemia coroidale primaria danneggia secondariamente i fotorecettori e lo strato delle fibre di Henle (HFL). I reperti OCT mostrano che la lesione principale dell’ARPE si trova negli strati retinici esterni piuttosto che nell’« epitelite pigmentaria ».
Sebbene la malattia sia chiamata « epitelite pigmentaria », i reperti OCT mostrano che gli strati retinici esterni, come IZ (giunzione segmento interno/esterno) e EZ (zona ellissoidale), sono principalmente coinvolti. IZ è coinvolta nel 100% dei casi, EZ nel 95,6%, mentre le anomalie dell’EPR/membrana di Bruch si riscontrano solo nell’8,9% dei casi 2). Le alterazioni dell’EPR sono probabilmente secondarie.
Il dibattito sul fatto che l’ARPE sia o meno un’entità patologica indipendente è ancora in corso. Due posizioni si contrappongono: quella che nega l’entità indipendente considerandola un « mito diagnostico » e quella che la sostiene come « non un mito diagnostico » 1, 3). Vengono esaminate le relazioni con MEWDS, AMN, APMPPE e la possibilità di inclusione nello spettro pachicoroideo.
Sen et al. (2025) hanno riportato l’ASHH (Angular Sign of Henle Fiber Layer Hyperreflectivity) in casi presunti di ARPE 3).
Sen et al. (2025) hanno identificato l’ASHH e i flow void della coriocapillare all’OCTA in casi presunti di ARPE, suggerendo che l’ischemia coroidale potrebbe essere coinvolta nella patogenesi dell’ARPE 3). È stato proposto di considerare l’ARPE come una delle diagnosi differenziali della pachicoroide pigment epitheliopathy.
Sasajima et al. (2022) hanno riportato un caso di ARPE insorto 31 giorni dopo la seconda dose del vaccino anti-COVID-19 4). Le interruzioni di EZ/IZ all’OCT si sono riparate in 5 settimane e l’acuità visiva è tornata a 1,5. È stata avanzata l’ipotesi che la reazione immunitaria post-vaccinale prenda di mira l’EPR o la retina esterna, provocando infiammazione.
L’ipotesi di deficit di MerTK è attualmente ancora a livello di ipotesi e necessita di una validazione diretta su casi umani2). Tuttavia, il fatto che l’ARPE possa essere indotta anche da farmaci (agonisti del recettore D2) attira l’attenzione sul meccanismo secondo cui il disturbo del ritmo circadiano retinico mediato dal sistema dopaminergico altera l’eliminazione dei POS1, 2).