Prévalence et épidémiologie
Âge et sexe prédominants : âge moyen 30,6 ans, femmes 62,3 %, majoritairement unilatéral
Atteinte bilatérale : rare, 9,8 %
Taux de récidive : rare, 3 %

L’épithéliite pigmentaire rétinienne aiguë (Acute Retinal Pigment Epitheliitis ; ARPE) est une maladie inflammatoire rétinienne rare, idiopathique et auto-limitée, décrite pour la première fois en 1972 par Alex E. Krill et August F. Deutman1, 2, 4). Elle est également appelée « maladie de Krill » d’après le nom de son découvreur. Elle est classée parmi les syndromes des points blancs.
Elle survient principalement chez les jeunes adultes en bonne santé, avec un âge moyen de 30,6 ± 10,7 ans (extrêmes 16-55 ans) et une prédominance féminine (62,3 %)2). Elle est le plus souvent unilatérale, l’atteinte bilatérale ne représentant que 9,8 % des cas. Les récidives sont rares (3 %)2).
Une association avec une infection virale est rapportée dans 25,9 % des cas2). Des symptômes pseudo-grippaux peuvent précéder l’apparition. Des cas ont été rapportés après administration d’agonistes des récepteurs D2 de la dopamine (bromocriptine, cabergoline) ou de bisphosphonates par voie intraveineuse1). Des cas après vaccination contre la COVID-19 ou la grippe ont également été signalés4).
Le concept de savoir si l’ARPE est une maladie indépendante ou un type d’autre maladie comme le MEWDS, la pachychoroïde, l’AMN, etc., fait toujours l’objet de débats 1).
C’est une maladie extrêmement rare. Même dans les revues de la littérature, seulement 29 articles et 61 cas ont été rapportés, et le taux d’incidence exact est inconnu. Chaque fois qu’un cas rare est signalé, le concept de la maladie est révisé.
Le début est aigu et présente les symptômes suivants.
Prévalence et épidémiologie
Âge et sexe prédominants : âge moyen 30,6 ans, femmes 62,3 %, majoritairement unilatéral
Atteinte bilatérale : rare, 9,8 %
Taux de récidive : rare, 3 %
Principaux symptômes subjectifs
Vision floue et métamorphopsie : apparition aiguë caractéristique
Scotome central : correspond à une lésion maculaire
Dyschromatopsie : bleu → vert, jaune → beige, rouge → gris
Pronostic visuel
Acuité visuelle initiale : ≈20/40 (acuité corrigée)
Acuité visuelle finale : ≈20/20
Taux de récupération complète : environ 89% atteignent 20/20 en 2 mois
Aucune anomalie du segment antérieur ni signe d’inflammation intraoculaire n’est observé4). Au fond d’œil, on note de fines taches pigmentaires entourées d’un halo hypopigmenté jaune-blanc dans la région maculaire2, 4). L’aspect caractéristique est celui d’un noyau sombre central avec un halo gris-blanc périphérique.
L’acuité visuelle initiale est d’environ 20/40 et, dans la plupart des cas, l’acuité visuelle finale se rétablit à environ 20/202). Les examens électrophysiologiques montrent une diminution de l’amplitude de l’onde P50 du pERG et une réduction de la densité de réponse du mfERG, reflétant un dysfonctionnement maculaire1).
Environ 89% des cas récupèrent une acuité de 20/20 en moins de 2 mois. Cependant, des cas de récupération incomplète ont été rapportés lorsque la rupture de la zone ellipsoïde (EZ) à l’OCT persiste plus de 12 mois ou en cas de lésions étendues atteignant la couche nucléaire externe (ONL) (voir Signes OCT).
La cause de l’ARPE est inconnue et la plupart des cas sont considérés comme idiopathiques2). Les facteurs de risque actuellement connus sont les suivants.
Infection virale (la plus fréquente) Une association avec une infection virale a été rapportée dans 25,9% des cas2). Des symptômes pseudo-grippaux peuvent précéder l’apparition de la maladie.
Après la vaccination Un cas a été rapporté avec apparition 31 jours après la deuxième dose du vaccin COVID-19. Dans ce cas, une fièvre légère (37,3–37,5 °C) et des douleurs articulaires ont été observées pendant 2 jours après la vaccination, et le vaccin contre la grippe avait également été administré 5 jours auparavant 4). Bolletta et al. ont rapporté des cas d’inflammation oculaire survenant 28 à 30 jours après le vaccin COVID-19 4).
Médicamenteux Des cas ont été rapportés lors du traitement de l’hyperprolactinémie par des agonistes des récepteurs D2 de la dopamine (bromocriptine, cabergoline) 1). Il existe également des cas après injection intraveineuse de bisphosphonates 1).
Des cas ont été rapportés après la vaccination contre la COVID-19 ou la grippe 4). La réaction immunitaire déclenchée par la vaccination pourrait être un déclencheur, mais la relation de cause à effet n’est pas encore établie.
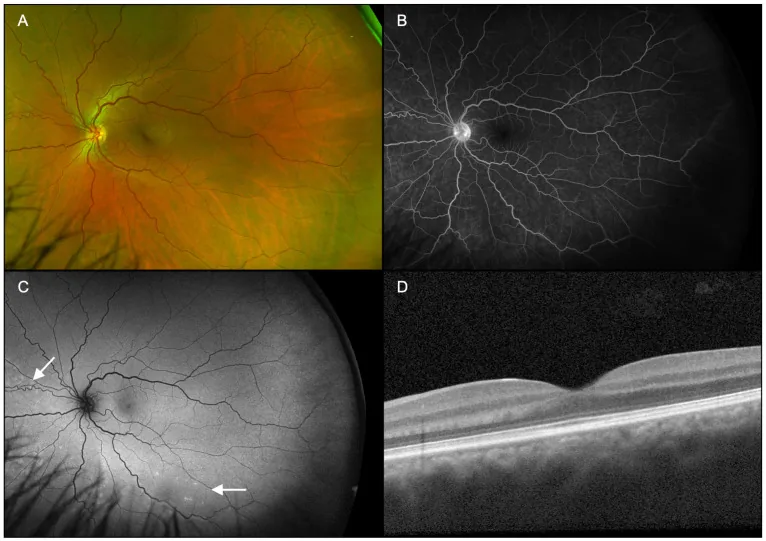
Le diagnostic de l’ARPE repose sur une combinaison d’examens d’imagerie multiples. Les caractéristiques de chaque examen sont présentées ci-dessous.
L’OCT (tomographie par cohérence optique) est l’outil le plus important pour le diagnostic et le suivi.
La fréquence d’atteinte de chaque couche rétinienne et la durée de guérison sont présentées ci-dessous.
| Couche atteinte | Fréquence | Durée de guérison |
|---|---|---|
| IZ (jonction segment interne/externe) | 100 % | 9,1 ± 8,3 semaines |
| EZ (zone ellipsoïde) | 95,6 % | 7,2 ± 5,2 semaines |
| ELM (membrane limitante externe) | 35,6 % | 5,1 ± 4,8 semaines |
Les principales observations sont les suivantes.
Les signes caractéristiques de chaque modalité d’imagerie sont présentés ci-dessous.
| Examen | Signes caractéristiques | Taux de positivité |
|---|---|---|
| FA | Hyperfluorescence par transmission, sans fuite | 83,6 % |
| ICGA | Halos hyperfluorescents en cocarde | 84,6 % |
| Autofluorescence du fond d’œil | Hyperfluorescence légère de la lésion | 40% |
Le diagnostic différentiel avec les maladies suivantes est important 3, 4).
L’ARPE est une maladie spontanément résolutive, avec une amélioration naturelle attendue en 6 à 12 semaines. En principe, aucun traitement actif n’est nécessaire 2).
La surveillance est la base De nombreux rapports montrent une récupération visuelle spontanée sans traitement. Dans le cas de Kilic (2021), l’acuité visuelle est revenue à 20/20 après un mois sans traitement 1). Dans le cas d’ARPE post-vaccinal de Sasajima et al. (2022), l’acuité visuelle est revenue à 1,5 (équivalent 20/13) après 5 semaines sans traitement 4).
Efficacité des stéroïdes non établie Bien qu’il existe des rapports de cas de récupération après 6 mois sous corticostéroïdes oraux 3), certains rapports indiquent que le groupe traité par stéroïdes récupère plus lentement que le groupe non traité. La décision de traitement et la surveillance sont les principes de base.
En principe, aucun traitement n’est nécessaire et la guérison spontanée survient en 6 à 12 semaines. Il n’existe aucune preuve que l’administration de stéroïdes accélère la récupération, et certains rapports suggèrent même qu’elle pourrait la retarder. Une surveillance régulière par OCT est recommandée.
La physiopathologie de l’ARPE n’est pas complètement élucidée, mais plusieurs hypothèses ont été proposées.
Hypothèse du déficit en MerTK
Trouble de la phagocytose des POS : Déficit en MerTK → Accumulation de POS → Hyperréflectivité des couches externes → Dégénérescence des photorécepteurs
Trois étapes du trouble : Reconnaissance et liaison (αvβ5 + MFG-E8), internalisation (activation de MerTK), digestion lysosomale
Maladies associées : Les mutations de MerTK provoquent une rétinite pigmentaire chez l’homme.
Hypothèse de l'ischémie choroïdienne
Résultats OCTA : Présence de flow void dans la choriocapillaire.
Similitude avec l’APMPPE : Ischémie choroïdienne primaire → lésions secondaires des photorécepteurs et de la couche des fibres de Henle.
Apparition d’ASHH : L’hyperréflectivité de la couche des fibres de Henle suggère un lien avec l’ischémie choroïdienne.
Hypothèse du trouble du rythme circadien
Dérèglement du système dopaminergique : Les agonistes des récepteurs D2 pourraient induire une ARPE.
Anomalie de l’élimination des POS : L’horloge circadienne rétinienne contrôle l’élimination des disques des segments externes des photorécepteurs.
Stimulation des récepteurs D2 : Inhibition des jonctions gap cône-bâtonnet → diminution de la sensibilité lumineuse des photorécepteurs.
La phagocytose des segments externes des photorécepteurs (POS) par l’EPR se déroule en trois étapes2).
Un déficit aigu et transitoire en MerTK est supposé être au cœur de la pathogénie de l’ARPE2). Les mutations de MerTK sont connues pour provoquer une rétinite pigmentaire chez l’homme, suggérant une continuité pathologique avec l’ARPE.
Les zones de non-perfusion (flow void) du choriocapillaire en OCTA suggèrent un mécanisme similaire à l’APMPPE 3). Un mécanisme a été proposé selon lequel une ischémie choroïdienne primaire endommage secondairement les photorécepteurs et la couche des fibres de Henle (HFL). Les résultats OCT montrent que la lésion principale de l’ARPE se situe dans les couches rétiniennes externes plutôt que dans l’« épithélite pigmentaire ».
Bien que la maladie soit appelée « épithélite pigmentaire », les résultats OCT montrent que les couches rétiniennes externes, telles que l’IZ (jonction segment interne/segment externe) et l’EZ (bande ellipsoïde), sont principalement touchées. L’IZ est atteinte dans 100 % des cas, l’EZ dans 95,6 %, tandis que les anomalies de l’EPR/membrane de Bruch ne sont observées que dans 8,9 % des cas 2). Les modifications de l’EPR sont probablement secondaires.
Le débat se poursuit quant à savoir si l’ARPE est une entité pathologique indépendante. Deux positions s’opposent : celle qui nie l’entité indépendante en la considérant comme un « mythe diagnostique » et celle qui la soutient comme « non un mythe diagnostique » 1, 3). Les relations avec MEWDS, AMN, APMPPE et la possibilité d’inclusion dans le spectre pachychoroïdien sont examinées.
Sen et al. (2025) ont rapporté l’ASHH (Angular Sign of Henle Fiber Layer Hyperreflectivity) dans des cas présumés d’ARPE 3).
Sen et al. (2025) ont identifié l’ASHH et les zones de non-perfusion du choriocapillaire en OCTA dans des cas présumés d’ARPE, suggérant que l’ischémie choroïdienne pourrait être impliquée dans la pathogénie de l’ARPE 3). Il a été proposé de considérer l’ARPE comme l’un des diagnostics différentiels de la pachychoroid pigment epitheliopathy.
Sasajima et al. (2022) ont rapporté un cas d’ARPE survenu 31 jours après la deuxième dose du vaccin contre la COVID-19 4). Les ruptures de l’EZ/IZ à l’OCT se sont réparées en 5 semaines et l’acuité visuelle est revenue à 1,5. L’hypothèse a été émise que la réaction immunitaire post-vaccinale cible l’EPR ou la rétine externe, provoquant une inflammation.
L’hypothèse de déficit en MerTK reste pour l’instant au stade d’hypothèse et nécessite une validation directe sur des cas humains2). Cependant, le fait que l’ARPE puisse également être induite par des médicaments (agonistes des récepteurs D2) attire l’attention sur le mécanisme selon lequel les troubles du rythme circadien rétinien médiés par la dopamine perturbent l’élimination des POS1, 2).