Einfache Episkleritis
Häufigkeit: häufiger
Beginn: plötzlich
Verlauf: erreicht nach etwa 12 Stunden seinen Höhepunkt und klingt nach 2–3 Tagen ab
Befund: sektorförmige (ca. 67 %) oder diffuse (ca. 33 %) Rötung

Episkleritis ist eine gutartige, selbstlimitierende kongestive Erkrankung des episkleralen Gewebes. Es handelt sich um eine Entzündung der oberflächlichen Gefäßplexus, wie des Tenon-Kapsel-Gefäßplexus. Im Vergleich zur Skleritis, die tiefere Gefäße betrifft, sind die Schmerzen geringer und die Auswirkungen auf das Sehvermögen geringer. Die meisten Fälle sind idiopathisch und rezidivierend, mit einer Tendenz zur bilateralen Beteiligung. Die jährliche Inzidenz wird mit 41,0 pro 100.000 Personen und die Prävalenz mit 52,6 angegeben.
Obwohl sie zu den relativ häufigen Ursachen für Rötung gehört, wird sie oft mit Konjunktivitis oder Skleritis verwechselt, und Fehldiagnosen beim ersten Besuch sind nicht selten. Bei dieser Erkrankung ist das Skleraparenchym selbst nicht betroffen, und ein Fortschreiten zu schwerwiegenden strukturellen Komplikationen wie einer Augenperforation tritt fast nie auf. Bei rezidivierenden Fällen oder solchen mit systemischen Autoimmunerkrankungen wie rheumatoider Arthritis oder Granulomatose mit Polyangiitis sind jedoch die Behandlung der Grunderkrankung und eine langfristige Nachsorge erforderlich. Das Verständnis der Episkleritis nicht als isolierte Augenerkrankung, sondern als „okuläre Manifestation“ einer systemischen Erkrankung ist entscheidend für das Rezidivmanagement und die Prognoseverbesserung.
Die Watson-Klassifikation wird häufig für die klinische Klassifikation entzündlicher Erkrankungen der Sklera und Episklera verwendet. Nach Lokalisation werden sie in drei Gruppen eingeteilt: Episkleritis, anteriore Skleritis und posteriore Skleritis. Die anteriore Skleritis wird weiter nach Form in diffuse, noduläre und nekrotisierende (entzündlich/nicht entzündlich) Typen unterteilt. Ein wichtiger Unterschied zur anterioren Skleritis ist, dass die Episkleritis keinen nekrotisierenden Typ aufweist und morphologisch in zwei Typen eingeteilt wird: einfache (diffuse Form) und noduläre. Diese Klassifikation spiegelt die Entzündungstiefe (oberflächlich oder tief) und den Schweregrad des Verlaufs und der Prognose wider, daher bildet die Bestimmung des Krankheitstyps zum Zeitpunkt der Diagnose die Grundlage für die Behandlungsstrategie und die Prognoseerklärung. Die Episkleritis wird in dieser Klassifikation als die mildeste Gruppe mit der besten Prognose eingestuft.
Einfache Episkleritis
Häufigkeit: häufiger
Beginn: plötzlich
Verlauf: erreicht nach etwa 12 Stunden seinen Höhepunkt und klingt nach 2–3 Tagen ab
Befund: sektorförmige (ca. 67 %) oder diffuse (ca. 33 %) Rötung
Noduläre Episkleritis
Häufigkeit: etwas seltener
Beginn: langsam
Verlauf: neigt dazu, länger anzuhalten als die einfache Form
Befund: lokalisierter episkleraler Knoten in der Nähe des Hornhautlimbus (beweglich)
Die Sklera besteht aus drei Schichten: Episklera, Sklerastroma und Lamina fusca. Die Episklera ist ein Bindegewebe mit Blutgefäßen über dem Sklerastroma und wird als fibroelastische Struktur zwischen Sklerastroma und Tenon-Kapsel verstanden. Sie besteht aus zwei Schichten: der äußeren parietalen Schicht (oberflächliches episklerales Kapillarnetz) und der inneren viszeralen Schicht (stark anastomosierendes Gefäßnetz), wobei beide Gefäßnetze aus den vorderen Ziliararterien stammen. Die meisten Nervenfasern sind Äste des Nervus trigeminus. Die Episklera bildet zwischen dem Ansatz der geraden Augenmuskeln und dem Limbus einen episkleralen Gefäßplexus, der normalerweise von der Bindehaut verdeckt wird, sich aber bei Entzündung erweitert und eine helle Rötung verursacht. Die Episklera wird nach hinten zum Augapfel hin allmählich dünner, wo die Tenon-Kapsel vorherrscht.
Es besteht kein Druckschmerz und kein Augenausfluss. Bei starken Schmerzen oder deutlichem Augenausfluss sollte eine Skleritis, infektiöse Konjunktivitis oder anteriore Uveitis in Betracht gezogen werden. Die Symptome klingen oft innerhalb weniger Tage ab oder verschwinden vollständig, ohne die Sehfunktion zu beeinträchtigen. Bei einem Rezidiv tritt es oft an derselben Stelle oder am anderen Auge auf, und der Patient bemerkt es oft als „das übliche rote Auge“. Starke Schmerzen, die den Nachtschlaf stören, wie bei Skleritis, oder starker Druckschmerz beim Berühren des Oberlids werden bei Episkleritis in der Regel nicht beobachtet.
Die Beobachtung von Lokalisation und Farbe der Rötung ist der Kern der Differentialdiagnose. Die Rötung bei Episkleritis ist hellrot bis rosa, im Gegensatz zur dunkelroten (purpurroten) tiefen Rötung bei Skleritis.
| Befund | Episkleritis | Skleritis |
|---|---|---|
| Farbe der Rötung | Hellrot bis rosa | Dunkelrot (purpurrot) |
| Schmerz | Leicht bis nicht vorhanden | Stark und ausstrahlend |
| Beweglichkeit des Knotens | Vorhanden | Nicht vorhanden |
Die Sehschärfe ist in der Regel normal. Bindehautödem, erhöhter Augeninnendruck, anteriore Uveitis und Keratitis sind seltene Komplikationen; bei Vorliegen dieser sollte an eine Skleritis oder andere Erkrankungen gedacht werden. Das Fehlen von Entzündungszeichen der Lidbindehaut ist hilfreich zur Abgrenzung von einer Konjunktivitis. Bei Skleritis kann sich die Entzündung auf das umliegende Gewebe ausbreiten und zu limbischen Infiltraten, Ulzera oder anteriorer Uveitis führen, während die Episkleritis selbstlimitierend ist und benachbarte Gewebe fast nie einbezieht. An der Spaltlampe die Ebene des skleralen Gefäßplexus identifizieren; wenn trotz einer roten erhabenen Läsion die Skleralgefäße nicht sichtbar sind, sollte auch an eine tumoröse Läsion gedacht werden.
Die Episkleritis ist gekennzeichnet durch fehlenden Augenausfluss und eine auf die Nähe des Hornhautlimbus begrenzte Rötung. Die Konjunktivitis ist in der Regel schmerzlos, mit Ausfluss, und die Rötung ist am stärksten im Fornix und nimmt zum Limbus hin ab. An der Spaltlampe sind die episkleralen Gefäße nicht beweglich, während die Bindehautgefäße beweglich sind. Siehe Abschnitt „Diagnose und Untersuchungsmethoden“ für Details.
Die meisten Fälle sind idiopathisch (Ursache unbekannt), wobei bei etwa 26–36 % aller Fälle eine systemische Erkrankung assoziiert ist. Auch bei idiopathischen Fällen wird ein immunologischer Mechanismus vermutet, der auf einer lymphozytenbetonten unspezifischen Entzündungsreaktion im oberflächlichen episkleralen Gefäßplexus beruht. Der rezidivierende Verlauf und die Tendenz zur bilateralen Beteiligung deuten auf eine zugrunde liegende systemische Immunregulationsstörung hin.
Kollagenosen und Autoimmunerkrankungen (am häufigsten rheumatoide Arthritis) 1) :
Vaskulitis:
Infektionen: Bakterien, Mykobakterien, Syphilis, Lyme-Borreliose, Herpesviren, Gürtelrose usw. können Ursachen sein. Eine Episkleritis im Zusammenhang mit einem Herpes zoster ophthalmicus wird eher als Immunantwort auf den Erreger denn als direkte Infektion angesehen. Es wurde auch ein Fall einer subkonjunktivalen Parasitose durch Dirofilaria repens berichtet, der fälschlicherweise als Episkleritis diagnostiziert wurde7).
Sonstiges: Gicht, Atopie, Fremdkörper, chemisches Trauma, Medikamente (Topiramat, Pamidronat) und Berichte als Frühsymptom von COVID-19.
Ja, bei etwa 30 % der Patienten liegt eine systemische Erkrankung vor. Am häufigsten ist die rheumatoide Arthritis, aber sie kann auch das erste Symptom von Erkrankungen wie Granulomatose mit Polyangiitis (GPA) oder Morbus Behçet sein, bei denen eine frühzeitige Diagnose und Behandlung die Prognose beeinflussen. Bei wiederholten Rückfällen oder systemischen Symptomen wird eine systemische Abklärung mit Rheumafaktor, antinukleären Antikörpern, ANCA und Urinuntersuchung empfohlen.
Die Episkleritis ist eine klinische Diagnose, die hauptsächlich auf Anamnese und Spaltlampenuntersuchung basiert. Die sorgfältige Beobachtung der Ebene der Skleragefäße (oberflächlich oder tief), der Farbton der Rötung, das Vorhandensein von Knoten sowie Ausdünnung/Nekrose ist grundlegend.
Phenylephrin 2,5 % verengt die Bindehautgefäße und hilft bei der Unterscheidung zwischen Konjunktivitis und Episkleritis. Phenylephrin 10 % verengt das oberflächliche episklerale Gefäßnetz, nicht jedoch das tiefe, und ermöglicht so die Unterscheidung zwischen Episkleritis und Skleritis.
Der Reaktionstest mit 1:1000 verdünntem Epinephrin ist eine einfache Methode, um die Beteiligung tiefer Gefäße zu beurteilen. Wenn die Rötung nach der Gabe verschwindet, spricht dies für eine Episkleritis; bleibt sie bestehen, für eine Skleritis. Die Beurteilung erfolgt durch Kombination von Anzahl und Beweglichkeit der Knoten, Schmerz/Druckschmerz und der Epinephrin-Reaktion.
Die Reaktionstests mit Epinephrin und Phenylephrin sind besonders hilfreich als ergänzende Diagnose, wenn die Schichtstruktur der Rötung mit der Spaltlampe nicht direkt beurteilt werden kann oder die Knoten klein sind. Die Beobachtung 10–15 Minuten nach der Gabe beurteilt die Verengung der oberflächlichen Gefäße; bleibt die Rötung der tiefen Gefäße bestehen, wird die Behandlung einer Skleritis priorisiert.
Die Tenon-Kapsulitis wird ebenfalls als eine Form der Episkleritis angesehen, und die klinische Unterscheidung zwischen beiden ist schwierig. Die Beurteilung erfolgt anhand der Beweglichkeit der Knoten, des Vorhandenseins von Schmerzen/Druckempfindlichkeit, der Reaktion auf Epinephrin-Augentropfen und der Fluorescein-Anfärbung.
Bei einer einzelnen, leichten Episkleritis ist eine umfassende systemische Abklärung nicht erforderlich. Bei wiederholten Rezidiven oder systemischen Symptomen sollten die folgenden Untersuchungen in Betracht gezogen werden.
In Fällen, in denen eine Episkleritis als Erstmanifestation einer Granulomatose mit Polyangiitis auftritt, kann eine Nierenfunktionsstörung vorliegen 3). Wenn sowohl eine Augenentzündung als auch eine Nierenfunktionsstörung festgestellt werden, sollte umgehend eine systemische Vaskulitis, einschließlich Granulomatose mit Polyangiitis, gesucht werden. Bei therapierefraktärer oder rezidivierender Episkleritis ist es wünschenswert, in Zusammenarbeit mit Rheumatologie und Innerer Medizin die Krankheitsaktivität zu beurteilen und eine Behandlung der Grunderkrankung einzuleiten.
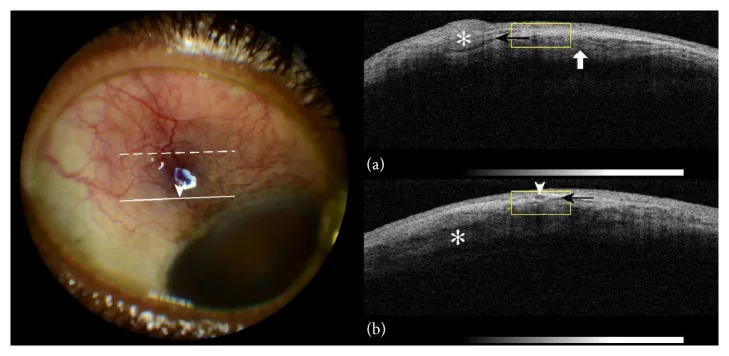
Neben der Beurteilung mit der Spaltlampe können die Dicke der episkleralen Schicht und der Gefäßverlauf mittels optischer Kohärenztomographie des vorderen Augenabschnitts (AS-OCT) und die Skleradicke mittels Ultraschall (B-Mode) als Hilfsdiagnostik eingesetzt werden. Zum Ausschluss einer nekrotisierenden Skleritis oder zur Beurteilung einer hinteren Skleritis wird im Ultraschall das T-Zeichen (Flüssigkeitsansammlung um die Optikusscheide) überprüft. Bei einer typischen Episkleritis fehlen in diesen bildgebenden Verfahren oft spezifische Befunde, und die Diagnose wird durch eine Kombination aus Spaltlampenuntersuchung, Anamnese und systemischer Abklärung gestellt.
Die meisten Episkleritiden heilen ohne Behandlung innerhalb weniger Tage bis Wochen spontan aus. Die Aufklärung des Patienten über die Gutartigkeit der Erkrankung, den natürlichen Verlauf und die Notwendigkeit einer systemischen Abklärung sowie die Vermittlung von Beruhigung sind der erste Schritt der Behandlung. Kälteanwendungen und gekühlte künstliche Tränen sind wirksam, um subjektive Symptome wie Reizung und Wärmegefühl zu lindern. Bei leichten Fällen ist keine aktive medikamentöse Intervention erforderlich; eine kurzfristige Nachkontrolle in Abständen von wenigen Tagen zur Bestätigung der spontanen Besserung kann Rebound-Effekte und Nebenwirkungen der Behandlung vermeiden.
Niedrig konzentrierte Steroid-Augentropfen sind die erste Wahl. Oft werden zusätzlich antibiotische Augentropfen verabreicht, um eine Skleritis abzugrenzen.
Bei unzureichendem Ansprechen auf die Augentropfen sollte ein Wechsel zur Untersuchung und Behandlung einer Skleritis erwogen werden. Steroid-Augentropfen unterdrücken zwar schnell die Symptome, können aber bei längerer oder wiederholter Anwendung das Rezidivrisiko erhöhen und eine Rebound-Hyperämie auslösen.
Die Behandlung basiert auf einer schrittweisen Reduktion und Beendigung nach Abklingen der Symptome; eine wahllose Fortführung ist zu vermeiden. Die langfristige Anwendung von Steroid-Augentropfen birgt das Risiko eines steroidreaktiven Augeninnendruckanstiegs und einer hinteren subkapsulären Katarakt. Daher sollte nach Bestätigung der Besserung innerhalb von 1–2 Wochen die Dosis reduziert werden. Bei Rezidiven ist die Krankheitsaktivität jedes einzelnen Schubs individuell zu bewerten und die Optimierung der Behandlung der zugrunde liegenden systemischen Erkrankung zu priorisieren.
Bei Episkleritis in Verbindung mit Kollagenosen wie rheumatoider Arthritis hat die Behandlung der Grunderkrankung direkten Einfluss auf die Prognose 1). Bei Resistenz gegen die Lokalbehandlung wird Prednisolon oral (20–30 mg/Tag mit ausschleichender Therapie) ergänzt. Außer bei offensichtlicher systemischer Entzündungserkrankung sind Fälle, die eine systemische Steroidgabe erfordern, äußerst selten.
Bei Episkleritis im Rahmen einer Granulomatose mit Polyangiitis ist eine Remissionsinduktionstherapie mit Cyclophosphamid oder Rituximab wirksam 3)4). Rituximab zeigt im Vergleich zu Cyclophosphamid eine höhere Remissionsrate nach 6 Monaten (64 % vs. 53 %) 3).
Steroid-Augentropfen unterdrücken die Symptome der Episkleritis schnell, können aber nach dem Absetzen einen „Rebound“ mit Rötung und möglicherweise stärkerem Wiederaufflammen verursachen. Daher ist der Einsatz von Steroiden umstritten; bei leichten Fällen wird von manchen eine abwartende Beobachtung ohne Behandlung oder die Priorisierung von NSAIDs befürwortet. Bei wiederholten Rezidiven werden COX2-Hemmer oral oder die Abklärung einer systemischen Erkrankung empfohlen.
Der Entstehungsmechanismus der Episkleritis ist noch nicht vollständig geklärt. Im betroffenen Bereich kommt es zu einer Erweiterung und Kongestion des oberflächlichen episkleralen Gefäßnetzes sowie zu einer Infiltration von Entzündungszellen, hauptsächlich Lymphozyten, in die Episklera und die Tenon-Kapsel. Der wesentliche Unterschied zur Skleritis besteht darin, dass das Skleraparenchym selbst nicht betroffen ist. Die entzündliche Zellinfiltration besteht hauptsächlich aus T-Zellen und wenigen Plasmazellen; eine neutrophilen-dominierte eitrige Entzündung oder Granulombildung wird normalerweise nicht beobachtet.
Histopathologisch handelt es sich um eine nicht-granulomatöse Entzündung, die hauptsächlich durch Vasodilatation und lymphozytäre Infiltration gekennzeichnet ist. Bei der nodulären Episkleritis findet sich im Zentrum der Läsion eine fibrinoide Nekrose, umgeben von einer Anordnung epitheloider Zellen. Diese Befunde ähneln denen der granulomatösen Entzündung bei Skleritis, und einige Autoren betrachten Episkleritis und Skleritis als ein Spektrum, das sich in der Tiefe der Entzündung unterscheidet. Die bei der Episkleritis beobachtete kleinherdige fibrinoide Nekrose kann als milde Form der ausgedehnteren nekrotischen Veränderungen bei der Skleritis verstanden werden.
Das Fortschreiten der Entzündung erhöht die Produktion reaktiver Sauerstoffspezies (ROS) und verstärkt den oxidativen Stress2). Die Gesamtmenge an Vitamin C in der menschlichen Netzhaut ist etwa 20-mal höher als im Plasma, und das Augengewebe ist stark auf das antioxidative System angewiesen. Bei der autoimmunen Episkleritis wurde vermutet, dass eine verminderte Funktion dieses antioxidativen Systems zu chronischer Entzündung und Gewebeschädigung der Episklera führen könnte2). ROS schädigen das Gefäßendothel und induzieren die Freisetzung von Entzündungszytokinen, was zu anhaltender Vasodilatation und erhöhter Permeabilität führt. Die chronische Exposition der Augenoberfläche und der Episklera gegenüber oxidativem Stress wird als ein Faktor für die rezidivierende Episkleritis angesehen, und die therapeutische Bedeutung einer antioxidativen Intervention wird untersucht.
Klinisch geht eine Episkleritis nur selten direkt in eine Skleritis über. Andererseits zeigt die Mehrzahl der Skleritisfälle auch eine Entzündung der Episklera (episkleritische Veränderungen), sodass beide nicht als völlig unabhängige Erkrankungen, sondern als ein Kontinuum verstanden werden, das sich in der Tiefe der betroffenen Gefäßschichten unterscheidet. Die Episkleritis betrifft hauptsächlich das oberflächliche episklerale Gefäßnetz (parietale Schicht), während die Skleritis das tiefe Gefäßnetz bis zum Skleraparenchym betrifft.
An der Ansatzstelle der geraden Augenmuskeln ist die Sklera mit etwa 0,3 mm am dünnsten, was ihre Anfälligkeit für Entzündungen und Traumata erhöht. Das episklerale Gefäßgeflecht wird über die vorderen Ziliararterien reichlich mit Blut versorgt, sodass sich eine Kongestion bei Entzündung schnell manifestiert. Die Sklera selbst ist dagegen ein gefäßarmes Gewebe, und eine tiefe Entzündung wie die Skleritis ist selten. Die anatomische Besonderheit, dass sich die von den vorderen Ziliararterien stammenden Gefäße bei der Episkleritis reversibel kongestionieren, ist die mechanistische Grundlage für das schnelle Abklingen der Kongestion im Epinephrin-Tropftest; das Fehlen dieser Reaktion bei der tiefen Skleravaskulitis ist ein pathophysiologisches Differenzialdiagnosekriterium.
Ein Fallbericht beschreibt einen 60-jährigen Mann mit idiopathischer rezidivierender Episkleritis, der nach Beginn einer oralen Einnahme von 500 mg/Tag Vitamin C 7 Monate lang keinen Rückfall erlitt 2). Vitamin C ist ein starkes Antioxidans, das durch Reduzierung von oxidativem Stress Entzündungen des Augengewebes unterdrücken könnte. Das Augengewebe ist stark vom Antioxidantiensystem abhängig; die Vitamin-C-Konzentration in der Netzhaut erreicht etwa das 20-fache des Plasmas. Eine Supplementierung mit Vitamin C und anderen antioxidativen Nährstoffen könnte eine Kandidatenstrategie zur Rückfallprävention sein 2). Zur Bestätigung der Wirksamkeit sind jedoch kontrollierte Fall-Kontroll-Studien und klinische Studien erforderlich 2). Derzeit wird sie nur ergänzend bei schweren Rückfällen oder Fällen mit trockenem Auge und chronischer Entzündung der Augenoberfläche in Betracht gezogen.
Die Granulomatose mit Polyangiitis (GPA) ist eine tödliche Erkrankung mit einer 1-Jahres-Mortalität von 80 % unbehandelt, aber durch Immunsuppression kann die Mortalität auf 10 % gesenkt werden 3). Da eine Episkleritis das erste Symptom einer GPA sein kann, sollten Augenärzte diesen Zusammenhang erkennen und bei rezidivierender Episkleritis aktiv systemische Untersuchungen durchführen 3)4). Insbesondere das gleichzeitige Auftreten von Augenentzündung und Nierenfunktionsstörung ist ein starker Hinweis auf GPA 3).
Die Wirksamkeit von Biologika wie TNFα-Inhibitoren und Rituximab bei Episkleritis und Skleritis im Zusammenhang mit rheumatoider Arthritis wurde berichtet 1). Infliximab und Adalimumab haben sich bei rheumatoider Arthritis und Uveitis bewährt, und ihre Anwendung wird auch bei refraktärer Skleritis/Episkleritis in Betracht gezogen. Etanercept hingegen ist dafür bekannt, Augenentzündungen paradoxerweise auszulösen oder zu verschlimmern, sodass bei der Arzneimittelauswahl Vorsicht geboten ist 1). Rituximab ist ein monoklonaler Antikörper gegen B-Zellen, dessen Wirksamkeit bei vaskulitisbedingten Augenentzündungen vermutet wird. Die Anwendung dieser Biologika wird in enger Zusammenarbeit mit Rheumatologen und Internisten für Kollagenosen entschieden.
Es wurden Fälle berichtet, bei denen Patienten mit der Diagnose einer Episkleritis tatsächlich einen intraokularen metastatischen Tumor 6) oder eine subkonjunktivale Parasitose 7) aufwiesen. Bei therapierefraktärer oder rezidivierender Episkleritis ist es wichtig, eine maligne Erkrankung oder Infektion auszuschließen. Bildgebende Untersuchungen und die detaillierte Beurteilung der Spaltlampenbefunde der Raumforderung einschließlich der Gefäße liefern diagnostische Hinweise. Es ist erforderlich, die Beweglichkeit der Raumforderung, die Durchsichtigkeit der Skleragefäße, das Vorhandensein oder Fehlen von Verwachsungen mit dem umliegenden Gewebe und das Ansprechen auf die Behandlung gemeinsam zu beurteilen. Eine persistierende erhabene Läsion, die nicht auf standardmäßige Steroid-Augentropfen anspricht, ist eine Grundlage für die Erwägung einer Biopsie oder einer erweiterten Bildgebung.
Langzeitbeobachtungsstudien zum natürlichen Verlauf der Episkleritis und zum Zeitraum bis zum Auftreten einer systemischen Erkrankung sind begrenzt, insbesondere für die japanische Bevölkerung liegen keine ausreichenden Daten zur Inzidenz und zum Profil der Begleiterkrankungen vor. Frühere Berichte aus westlichen Ländern zeigen eine Inzidenz von etwa 40–60 Fällen pro 100.000 Personen pro Jahr, aber die Zahlen variieren aufgrund von Unterschieden in Ethnie, Lebensumfeld und der Führung von Uveitis-Registern. Zukünftige klinische Register und multizentrische Studien sollen die Identifizierung von Risikofaktoren für ein Rezidiv und den Zeitplan für das Auftreten systemischer Erkrankungen ermöglichen.
- Promelle V, Goeb V, Gueudry J. Rheumatoid Arthritis Associated Episcleritis and Scleritis: An Update on Treatment Perspectives. J Clin Med. 2021;10(10):2118.
- Goyal L, Ajmera K, Pandit R. Reoccurring Episcleritis and the Role of Antioxidants. Cureus. 2022;14(4):e24111.
- Foster LD, Nyugen M, Margolin E. Conjunctivitis, episcleritis and anterior uveitis as the first presenting features of granulomatosis with polyangiitis. BMJ Case Rep. 2021;14:e243558.
- Ciotoracu AC, Dimăncescu MG, Mitulescu TC, et al. A clinical case of recurrent episcleritis as the initial manifestation of granulomatosis with polyangiitis. Rom J Ophthalmol. 2021;65(4):386-390.
- Jari M, Nasiri S, Ghandehari M. Episcleritis and posterior uveitis misdiagnosed as orbital cellulitis in a child patient with Behçet’s disease. SAGE Open Med Case Rep. 2023;11:1-4.
- Chong YJ, Azzopardi M, Ng B, et al. Ocular Metastasis as First Presentation of Large-Cell Neuroendocrine Carcinoma. Case Rep Ophthalmol. 2023;14:684-691.
- Redón-Soriano M, Blasco A, Gomila B, et al. Subconjunctival human dirofilariasis by Dirofilaria repens in the Mediterranean Basin. Am J Ophthalmol Case Rep. 2022;26:101570.