視桿細胞優勢型
主要症狀:夜盲、視野狹窄、環狀暗點
代表性抗體:抗恢復蛋白抗體
進展速度:快速(數週至數月)
特徵:急劇重度視力下降。典型表現為旁中心至赤道部暗點。

癌症相關視網膜病變(Cancer Associated Retinopathy; CAR)是一種伴隨惡性腫瘤發生的自體免疫性視網膜變性疾病。它被歸類為副腫瘤症候群的眼部表現之一 1)。
該疾病的概念與自體免疫機制在1970至1980年代被釐清。腫瘤細胞異位表現與視網膜蛋白交叉反應的抗原,產生自體抗體,進而損傷視細胞。
在自體免疫性視網膜病變(Autoimmune Retinopathy; AIR)的分類中,主要分為腫瘤相關型(tumoral AIR)與非腫瘤相關型(non-tumoral AIR; npAIR)。腫瘤相關型包括CAR與黑色素瘤相關視網膜病變(MAR)1)。
最常見的致病腫瘤是小細胞肺癌(SCLC),其次是消化道癌、婦科癌、乳癌、腎癌、胰臟癌和淋巴瘤。發病年齡為40至85歲,性別差異不明顯。Adamus等人的209例系列研究中報告了女性優勢。
ICI相關的眼部免疫相關不良事件已有報導,與CAR/MAR樣視網膜症狀的鑑別可能成為問題3)。
CAR的主觀症狀特徵為亞急性、雙側(常不對稱)無痛性視力下降,在數週至數月內進展。
症狀特徵因致病抗體而異。抗恢復蛋白抗體陽性病例常表現為快速且嚴重的視力下降,多形成旁中心至赤道部暗點。抗烯醇化酶抗體陽性病例傾向於相對緩慢、不對稱的中心視力下降。
以下報告為代表性病例1)。
Bordin等人(2023)病例1:58歲女性。右肺腫瘤肺葉切除術後出現進行性視力下降、視野狹窄和雙眼暗點。最佳矯正視力為20/401)。 病例2:66歲男性。1.5年前因腎腫瘤接受腎切除術,出現進行性無痛性視力下降。右眼20/200,左眼手動。
ICI給藥期間出現快速視力下降時,應同時評估藥物相關眼部炎症、腫瘤相關AIR和轉移性病變3)。
視桿細胞優勢型
主要症狀:夜盲、視野狹窄、環狀暗點
代表性抗體:抗恢復蛋白抗體
進展速度:快速(數週至數月)
特徵:急劇重度視力下降。典型表現為旁中心至赤道部暗點。
視錐細胞優勢型
早期眼底可能幾乎正常,導致診斷困難。
下表顯示依自體抗體分類的主要臨床特徵。
| 自體抗體 | 主要症狀 | 進展速度 |
|---|---|---|
| 抗恢復蛋白 | 急劇重度視力下降 | 快速 |
| 抗烯醇酶 | 不對稱的中心視力下降 | 緩慢 |
腫瘤細胞異位表達正常情況下具有免疫特權的視網膜蛋白,從而產生針對這些蛋白的自體抗體。分子擬態(molecular mimicry)扮演重要角色1)。主要的自體抗體如下。
ICI解除免疫檢查點,可能成為自體免疫性眼部不良事件的背景。出現視網膜症狀時,鑑別藥物相關眼部不良事件和腫瘤相關AIR至關重要3)。
小細胞肺癌最常見,其次為乳癌、消化道癌、婦科癌、腎癌、胰臟癌及淋巴瘤。在MAR中,惡性黑色素瘤是主要致病腫瘤。
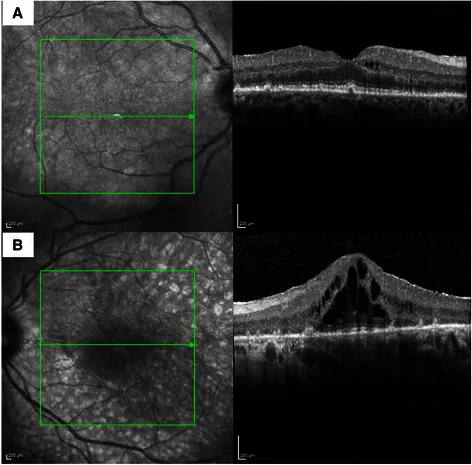
目前尚無明確的診斷標準,需結合臨床表現、電生理檢查、自體抗體檢測及全身癌症篩檢進行綜合診斷。
這是診斷中最重要的一項檢查,對於鑑別CAR和MAR也至關重要。
在一例與APECED(自體免疫性多內分泌腺病-念珠菌病-外胚層發育不良)相關的2歲患兒報告中,視網膜電圖無法記錄,OCT顯示ELM和EZ消失2)。
視網膜自體抗體在健康者和npAIR中也可能呈陽性,因此無法單獨用於確診。抗體效價會波動,建議測量三次以上。
全身癌症檢查包括胸部X光、CT、血液檢查、腹部CT、PET、大腸鏡、乳房及泌尿生殖器評估。50歲以上、眼底表現類似RP且無家族史者,應考慮全身檢查4)。
下表顯示CAR和MAR的主要鑑別點。
| 特徵 | CAR | MAR |
|---|---|---|
| 受損細胞 | 視細胞 | 雙極細胞 |
| 視網膜電圖所見 | a波、b波降低 | 負性視網膜電圖 |
| 原發腫瘤 | 多樣,如肺癌 | 惡性黑色素瘤 |
尚無確立的治療指南。治療目標不是完全恢復,而是功能穩定,主要著眼於抑制病情進展1)。
Bordin等人(2023)的報告中,對於口服類固醇和Tenon囊下類固醇無效且全身免疫抑制劑不耐受的病例,每6個月給予Ozurdex,實現了功能性穩定1)。
Ozurdex通過3-4個月的持續藥物釋放控制局部炎症,並有助於血-視網膜屏障(BRB)的重建。抗恢復蛋白抗體滴度的監測也顯示Ozurdex給藥後抗體滴度下降1)。
抗IL-6受體抗體(托珠單抗、薩瑞魯單抗)已被報導應用於伴有難治性囊樣黃斑水腫的npAIR 1)。
即使對原發腫瘤進行切除、化療或放療,由於體內已循環的自體抗體,視力往往無法改善1)。腫瘤治療作為全身管理進行,但僅靠腫瘤治療難以期待眼病變的改善。
在APECED相關的視網膜病例中,有報導稱即使進行免疫抑制治療,視網膜變性仍持續進展2)。
即使治療原發腫瘤,體內已經產生並循環的自體抗體難以消失,因此視力往往無法恢復1)。腫瘤治療對全身管理不可或缺,但對眼部病變的改善效果有限。治療目標應設定為穩定視功能。
當腫瘤細胞異位表達正常情況下僅在免疫豁免部位(視網膜)表達的蛋白質時,免疫系統會識別這些蛋白質並產生自體抗體。這種分子擬態是視網膜損傷的起點1)。
抗恢復蛋白抗體被認為進入細胞內,破壞鈣恆定並誘導細胞凋亡。在CAR中,桿細胞和錐細胞同時受損4)。
MAR具有不同的機制,涉及針對雙極細胞膜蛋白(TRPM1)的自體抗體。受影響細胞的不同表現為前述視網膜電圖差異(CAR表現為a+b波降低,MAR表現為負性ERG)。
ICIs增強T細胞反應,可能誘發自體免疫性發炎。在眼科領域,已報告了葡萄膜炎、眼內發炎和乾眼症等不良事件3)。
在使用ICI期間出現視網膜症狀時,應根據臨床病程和影像學檢查鑑別藥物相關眼部不良事件、副腫瘤性自體免疫性視網膜病變和腫瘤轉移。
對於全身免疫抑制治療困難的病例,Ozurdex作為局部治療選擇備受關注。Bordin等人(2023)的病例報告顯示,每6個月重複給藥可實現功能穩定,並觀察到抗恢復蛋白抗體滴度下降1)。結合給藥後的自身抗體監測,可能有助於評估治療反應。
隨著ICI的普及,區分藥物相關眼部不良事件與CAR/MAR的需求日益增加3)。早期診斷與適當介入方案的建立是未來的課題。
托珠單抗、薩瑞魯單抗等抗IL-6受體抗體已用於伴有難治性囊樣黃斑水腫的AIR,並正在探討應用於CAR的可能性1)。
在CAR大鼠模型中,鈣通道阻斷劑已被證明有效,作為抗恢復蛋白抗體引起的鈣穩態障礙的干預措施,未來研究值得期待。
在由AIRE基因突變引起的APECED中,已有從幼兒期開始發生自體免疫性視網膜病變的病例報告2)。Sakaguchi等人(2021)的報告顯示,患者在2歲時視網膜電圖已無法記錄,提示早期介入的重要性,但有效的治療方法尚未確立2)。