视杆细胞优势型
主要症状:夜盲、视野狭窄、环形暗点
代表性抗体:抗恢复蛋白抗体
进展速度:快速(数周至数月)
特征:急剧重度视力下降。典型表现为旁中心至赤道部暗点。

癌症相关性视网膜病变(Cancer Associated Retinopathy; CAR)是一种伴随恶性肿瘤发生的自身免疫性视网膜变性疾病。它被视为副肿瘤综合征的眼部表现之一 1)。
该疾病的概念和自身免疫机制在1970至1980年代被阐明。肿瘤细胞异位表达与视网膜蛋白交叉反应的抗原,产生自身抗体,从而损伤视细胞。
在自身免疫性视网膜病变(Autoimmune Retinopathy; AIR)的分类中,主要分为肿瘤相关型(tumoral AIR)和非肿瘤相关型(non-tumoral AIR; npAIR)。肿瘤相关型包括CAR和黑色素瘤相关性视网膜病变(MAR)1)。
最常见的原发肿瘤是小细胞肺癌(SCLC),其次是消化道癌、妇科癌、乳腺癌、肾癌、胰腺癌和淋巴瘤。发病年龄为40至85岁,性别差异不明显。Adamus等人的209例系列研究中报告了女性优势。
ICI相关的眼部免疫相关不良事件已有报道,与CAR/MAR样视网膜症状的鉴别可能存在问题3)。
CAR的主观症状特征为亚急性、双侧(常不对称)无痛性视力下降,在数周至数月内进展。
症状特征因致病抗体而异。抗恢复蛋白抗体阳性病例常表现为快速且严重的视力下降,多形成旁中心至赤道部暗点。抗烯醇化酶抗体阳性病例倾向于相对缓慢、不对称的中心视力下降。
以下报告为代表性病例1)。
Bordin等人(2023)病例1:58岁女性。右肺肿瘤肺叶切除术后出现进行性视力下降、视野狭窄和双眼暗点。最佳矫正视力为20/401)。 病例2:66岁男性。1.5年前因肾肿瘤接受肾切除术,出现进行性无痛性视力下降。右眼20/200,左眼手动。
ICI给药期间出现快速视力下降时,应同时评估药物相关眼部炎症、肿瘤相关AIR和转移性病变3)。
视杆细胞优势型
主要症状:夜盲、视野狭窄、环形暗点
代表性抗体:抗恢复蛋白抗体
进展速度:快速(数周至数月)
特征:急剧重度视力下降。典型表现为旁中心至赤道部暗点。
视锥细胞优势型
早期眼底可能几乎正常,导致诊断困难。
下表显示了按自身抗体分类的主要临床特征。
| 自身抗体 | 主要症状 | 进展速度 |
|---|---|---|
| 抗恢复蛋白 | 急剧重度视力下降 | 快速 |
| 抗烯醇化酶 | 不对称的中心视力下降 | 缓慢 |
肿瘤细胞异位表达正常情况下具有免疫豁免权的视网膜蛋白,从而产生针对这些蛋白的自身抗体。分子模拟(molecular mimicry)起重要作用1)。主要的自身抗体如下。
ICI解除免疫检查点,可能成为自身免疫性眼部不良事件的背景。出现视网膜症状时,鉴别药物相关眼部不良事件和肿瘤相关AIR至关重要3)。
小细胞肺癌最常见,其次是乳腺癌、消化道癌、妇科癌、肾癌、胰腺癌和淋巴瘤。在MAR中,恶性黑色素瘤是主要致病肿瘤。
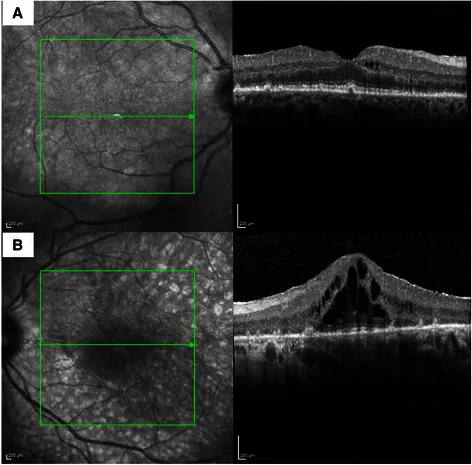
目前尚无明确的诊断标准,需结合临床表现、电生理检查、自身抗体检测及全身癌症筛查进行综合诊断。
这是诊断中最重要的检查,对于鉴别CAR和MAR也至关重要。
在一例与APECED(自身免疫性多内分泌腺病-念珠菌病-外胚层发育不良)相关的2岁患儿报告中,视网膜电图无法记录,OCT显示ELM和EZ消失2)。
视网膜自身抗体在健康人和npAIR中也可能呈阳性,因此不能单独用于确诊。抗体滴度会波动,建议测量三次以上。
作为全身癌症检查,考虑胸部X线、CT、血液检查、腹部CT、PET、结肠镜、乳房及泌尿生殖器评估。对于50岁以上、眼底表现类似RP且无家族史的患者,应进行全身检查4)。
下表显示CAR和MAR的主要鉴别点。
| 特征 | CAR | MAR |
|---|---|---|
| 受损细胞 | 视细胞 | 双极细胞 |
| 视网膜电图所见 | a波、b波降低 | 负性视网膜电图 |
| 原发肿瘤 | 多种,如肺癌 | 恶性黑色素瘤 |
尚无确定的治疗指南。治疗目标不是完全恢复,而是功能稳定,主要着眼于抑制病情进展1)。
Bordin等人(2023)的报告中,对于口服类固醇和Tenon囊下类固醇无效且全身免疫抑制剂不耐受的病例,每6个月给予Ozurdex,实现了功能性稳定1)。
Ozurdex通过3-4个月的持续药物释放控制局部炎症,并有助于血-视网膜屏障(BRB)的重建。抗恢复蛋白抗体滴度的监测也显示Ozurdex给药后抗体滴度下降1)。
抗IL-6受体抗体(托珠单抗、萨瑞鲁单抗)已被报道用于伴有难治性囊样黄斑水肿的npAIR 1)。
即使对原发肿瘤进行切除、化疗或放疗,由于体内已循环的自身抗体,视力往往无法改善1)。肿瘤治疗作为全身管理进行,但仅靠肿瘤治疗难以期待眼病变的改善。
在APECED相关的视网膜病例中,有报道称即使进行免疫抑制治疗,视网膜变性仍继续进展2)。
即使治疗原发肿瘤,体内已经产生并循环的自身抗体也难以消失,因此视力往往无法恢复1)。肿瘤治疗对于全身管理不可或缺,但对眼部病变的改善效果有限。治疗目标应设定为稳定视功能。
当肿瘤细胞异位表达正常情况下仅在免疫豁免部位(视网膜)表达的蛋白质时,免疫系统会识别这些蛋白质并产生自身抗体。这种分子模拟是视网膜损伤的起点1)。
抗恢复蛋白抗体被认为进入细胞内,破坏钙稳态并诱导凋亡。在CAR中,杆细胞和锥细胞同时受损4)。
MAR具有不同的机制,涉及针对双极细胞膜蛋白(TRPM1)的自身抗体。受累细胞的不同表现为前述视网膜电图差异(CAR表现为a+b波降低,MAR表现为负性ERG)。
ICIs增强T细胞反应,可能诱发自身免疫性炎症。在眼科领域,已报告了葡萄膜炎、眼内炎症和干眼症等不良事件3)。
在使用ICI期间出现视网膜症状时,应根据临床病程和影像学检查鉴别药物相关眼部不良事件、副肿瘤性自身免疫性视网膜病变和肿瘤转移。
对于全身免疫抑制治疗困难的病例,Ozurdex作为局部治疗选择备受关注。Bordin等人(2023)的病例报告显示,每6个月重复给药可实现功能稳定,并观察到抗恢复蛋白抗体滴度下降1)。结合给药后的自身抗体监测,可能有助于评估治疗反应。
随着ICI的普及,将药物相关眼部不良事件与CAR/MAR进行鉴别处理的需求日益增加3)。早期诊断和适当干预方案的制定是未来的课题。
托珠单抗、萨瑞鲁单抗等抗IL-6受体抗体已用于伴有难治性囊样黄斑水肿的AIR,并正在探讨应用于CAR的可能性1)。
在CAR大鼠模型中,钙通道阻滞剂已被证明有效,作为抗恢复蛋白抗体引起的钙稳态障碍的干预措施,未来研究值得期待。
在由AIRE基因突变引起的APECED中,已有从幼儿期开始发生自身免疫性视网膜病变的病例报道2)。Sakaguchi等人(2021)的报告显示,患者在2岁时视网膜电图已无法记录,提示早期干预的重要性,但有效的治疗方法尚未确立2)。