간체 우세형

암 관련 망막병증
한눈에 보는 포인트
섹션 제목: “한눈에 보는 포인트”1. 암 관련 망막병증
섹션 제목: “1. 암 관련 망막병증”암 관련 망막병증(Cancer Associated Retinopathy; CAR)은 악성 종양에 동반되어 발생하는 자가면역성 망막 변성 질환입니다. 이는 종양 관련 증후군(paraneoplastic syndrome)의 안과적 표현형 중 하나로 분류됩니다 1).
1970~1980년대에 질환 개념과 자가면역 기전이 정립되었습니다. 종양 세포가 망막 단백질과 교차 반응하는 항원을 이소 발현하고, 이에 대한 자가항체가 생성되어 시세포를 손상시킵니다.
자가면역성 망막병증(Autoimmune Retinopathy; AIR)의 분류에서는 종양 관련형(tumoral AIR)과 비종양 관련형(non-tumoral AIR; npAIR)으로 크게 나뉩니다. 종양 관련형에는 CAR과 흑색종 관련 망막병증(MAR)이 포함됩니다 1).
가장 흔한 원인 종양은 소세포폐암(SCLC)이며, 다음으로 소화기암, 부인과암, 유방암, 신장암, 췌장암, 림프종이 있습니다. 발병 연령은 40~85세이며, 성별 차이는 명확하지 않습니다. Adamus 등의 209례 시리즈에서는 여성 우위가 보고되었습니다.
ICI와 관련된 안구 면역 관련 이상 반응이 보고되었으며, CAR/MAR 유사 망막 증상과의 감별이 문제가 될 수 있습니다3).
많은 증례에서 안구 증상이 암 진단에 선행합니다. 비교적 드문 질환이지만, 안과적 진단이 전신 암 발견으로 이어질 수 있습니다. 50세 이상에서 망막색소변성(RP)과 유사한 안저 소견이 있고 가족력이 없는 경우, CAR을 의심하고 전신 검색을 고려합니다4).
2. 주요 증상 및 임상 소견
섹션 제목: “2. 주요 증상 및 임상 소견”자각 증상
섹션 제목: “자각 증상”CAR의 자각 증상은 아급성, 양측성(종종 비대칭)의 무통성 시력 저하가 특징이며, 수주에서 수개월에 걸쳐 진행됩니다.
- 광시증 및 눈부심: 이러한 증상은 초기에 나타나기 쉽습니다.
- 야맹 및 시야 협착: 간상세포 우세형에서는 환상 암점과 시야 협착이 주를 이룹니다.
- 중심 암점 및 색각 이상: 원추세포 우세형에서는 눈부심, 중심 암점, 색각 장애가 두드러집니다.
원인 항체에 따라 증상의 특징이 다릅니다. 항리커버린 항체 양성 예에서는 급속하고 심각한 시력 저하를 보이며, 중심와 주변에서 적도부까지의 암점을 형성하는 경우가 많습니다. 항에놀라제 항체 양성 예에서는 비교적 완만하고 비대칭적인 중심 시력 저하를 보이는 경향이 있습니다.
대표적인 증례로 다음과 같은 보고가 있습니다1).
Bordin 등(2023) 증례 1: 58세 여성. 우측 폐종양의 엽절제술 후 진행성 시력 저하, 시야 협착, 양안 암점을 호소함. 최대교정시력은 20/401). 증례 2: 66세 남성. 1.5년 전 신장 종양으로 신절제술을 받은 과거력이 있으며, 진행성 무통성 시력 저하를 보임. 우안 20/200, 좌안 안전수동.
ICI 투여 중 급속한 시력 저하 시, 약물 관련 안구 염증, 종양 관련 AIR, 전이성 병변을 동시에 평가해야 함3).
원추세포 우세형
임상 소견
섹션 제목: “임상 소견”초기에는 안저 소견이 거의 정상으로 보일 수 있어 진단이 어렵다.
- 안저 소견(진행기): RPE 얇아짐, 색소반, 세동맥 협착, 시신경 유두 창백. 경미한 유리체 세포 침윤 또는 혈관염을 동반할 수 있다.
- OCT: 외층(타원체대 EZ, 광수용체층) 소실, 낭포성 변화.
- 망막전위도: 거의 모든 예에서 이상을 보이며, 간체와 원추체계 모두 감소한다. 진단에 필수적인 검사이다.
- FAF(안저 자가형광): 특징적인 중심와 주변 고형광 고리, APECED 관련 증례에서도 확인됨2).
다음 표는 자가항체별 주요 임상 특징을 보여줍니다.
| 자가항체 | 주요 증상 | 진행 속도 |
|---|---|---|
| 항리커버린 | 급성 중증 시력 저하 | 빠름 |
| 항에놀라제 | 비대칭적인 중심 시력 저하 | 완만 |
3. 원인 및 위험 요인
섹션 제목: “3. 원인 및 위험 요인”발병 기전 개요
섹션 제목: “발병 기전 개요”종양 세포가 정상적으로 면역 특권을 가진 망막 단백질을 이소성 발현하여 이에 대한 자가항체가 생성됩니다. 분자 모방(molecular mimicry)이 중요한 역할을 합니다1). 주요 자가항체는 다음과 같습니다.
- 항리커버린 항체: 대표적인 CAR 관련 항체입니다. 악성 종양 없이도 양성일 수 있습니다 2, 4).
- 항α-에놀라제 항체: 비교적 흔합니다.
- 기타: 항탄산탈수효소II(CAII), 항트랜스듀신β, 항TULP1, 항아레스틴, 항GAPDH 등 많은 자가항체가 보고되었습니다.
ICI(면역관문억제제)로 인한 CAR/MAR
섹션 제목: “ICI(면역관문억제제)로 인한 CAR/MAR”ICI는 면역관문을 해제하여 자가면역성 안구 이상반응의 배경이 됩니다. 망막 증상이 나타나는 경우 약물 관련 안구 이상반응과 종양 관련 AIR의 감별이 중요합니다 3).
원인이 되는 악성 종양
섹션 제목: “원인이 되는 악성 종양”소세포폐암이 가장 흔하며, 유방암, 소화기암, 부인과암, 신장암, 췌장암, 림프종이 그 뒤를 잇습니다. MAR의 경우 악성 흑색종이 주요 원인 종양입니다.
4. 진단 및 검사 방법
섹션 제목: “4. 진단 및 검사 방법”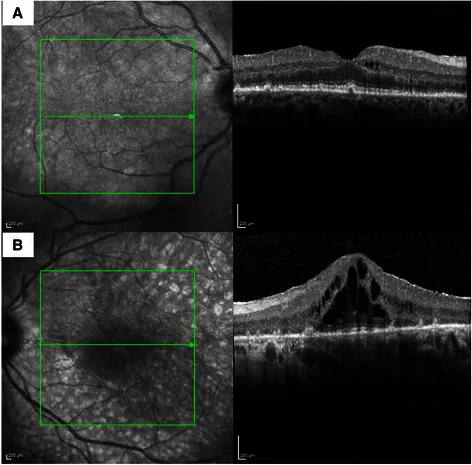
확립된 진단 기준은 없으며, 임상 소견, 전기생리학적 검사, 자가항체 검사, 전신 암 선별검사를 조합하여 진단합니다.
전기생리학적 검사(ERG)
섹션 제목: “전기생리학적 검사(ERG)”진단에 가장 중요한 검사입니다. CAR과 MAR의 감별에도 필수적입니다.
- CAR: 암순응(간상체계)과 명순응(원추체계) 모두에서 a파와 b파가 감소합니다.
- MAR: 음성 망막전위도(a파는 정상 또는 거의 정상이나 b파가 현저히 감소)가 특징적이며, 양극세포 손상을 반영합니다.
APECED(자가면역 다내분비병증-칸디다증-외배엽 형성이상)와 관련된 2세 아동의 보고에서 망막전위도가 기록 불가능하였고, OCT에서 ELM과 EZ의 소실이 확인되었습니다2).
자가항체 검사
섹션 제목: “자가항체 검사”망막 자가항체는 건강한 사람이나 npAIR에서도 양성으로 나올 수 있어 단독으로 확진할 수 없습니다. 항체가는 변동하므로 3회 이상 측정이 권장됩니다.
영상 검사
섹션 제목: “영상 검사”- OCT: 외층 소실(EZ 및 시세포층) 확인에 유용1, 2).
- FAF: 중심와 주변 고형광 고리가 특징적2).
- ICI 사용 중 평가: 안내 염증, 약물 관련 안구 이상반응, 종양 관련 AIR를 동시에 감별3).
암 검진
섹션 제목: “암 검진”전신 암 검사로 흉부 X선, CT, 혈액 검사, 복부 CT, PET, 대장 내시경, 유방 및 비뇨생식기 평가를 고려합니다. 50세 이상이고 RP와 유사한 안저 소견이 있으며 가족력이 없는 경우 전신 검사를 염두에 두어야 합니다4).
다음 표는 CAR과 MAR의 주요 감별점을 보여줍니다.
| 특징 | CAR | MAR |
|---|---|---|
| 손상된 세포 | 시세포 | 양극 세포 |
| 망막전도 소견 | a파·b파 저하 | 음성 망막전도 |
| 원인 종양 | 다양함, 예: 폐암 | 악성 흑색종 |
망막전도도 소견이 가장 중요한 감별점입니다. CAR에서는 간상체와 원추체 모두에서 a파와 b파가 감소하는 반면, MAR에서는 음성 망막전도도(a파 정상, b파 현저히 감소)를 보입니다. 또한 MAR에서는 악성 흑색종이 원인 종양인 경우가 많고, CAR에서는 소세포 폐암 등이 많습니다. 손상되는 세포도 CAR는 시세포, MAR는 양극세포로 다릅니다.
5. 표준 치료법
섹션 제목: “5. 표준 치료법”확립된 치료 지침은 없습니다. 치료 목표는 완전 회복이 아닌 기능 안정화이며, 진행을 억제하는 데 중점을 둡니다1).
전신 면역억제 요법
섹션 제목: “전신 면역억제 요법”- 전신 스테로이드: 호전 사례 보고가 있으나, 암 면역을 억제할 위험이 있어 신중히 투여해야 합니다.
- 면역억제제: 사이클로스포린, 아자티오프린, 알렘투주맙 등이 사용됩니다.
- 리툭시맙(항CD20 항체): AIR 16예(CAR 6예 포함)를 대상으로 한 보고에서 병용 요법으로 77%의 눈이 안정~호전을 보였습니다.
- IVIG(정맥 면역글로불린): 자가항체 중화를 기대하여 사용됩니다. 일정한 효과 보고가 있습니다.
- 혈장 교환: 자가항체 제거를 목적으로 시행됩니다.
국소 요법: 덱사메타손 유리체강내 임플란트(Ozurdex)
섹션 제목: “국소 요법: 덱사메타손 유리체강내 임플란트(Ozurdex)”Bordin 등(2023)의 보고에 따르면, 경구 스테로이드 및 테논낭하 스테로이드가 효과가 없고 전신 면역억제제를 견딜 수 없었던 증례에 대해 Ozurdex를 6개월마다 투여한 결과 기능적 안정화가 얻어졌습니다1).
Ozurdex는 3~4개월에 걸친 지속적인 약물 방출로 국소 염증을 조절하고 혈액-망막 장벽(BRB) 재구성에 기여하는 것으로 생각됩니다. 항리커버린 항체가 모니터링에서도 Ozurdex 투여 후 항체가 감소가 확인되었습니다1).
항IL-6 수용체 항체(토실리주맙, 사릴루맙)는 난치성 낭포황반부종을 동반한 npAIR에 적용된 보고가 있습니다1).
종양 치료
섹션 제목: “종양 치료”원발 종양의 절제, 화학요법, 방사선 치료를 시행하더라도 이미 체내에 순환하는 자가항체로 인해 시력 개선이 이루어지지 않는 경우가 많습니다1). 종양 치료는 전신 관리로 시행하지만, 이만으로 안구 병변의 호전을 기대하기는 어렵습니다.
APECED 관련 망막 증례에서는 면역억제 요법을 시행해도 망막 변성의 진행이 멈추지 않았다는 보고가 있습니다2).
원발 종양을 치료해도 이미 체내에서 생성되어 순환하는 자가항체는 사라지기 어렵기 때문에 시력 회복이 이루어지지 않는 경우가 많습니다1). 종양 치료는 전신 관리로서 필수적이지만, 안구 병변에 대한 개선 효과는 제한적입니다. 치료 목표는 시 기능의 안정화에 두어야 합니다.
6. 병태생리학 및 상세 발병 기전
섹션 제목: “6. 병태생리학 및 상세 발병 기전”종양 항원에 의한 자가면역 유도
섹션 제목: “종양 항원에 의한 자가면역 유도”종양 세포가 정상적으로는 면역 특권 부위(망막)에서만 발현되는 단백질을 이소성 발현하면, 면역계가 이를 인식하여 자가항체를 생성합니다. 이러한 분자 모방이 망막 손상의 시작점이 됩니다1).
항리커버린 항체는 세포 내로 침투하여 칼슘 항상성을 손상시키고 세포자멸사를 유도하는 것으로 생각됩니다. CAR에서는 간상체와 원추체 시세포가 동시에 손상됩니다4).
MAR은 다른 기전을 가지며, 양극 세포 막 단백질(TRPM1)에 대한 자가항체가 관여합니다. 손상된 세포의 차이가 앞서 언급한 망막전위도 소견의 차이(CAR은 a+b파 감소, MAR은 음성 ERG)로 나타납니다.
ICI에 의한 자가면역 망막병증의 기전
섹션 제목: “ICI에 의한 자가면역 망막병증의 기전”ICI는 T세포 반응을 강화하여 자가면역 염증을 유발할 수 있습니다. 안과 영역에서는 포도막염, 안구 염증, 안구건조증 등의 이상 반응이 보고되었습니다3).
ICI 사용 중 망막 증상이 나타나면 약물 관련 안구 이상 반응, 종양 관련 자가면역 망막병증, 종양 전이를 임상 경과와 영상 검사로 감별합니다.
7. 최신 연구 및 향후 전망 (연구 단계 보고)
섹션 제목: “7. 최신 연구 및 향후 전망 (연구 단계 보고)”덱사메타손 유리체강내 임플란트(Ozurdex)의 국소 치료로서 가능성
섹션 제목: “덱사메타손 유리체강내 임플란트(Ozurdex)의 국소 치료로서 가능성”전신 면역억제 치료가 어려운 증례에 대한 국소 치료 옵션으로 Ozurdex가 주목받고 있습니다. Bordin 등(2023)의 증례 보고에서는 6개월마다 반복 투여로 기능 안정화가 이루어졌고, 항리커버린 항체 역가 감소도 확인되었습니다1). 투여 후 자가항체 모니터링을 병행하면 치료 반응 평가가 가능할 수 있습니다.
ICI 관련 CAR/MAR의 증가와 관리
섹션 제목: “ICI 관련 CAR/MAR의 증가와 관리”ICI의 보급에 따라 약물 관련 안구 이상반응을 CAR/MAR과 감별하여 다루어야 할 필요성이 증가하고 있습니다3). 조기 진단과 적절한 중재 프로토콜의 정비가 향후 과제입니다.
항IL-6 수용체 항체 요법
섹션 제목: “항IL-6 수용체 항체 요법”토실리주맙, 사릴루맙 등의 항IL-6 수용체 항체가 난치성 낭포황반부종을 동반한 AIR에 사용되고 있으며, CAR에의 응용도 검토되고 있습니다1).
칼슘 채널 차단제
섹션 제목: “칼슘 채널 차단제”CAR 랫드 모델에서 칼슘 채널 차단제가 효과적임이 입증되었으며, 항리커버린 항체에 의한 칼슘 항상성 장애에 대한 중재로서 향후 연구가 기대됩니다.
APECED 관련 망막병증
섹션 제목: “APECED 관련 망막병증”AIRE 유전자 돌연변이로 인한 APECED에서는 유아기부터 자가면역 망막병증이 발생하는 사례가 보고되었습니다2). Sakaguchi 등(2021)의 보고에 따르면 2세 때 망막전위도가 기록 불가능해져 조기 개입의 중요성이 시사되지만, 효과적인 치료법은 아직 확립되지 않았습니다2).
8. 참고문헌
섹션 제목: “8. 참고문헌”- Bordin FL, et al. Intravitreal Dexamethasone Implant in Autoimmune Retinopathy. Case Rep Ophthalmol Med. 2023;2023:5670538.
- Sakaguchi H, Mizuochi T, Haruta M, Takase R, Yoshida S, Yamashita Y, Nishikomori R. AIRE gene mutation presenting at age 2 years with autoimmune retinopathy and steroid-responsive acute liver failure: a case report and literature review. Front Immunol. 2021;12:687280. doi:10.3389/fimmu.2021.687280.
- Fang T, Maberley DA, Etminan M. Ocular adverse events with immune checkpoint inhibitors. J Curr Ophthalmol. 2019;31(3):319-322. doi:10.1016/j.joco.2019.05.002.
- Singh D, Tripathy K. Cancer-Associated Retinopathy. In: StatPearls. Treasure Island (FL): StatPearls Publishing; 2024.
