نوع غالب میلهای
علائم اصلی: شبکوری، تنگ شدن میدان بینایی، اسکوتوم حلقوی
آنتیبادی نماینده: آنتیبادی ضد ریکاورین
سرعت پیشرفت: سریع (چند هفته تا چند ماه)
ویژگی: کاهش شدید و ناگهانی بینایی. اسکوتوم مرکزی تا ناحیه استوایی معمول است.

رتینوپاتی مرتبط با سرطان (CAR) یک بیماری دژنراتیو خودایمنی شبکیه است که به دنبال تومور بدخیم ایجاد میشود. این بیماری به عنوان یکی از تظاهرات چشمی سندرم پارانئوپلاستیک در نظر گرفته میشود1).
مفهوم بیماری و مکانیسم خودایمنی آن در دهههای ۱۹۷۰ تا ۱۹۸۰ تبیین شد. سلولهای توموری آنتیژنهایی را بیان میکنند که با پروتئینهای شبکیه واکنش متقاطع دارند و در نتیجه آنتیبادیهای خودی تولید میشوند که به سلولهای بینایی آسیب میرسانند.
در طبقهبندی رتینوپاتی خودایمنی (AIR)، دو نوع مرتبط با تومور (tumoral AIR) و غیرمرتبط با تومور (non-tumoral AIR; npAIR) وجود دارد. نوع مرتبط با تومور شامل CAR و رتینوپاتی مرتبط با ملانوم (MAR) است 1).
شایعترین تومور زمینهای، سرطان ریه سلول کوچک (SCLC) است و پس از آن سرطانهای دستگاه گوارش، زنان، پستان، کلیه، پانکراس و لنفوم قرار دارند. سن شروع ۴۰ تا ۸۵ سال است و تفاوت جنسیتی مشخصی ندارد. در سری ۲۰۹ موردی Adamus، غلبه زنان گزارش شده است.
عوارض جانبی ایمنی مرتبط با چشم ناشی از ICI گزارش شده است و تشخیص افتراقی آن از علائم شبکیهای شبیه CAR/MAR ممکن است مشکل باشد 3).
در بسیاری از موارد، علائم چشمی پیش از تشخیص سرطان ظاهر میشوند. اگرچه این بیماری نسبتاً نادر است، اما تشخیص چشمی میتواند منجر به کشف سرطان در سراسر بدن شود. در افراد بالای ۵۰ سال که یافتههای فوندوس مشابه رتینیت پیگمانتوزا (RP) دارند و سابقه خانوادگی ندارند، باید به CAR مشکوک شد و بررسی سیستمیک را در نظر گرفت4).
علائم ذهنی CAR با کاهش بینایی بدون درد، تحتحاد و دوطرفه (اغلب نامتقارن) مشخص میشود. این کاهش بینایی طی چند هفته تا چند ماه پیشرفت میکند.
ویژگیهای علائم بسته به آنتیبادی عامل متفاوت است. در موارد مثبت آنتیبادی ضد ریکاورین، کاهش سریع و شدید بینایی و اغلب تشکیل اسکوتومهای پارامرکزی تا ناحیه استوایی دیده میشود. در موارد مثبت آنتیبادی ضد انولاز، تمایل به کاهش تدریجی و نامتقارن بینایی مرکزی وجود دارد.
به عنوان موارد بالینی نماینده، گزارشهای زیر وجود دارد1).
مورد ۱ از Bordin و همکاران (۲۰۲۳): زن ۵۸ ساله. پس از لوبکتومی تومور ریه راست، از کاهش پیشرونده بینایی و تنگ شدن میدان بینایی و اسکوتوم دوطرفه شکایت داشت. بهترین دید اصلاحشده ۲۰/۴۰ بود1). مورد ۲: مرد ۶۶ ساله. سابقه نفرکتومی به دلیل تومور کلیه ۱.۵ سال قبل، با کاهش پیشرونده و بدون درد بینایی مراجعه کرد. چشم راست ۲۰/۲۰۰، چشم چپ حرکت دست.
در کاهش سریع بینایی حین مصرف ICI، باید التهاب چشمی مرتبط با دارو، AIR مرتبط با تومور و ضایعات متاستاتیک به طور همزمان ارزیابی شوند3).
نوع غالب میلهای
علائم اصلی: شبکوری، تنگ شدن میدان بینایی، اسکوتوم حلقوی
آنتیبادی نماینده: آنتیبادی ضد ریکاورین
سرعت پیشرفت: سریع (چند هفته تا چند ماه)
ویژگی: کاهش شدید و ناگهانی بینایی. اسکوتوم مرکزی تا ناحیه استوایی معمول است.
نوع غالب مخروطی
علائم اصلی: فوتوفوبی، اسکوتوم مرکزی، دیسکروماتوپسی
آنتیبادی نماینده: آنتیبادی ضد انولاز
سرعت پیشرفت: نسبتاً آهسته و نامتقارن
ویژگی: دید مرکزی زودتر مختل میشود.
در مراحل اولیه، یافتههای فوندوس ممکن است تقریباً طبیعی به نظر برسند که تشخیص را دشوار میکند.
جدول زیر ویژگیهای بالینی اصلی را بر اساس نوع آنتیبادی خودایمنی نشان میدهد.
| آنتیبادی خودایمنی | علائم اصلی | سرعت پیشرفت |
|---|---|---|
| ضد ریکاورین | کاهش شدید و ناگهانی بینایی | سریع |
| ضد انولاز | کاهش نامتقارن بینایی مرکزی | آهسته |
سلولهای توموری پروتئینهای شبکیه را که به طور طبیعی دارای مصونیت ایمنی هستند، به صورت نابجا بیان میکنند و آنتیبادیهای خودی علیه آنها تولید میشود. تقلید مولکولی نقش مهمی ایفا میکند1). آنتیبادیهای خودی اصلی به شرح زیر هستند.
ICIها با برداشتن ایست بازرسی ایمنی، زمینهساز عوارض چشمی خودایمنی میشوند. در صورت بروز علائم شبکیه، افتراق بین عوارض چشمی مرتبط با دارو و AIR مرتبط با تومور اهمیت دارد3).
شایعترین علت، سرطان سلول کوچک ریه است و پس از آن سرطان پستان، سرطان دستگاه گوارش، سرطان زنان، سرطان کلیه، سرطان پانکراس و لنفوم قرار دارند. در MAR، ملانوم بدخیم تومور اصلی ایجادکننده است.
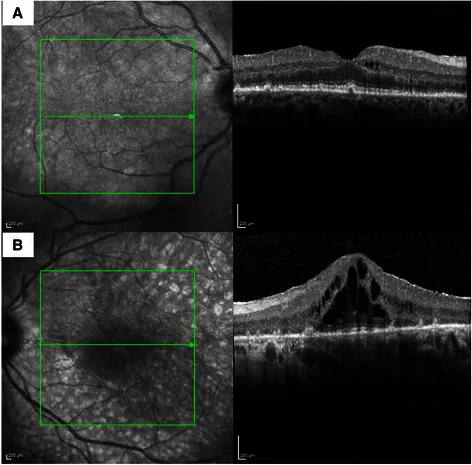
معیار تشخیصی قطعی وجود ندارد و تشخیص با ترکیبی از یافتههای بالینی، آزمایشهای الکتروفیزیولوژیک، آزمایش آنتیبادی و غربالگری سرطان در سراسر بدن انجام میشود.
این مهمترین آزمایش برای تشخیص است. همچنین برای افتراق CAR و MAR ضروری است.
در گزارش یک کودک ۲ ساله مبتلا به APECED (پلیاندوکرینوپاتی خودایمنی-کاندیدیاز-اکتودرمال دیسپلازی)، الکترورتینوگرام غیرقابل ثبت بود و OCT ناپدید شدن ELM و EZ را تأیید کرد2).
آنتیبادیهای خودایمنی شبکیه ممکن است در افراد سالم و npAIR نیز مثبت شوند و به تنهایی برای تشخیص قطعی کافی نیستند. از آنجایی که تیتر آنتیبادی متغیر است، اندازهگیری حداقل سه بار توصیه میشود.
برای بررسی سرطان در سراسر بدن، رادیوگرافی قفسه سینه، سیتی اسکن، آزمایش خون، سیتی اسکن شکم، پت اسکن، کولونوسکوپی، و ارزیابی پستان و دستگاه ادراری-تناسلی در نظر گرفته میشود. در افراد بالای ۵۰ سال با یافتههای فوندوس مشابه رتینوپاتی پارانئوپلاستیک (RP) و بدون سابقه خانوادگی، باید جستجوی سیستمیک مد نظر قرار گیرد4).
جدول زیر تفاوتهای اصلی بین کارسینوم مرتبط با رتینوپاتی (CAR) و ملانوم مرتبط با رتینوپاتی (MAR) را نشان میدهد.
| ویژگی | CAR | MAR |
|---|---|---|
| سلولهای آسیبدیده | سلولهای بینایی | سلولهای دوقطبی |
| یافتههای الکترورتینوگرافی | کاهش امواج a و b | الکترورتینوگرافی منفی |
| تومور زمینهای | متنوع مانند سرطان ریه | ملانوم بدخیم |
تنها مثبت بودن آنتیبادیهای خودایمنی شبکیه برای تشخیص قطعی CAR کافی نیست. زیرا ممکن است در افراد سالم و npAIR نیز مثبت شود و تیتر آنتیبادی نیز تغییر میکند. برای تشخیص باید یافتههای الکتروفیزیولوژیک و مورفولوژیک مانند الکترورتینوگرافی، OCT و FAF و همچنین وجود یا عدم وجود تومور بدخیم سیستمیک به طور جامع ارزیابی شود.
یافتههای الکترورتینوگرافی مهمترین نکته افتراقی است. در CAR، امواج a و b هر دو در سیستم میلهای و مخروطی کاهش مییابند، در حالی که در MAR الکترورتینوگرافی منفی (موج a طبیعی و موج b به شدت کاهش یافته) دیده میشود. همچنین، در MAR تومور عامل اغلب ملانوم بدخیم است، در حالی که در CAR سرطان سلول کوچک ریه شایعتر است. سلولهای درگیر نیز متفاوت هستند: در CAR سلولهای گیرنده نور و در MAR سلولهای دوقطبی آسیب میبینند.
راهنمای درمانی استانداردی وجود ندارد. هدف درمان، بهبودی کامل نیست، بلکه تثبیت عملکرد و جلوگیری از پیشرفت بیماری است1).
در گزارش Bordin و همکاران (2023)، در مواردی که استروئید خوراکی و استروئید زیر تانون بیاثر بوده و داروهای سرکوبکننده سیستم ایمنی قابل تحمل نبودهاند، تزریق Ozurdex هر شش ماه منجر به تثبیت عملکردی شده است1).
تصور میشود Ozurdex با آزادسازی پایدار دارو به مدت ۳ تا ۴ ماه، التهاب موضعی را کنترل کرده و به بازسازی سد خونی-شبکیه (BRB) کمک میکند. در پایش تیتر آنتیبادی ضد ریکاورین نیز کاهش تیتر پس از تزریق Ozurdex تأیید شده است1).
استفاده از آنتیبادی ضد گیرنده IL-6 (توسیلیزوماب و ساریلوماب) در npAIR مقاوم همراه با ادم ماکولار کیستیک گزارش شده است1).
حتی پس از برداشتن تومور اولیه، شیمیدرمانی و پرتودرمانی، به دلیل وجود آنتیبادیهای خودایمنی که قبلاً در بدن در گردش هستند، اغلب بهبودی در بینایی حاصل نمیشود1). درمان تومور به عنوان مدیریت سیستمیک انجام میشود، اما انتظار بهبود ضایعات چشمی تنها با آن دشوار است.
در موارد رتینوپاتی مرتبط با APECED گزارش شده است که حتی با درمان سرکوبکننده ایمنی، پیشرفت دژنراسیون شبکیه متوقف نشده است2).
حتی با درمان تومور اولیه، آنتیبادیهای خودی که قبلاً در بدن تولید و در گردش هستند به راحتی از بین نمیروند، بنابراین اغلب بهبود بینایی حاصل نمیشود1). درمان تومور برای مدیریت سیستمیک ضروری است، اما اثر بهبودی بر ضایعات چشمی محدود است. هدف درمان باید بر تثبیت عملکرد بینایی متمرکز شود.
هنگامی که سلولهای توموری پروتئینهایی را که به طور طبیعی فقط در محلهای دارای امتیاز ایمنی (شبکیه) بیان میشوند، به صورت نابجا بیان میکنند، سیستم ایمنی آنها را شناسایی کرده و آنتیبادیهای خودی تولید میکند. این تقلید مولکولی نقطه شروع آسیب شبکیه است1).
تصور میشود آنتیبادی ضد ریکاورین وارد سلول شده، هموستاز کلسیم را مختل کرده و آپوپتوز را القا میکند. در CAR، هر دو سلول گیرنده نوری استوانهای و مخروطی به طور همزمان آسیب میبینند4).
MAR مکانیسمهای متفاوتی دارد و شامل آنتیبادیهای خودایمن علیه پروتئین غشایی سلولهای دوقطبی (TRPM1) است. تفاوت در سلولهای آسیبدیده به صورت تفاوت در یافتههای الکترورتینوگرافی ذکر شده (کاهش امواج a+b در CAR و ERG منفی در MAR) ظاهر میشود.
ICI پاسخ سلولهای T را تقویت کرده و میتواند التهاب خودایمنی را القا کند. در حوزه چشم، عوارض جانبی مانند یووئیت، التهاب چشم و خشکی چشم گزارش شده است3).
در صورت مشاهده علائم شبکیه در حین استفاده از ICI، باید عوارض چشمی مرتبط با دارو، رتینوپاتی خودایمن پارانئوپلاستیک و متاستاز تومور با توجه به سیر بالینی و تصویربرداری افتراق داده شوند.
Ozurdex به عنوان گزینهای برای درمان موضعی در مواردی که درمان سرکوبکننده سیستم ایمنی دشوار است، مورد توجه قرار گرفته است. در گزارش موردی Bordin و همکاران (2023)، تزریق مکرر هر شش ماه منجر به تثبیت عملکرد و کاهش تیتر آنتیبادی ضد ریکاورین شد 1). ترکیب این درمان با پایش خودآنتیبادیها پس از تزریق ممکن است ارزیابی پاسخ درمانی را امکانپذیر سازد.
با گسترش استفاده از ICI، نیاز به تمایز عوارض چشمی مرتبط با دارو از CAR/MAR افزایش یافته است 3). تشخیص زودهنگام و تدوین پروتکل مداخله مناسب از چالشهای آینده است.
آنتیبادیهای ضد گیرنده IL-6 مانند توسیلیزوماب و ساریلوماب برای AIR همراه با ادم ماکولار سیستوئید مقاوم به درمان استفاده شدهاند و کاربرد آنها در CAR نیز در حال بررسی است1).
در مدل رت CAR، مسدودکنندههای کانال کلسیم مؤثر نشان داده شدهاند و به عنوان مداخلهای در اختلال هموستاز کلسیم ناشی از آنتیبادی ضد ریکاورین، تحقیقات آینده مورد انتظار است.
در APECED ناشی از جهش ژن AIRE، مواردی از رتینوپاتی خودایمنی از دوران کودکی گزارش شده است 2). در گزارش Sakaguchi و همکاران (2021)، الکترورتینوگرام در سن ۲ سالگی غیرقابل ثبت بود که اهمیت مداخله زودهنگام را نشان میدهد، اما درمان مؤثری هنوز ایجاد نشده است 2).