mtDNA突變
單一大片段缺失:最常見原因,佔病例的60-80%。大多數缺失範圍為1.3-1.9 kb。散發病例提示新生突變。
點突變:tRNA基因是熱點。至少35種點突變可表現為孤立性CPEO。MT-TN基因(tRNAAsn)是散發性PEO的熱點,11種突變中有7種呈現PEO表型2)。
遺傳方式:母系遺傳。異質性(正常mtDNA與突變mtDNA混合存在)是其特徵,當突變比例超過80%時,細胞層級的功能障礙會顯現出來2)3)。

慢性進行性眼外肌麻痺(CPEO)是一種由粒線體功能障礙引起的全身性疾病(粒線體腦肌病)的一種類型。它選擇性損害眼外肌,導致緩慢進展的雙側眼瞼下垂和眼球運動受限。
它是粒線體病中最常見的表型。根據英國佇列資料庫,盛行率約為1/30,000,發生率為1~2/100,000 1)。
CPEO的歷史始於1868年von Graefe的首次描述。1958年,Kearns和Sayre描述了CPEO、視網膜色素變性和心臟傳導阻滯三聯徵。1972年,肌肉活檢發現破碎紅纖維,1988~1989年檢測到mtDNA缺失。2000年,發現了首個與多發性mtDNA缺失相關的核DNA(nDNA)突變 1)。
臨床上,CPEO大致分為以下兩種類型。
部分病例在青春期前後發病,由於缺乏全身性臨床徵候,常首診於眼科。
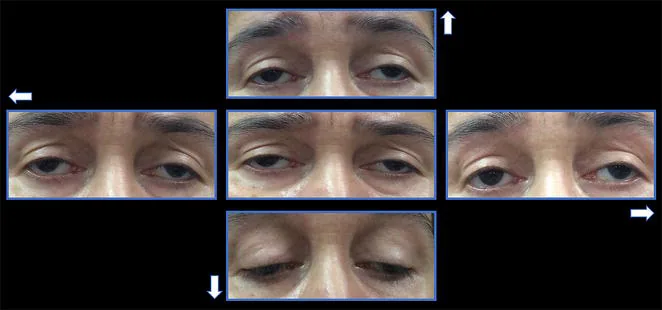
CPEO的症狀出現極為緩慢。初發症狀多為眼瞼下垂。
無痛是CPEO的特徵。眼痛、眼球突出或瞳孔異常提示其他病因。
由於CPEO雙眼對稱且緩慢受損,左右眼球運動差異小,不易產生複視。此外,進展極為緩慢,中樞適應發生。僅約1/3患者出現持續性或間歇性複視。
CPEO的原因大致分為粒線體DNA(mtDNA)突變和核DNA(nDNA)突變。
mtDNA突變
單一大片段缺失:最常見原因,佔病例的60-80%。大多數缺失範圍為1.3-1.9 kb。散發病例提示新生突變。
點突變:tRNA基因是熱點。至少35種點突變可表現為孤立性CPEO。MT-TN基因(tRNAAsn)是散發性PEO的熱點,11種突變中有7種呈現PEO表型2)。
遺傳方式:母系遺傳。異質性(正常mtDNA與突變mtDNA混合存在)是其特徵,當突變比例超過80%時,細胞層級的功能障礙會顯現出來2)3)。
nDNA突變
mtDNA維持相關基因:已報導POLG(DNA聚合酶γ)、TWNK(Twinkle)、SLC25A4(ANT1)、POLG2、RRM2B、RNASEH1、MGME1、DNA2、TK2、DGUOK等基因的突變1)5)。
多發性mtDNA缺失:nDNA突變透過損害mtDNA複製與修復導致多發性mtDNA缺失。
遺傳方式:體染色體顯性或體染色體隱性遺傳。詢問家族史很重要。
外眼肌選擇性受累的原因在於,與骨骼肌相比,其粒線體含量更高、代謝需求更大,因此對氧化磷酸化障礙的脆弱性更高。
遺傳方式因致病基因而異。mtDNA突變的散發案例為新發突變,遺傳風險較低。nDNA突變案例表現為體染色體顯性或隱性遺傳,可見家族內發病。mtDNA突變也可能透過母系遺傳傳播。建議進行遺傳諮詢。
CPEO主要基於臨床診斷,但各種檢查對確診和鑑別診斷很有幫助。在專科診所,注意力可能集中在特定疾病上,從而忽略眼瞼下垂或眼球運動障礙6)。
這是確診的關鍵檢查。
眼外肌肌電圖檢查顯示,即使眼球不能運動,仍可見干擾波形,其振幅略低於正常肌肉但放電充分。這有助於與神經源性疾病的鑑別。
需要與CPEO鑑別的主要疾病如下所示。
| 疾病 | 鑑別要點 |
|---|---|
| 重症肌無力 | 有日內波動和易疲勞性。抗AChR抗體陽性 |
| 甲狀腺眼病變 | 眼外肌肥大。伴有眼球突出 |
| 強直性肌肉萎縮症 | 以遠端肌肉為主的萎縮。叩擊性肌強直 |
重症肌無力症是最重要的鑑別診斷,因為它會導致眼瞼下垂和眼球運動障礙。重症肌無力症的特點是日間波動和易疲勞性,Tensilon試驗或冰袋試驗可改善。CPEO的眼瞼下垂是非波動性的,這些試驗不會改善。
CPEO尚無根治性治療方法。對症治療以維持生活品質(QOL)是治療的核心。
為補充粒線體功能異常,可嘗試使用以下藥物。
提肌前徙術
適應症:提肌功能中等以上保留時。
方法:進行上眼瞼提肌前徙術或切除術。經皮入路前徙固定腱膜,必要時加做Müller肌摺疊術。
注意:CPEO中提肌功能進行性惡化,因此長期效果可能減弱。
額肌懸吊術
適應症:提眼瞼肌功能不良(小於4mm)。CPEO通常選擇此術式。
方法:使用自體筋膜(闊筋膜、顳筋膜)、Gore-Tex®片、尼龍線、矽膠棒等將上眼瞼連接到額肌。
注意:過度矯正會導致兔眼和角膜暴露,有引起暴露性角膜病變和角膜潰瘍的風險。
必須由經驗豐富的眼整形外科醫師進行仔細的術前評估。如果Bell現象缺失,應保持低矯。
CPEO是進展性疾病,術後提眼瞼肌功能可能逐漸惡化,導致眼瞼下垂復發。尤其在兒童病例中,隨著生長發育常需再次手術。額肌懸吊術使用的材料長期可能減弱牽引力。定期追蹤很重要。
CPEO的本質是由於mtDNA或nDNA突變導致的氧化磷酸化障礙。
粒線體擁有自己的DNA(mtDNA),編碼氧化磷酸化所需的13種蛋白質。mtDNA的缺失或點突變會降低電子傳遞鏈酶的活性,導致ATP生成不足。與骨骼肌相比,眼外肌的粒線體含量更高,為維持抗疲勞性需要更大的代謝需求。這一特性被認為是CPEO中選擇性累及眼外肌的原因之一。
異質性(heteroplasmy)是CPEO的重要病理概念。正常mtDNA和突變mtDNA共存於同一細胞內,當突變mtDNA的比例超過閾值(通常80%以上)時,粒線體功能就會發生障礙。
Visuttijai等人(2021)報導了MT-TN基因的兩個新發點突變(m.5669G>A和m.5702delA)。單肌纖維分析顯示,COX陰性纖維中的突變比例平均為93%,與COX正常纖維(32%和57%)相比有顯著差異(P < 0.0001)。兩例的COX功能障礙閾值均在80%以上2)。
Katayama Ueda等人(2025)在一例日本男性CPEO病例中鑑定出tRNAGlu基因的新發突變(m.14677T>C)。破碎紅纖維(ragged red fiber)中的突變比例中位數為88.1%,顯著高於非破碎紅纖維(中位數17.1%)(P = 0.03)3)。
關於nDNA突變,POLG基因是CPEO最常見的核基因原因之一。POLG編碼mtDNA複製所需的DNA聚合酶γ,其突變通過損害mtDNA複製導致多發性mtDNA缺失。
Liu等人(2023)報導了一名38歲女性,攜帶POLG基因已知突變c.2857C>T(p.R953C)和新發突變c.2391G>C(p.M797I)。她出現肢體無力和麻木,隨後出現眼瞼下垂,肌肉活檢顯示破碎紅纖維5)。
在兒童期發病的粒線體腦肌病中,5-氨基乙醯丙酸(5-ALA)與鐵劑的聯合治療被認為可提高ATP生成,並已開始臨床試驗。然而,其在CPEO中的療效尚不清楚。
KH176是一種線粒體靶向的氧化還原調節劑,可減少活性氧介導的細胞損傷。
一項評估KH176(100mg,每日兩次)在CPEO患者中的安全性和有效性的II期臨床試驗已啟動(NCT04604548)5)。
正在嘗試使用安全載體導入正常基因。此外,利用異質性特性,通過寡核苷酸RNA抑制突變mtDNA的方法也有報導。
作為線粒體基因組操作技術,使用限制酶、TALEN、ZFN和CRISPR選擇性去除突變mtDNA的研究正在進行中1)。生殖系替代療法(原核移植、卵母細胞紡錘體移植)也處於動物模型和臨床試驗階段。
Fan等人(2021)在CPEO-plus症候群患者的肌肉MR頻譜中檢測到1-2ppm的雙峰(提示乳酸積累)。在水腫肌肉中更為明顯,表明其作為疾病監測生物標誌物的潛力4)。