โรคกล้ามเนื้อตาอ่อนแรงเรื้อรังแบบลุกลาม (CPEO) เป็นโรคกล้ามเนื้อเสื่อมทางพันธุกรรมชนิดหนึ่งที่เกิดจากความผิดปกติของไมโทคอนเดรีย
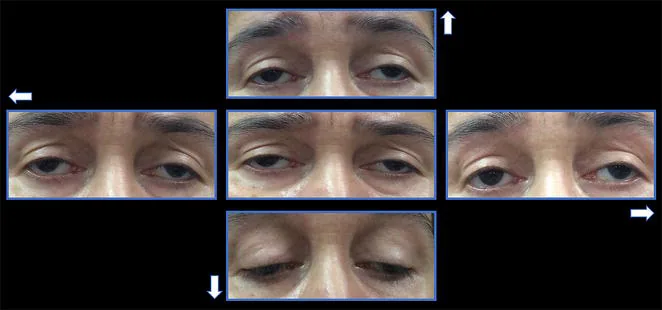
ลักษณะสำคัญคือหนังตาตก ทั้งสองข้างแบบสมมาตร ค่อยเป็นค่อยไป และการเคลื่อนไหวลูกตาผิดปกติทุกทิศทาง โดยรูม่านตา ยังปกติ
60-80% ของผู้ป่วยพบการขาดหายของดีเอ็นเอไมโทคอนเดรีย (mtDNA)
CPEO แบ่งเป็นชนิดที่เกิดเฉพาะที่ และชนิด CPEO-plus ที่มีอาการทั่วร่างกาย (เช่น Kearns-Sayre syndrome)
ยังไม่มีการรักษาที่หายขาด แต่สามารถลองใช้โคเอนไซม์คิวเท็นและวิตามินเสริม
สำหรับหนังตาตก อาจทำการผ่าตัดร่นกล้ามเนื้อลืมตาหรือผูกกล้ามเนื้อหน้าผาก แต่ต้องระวังกระจกตา โผล่จากการแก้ไขมากเกินไป
การตัดชิ้นเนื้อกล้ามเนื้อและการตรวจทางพันธุกรรมมีประโยชน์ในการยืนยันการวินิจฉัย และสิ่งสำคัญคือต้องแยกโรคกล้ามเนื้ออ่อนแรงชนิดไมแอสทีเนีย กราวิส และโรคตาจากต่อมไทรอยด์
โรคกล้ามเนื้อตาอ่อนแรงเรื้อรังแบบลุกลาม (chronic progressive external ophthalmoplegia: CPEO) เป็นโรคทางระบบชนิดหนึ่ง (โรคสมองและกล้ามเนื้อจากไมโทคอนเดรีย) ที่เกิดจากความผิดปกติของไมโทคอนเดรีย โดยเลือกทำลายกล้ามเนื้อนอกลูกตา ทำให้หนังตาตก ทั้งสองข้างแบบค่อยเป็นค่อยไป และจำกัดการเคลื่อนไหวของลูกตา
CPEO ถือเป็นฟีโนไทป์ที่พบบ่อยที่สุดของโรคไมโทคอนเดรีย ตามฐานข้อมูลกลุ่มประชากรในสหราชอาณาจักร ความชุกประมาณ 1/30,000 และอุบัติการณ์ 1-2/100,000 1)
ประวัติของ CPEO เริ่มต้นจากคำอธิบายครั้งแรกโดย von Graefe ในปี 1868 ในปี 1958 Kearns และ Sayre บรรยายสามอาการของ CPEO จอประสาทตา อักเสบชนิดรงควัตถุ และความผิดปกติของการนำไฟฟ้าหัวใจ ในปี 1972 พบเส้นใยกล้ามเนื้อสีแดงขาดรุ่งริ่ง (ragged red fiber) ในการตัดชิ้นเนื้อกล้ามเนื้อ และในปี 1988-1989 ตรวจพบการขาดหายของ mtDNA ในปี 2000 พบการกลายพันธุ์ของดีเอ็นเอนิวเคลียส (nDNA) ครั้งแรกที่เกี่ยวข้องกับการขาดหายหลายตำแหน่งของ mtDNA 1)
ทางคลินิก CPEO แบ่งออกเป็น 2 ชนิดดังต่อไปนี้
CPEO แบบแยกเดี่ยว : มีเฉพาะอาการทางตาโดยไม่มีอาการทางระบบ มักเริ่มในอายุ 30-40 ปีCPEO-plus : ร่วมกับอาการทางระบบ เช่น การสูญเสียการได้ยินแบบประสาทรับเสียง, กลืนลำบาก, ความผิดปกติของการนำไฟฟ้าหัวใจ, การเคลื่อนไหวผิดปกติของสมองน้อย, และกล้ามเนื้อส่วนต้นอ่อนแรง กลุ่มอาการ Kearns-Sayre (KSS) เป็นตัวอย่างที่พบบ่อย
บางรายเริ่มก่อนหรือหลังวัยรุ่น โดยมีอาการทางระบบน้อย มักมาพบจักษุแพทย์เป็นอันดับแรก
Q
ความแตกต่างระหว่าง CPEO และ CPEO-plus คืออะไร?
A
CPEO แบบแยกเดี่ยวมีเฉพาะหนังตาตก และการเคลื่อนไหวตาผิดปกติโดยไม่มีอาการทางระบบ CPEO-plus ร่วมกับอาการทางระบบ เช่น การสูญเสียการได้ยินแบบประสาทรับเสียง, กลืนลำบาก, ความผิดปกติของการนำไฟฟ้าหัวใจ, และการเคลื่อนไหวผิดปกติของสมองน้อย กลุ่มอาการ Kearns-Sayre เป็นโรค CPEO-plus ที่พบบ่อย เริ่มก่อนอายุ 20 ปี ร่วมกับจอประสาทตา อักเสบชนิดรงควัตถุและความผิดปกติของการนำไฟฟ้าหัวใจ
?????????????????????? Alvaro Ortiz, Juan Arias, Pedro Cárdenas et al. Macular findings in Spectral Domain Optical Coherence Tomography and
OCT Angiography in a patient with Kearns–Sayre syndrome. International Journal of Retina and Vitreous. 2017 Jul 10; 3:24. Figure 1. PM
CI D: PMC5502322. License: CC BY.
????????????????????????????????CPEO??????????????????????????
อาการของ CPEO เริ่มช้ามาก อาการแรกมักเป็นหนังตาตก
หนังตาตก การเคลื่อนไหวตาผิดปกติ : เกิดขึ้นหลังจากหนังตาตก ไม่กี่ปี การจำกัดการเคลื่อนไหวทุกทิศทางค่อยเป็นค่อยไปไม่มีภาพซ้อน : เนื่องจากตาทั้งสองข้างถูกกระทบแบบสมมาตร จึงมักไม่มีภาพซ้อน แม้การเคลื่อนไหวตาจะผิดปกติมากการชดเชยด้วยท่าศีรษะ : ชดเชยการเคลื่อนไหวตาที่จำกัดโดยการเปลี่ยนท่าศีรษะการไม่ทนต่อการออกแรง : ในรายที่มีกล้ามเนื้ออ่อนแรงทั่วร่างกาย ผู้ป่วยจะเหนื่อยง่าย
ลักษณะเด่นของ CPEO คือไม่เจ็บปวด อาการปวดตา ตาโปน หรือความผิดปกติของรูม่านตา บ่งชี้สาเหตุอื่น
หนังตาตก 1) ในรายที่รุนแรง หนังตาตก จะมากจำกัดการเคลื่อนไหวลูกตา : ทุกทิศทาง อาจพบตาเหล่ แบบออกในท่าปกติรูม่านตา ปกติความผิดปกติของรูม่านตา หากมีม่านตา ขยาย ควรคิดถึงสาเหตุอื่น เช่น อัมพาตเส้นประสาทกล้ามเนื้อตาหลับตาไม่สนิท : ร่วมกับหนังตาตก กล้ามเนื้อ orbicularis oculi อ่อนแรงทำให้หลับตาไม่สนิท อาจมีกระจกตา อักเสบจากตาแห้ง ผลตรวจจอตา : การถ่ายภาพหลอดเลือดด้วยฟลูออเรสซีน อาจพบการเรืองแสงมากเกินแบบเม็ดเล็กๆ ที่ระดับ retinal pigment epithelium ถ้าร่วมกับจอตาเสื่อมแบบ salt and pepper บ่งชี้ถึง Kearns-Sayre syndromeMRI เบ้าตา : พบกล้ามเนื้อนอกตาฝ่อ
Q
ทำไมผู้ป่วย CPEO จึงไม่ค่อยรู้สึกเห็นภาพซ้อน?
A
เนื่องจาก CPEO ส่งผลต่อตาทั้งสองข้างอย่างสมมาตรและช้า ความแตกต่างของการเคลื่อนไหวตาจึงน้อย ทำให้เกิดภาพซ้อน ได้ยาก นอกจากนี้ การดำเนินโรคช้ามากทำให้เกิดการปรับตัวจากส่วนกลาง ผู้ป่วยประมาณหนึ่งในสามเท่านั้นที่มีภาพซ้อน แบบคงที่หรือเป็นๆ หายๆ
สาเหตุของ CPEO แบ่งออกเป็นหลักๆ คือ การกลายพันธุ์ของ DNA ในไมโตคอนเดรีย (mtDNA) และการกลายพันธุ์ของ DNA ในนิวเคลียส (nDNA)
การกลายพันธุ์ mtDNA
การขาดหายขนาดใหญ่เดี่ยว : สาเหตุที่พบบ่อยที่สุด คิดเป็น 60-80% ของกรณี ส่วนใหญ่เป็นการขาดหายในช่วง 1.3-1.9 kb กรณีที่เกิดขึ้นประปรายบ่งชี้ถึงการกลายพันธุ์แบบ de novo
การกลายพันธุ์แบบจุด : ยีน tRNA เป็นจุดร้อน การกลายพันธุ์แบบจุดอย่างน้อย 35 ชนิดสามารถแสดงออกเป็น CPEO แบบเดี่ยวได้ ยีน MT-TN (tRNAAsn) เป็นจุดร้อนสำหรับ PEO แบบประปราย โดย 7 ใน 11 การกลายพันธุ์ให้ฟีโนไทป์ PEO 2)
รูปแบบการถ่ายทอดทางพันธุกรรม : การถ่ายทอดทางมารดา ลักษณะเฉพาะคือ Heteroplasmy (การผสมของ mtDNA ปกติและ mtDNA กลายพันธุ์) และเมื่อสัดส่วนการกลายพันธุ์เกิน 80% ความผิดปกติในระดับเซลล์จะปรากฏชัดเจน2) 3)
การกลายพันธุ์ของ nDNA
ยีนที่เกี่ยวข้องกับการบำรุงรักษา mtDNA : มีรายงานการกลายพันธุ์ใน POLG (DNA polymerase γ), TWNK (Twinkle), SLC25A4 (ANT1), POLG2, RRM2B, RNASEH1, MGME1, DNA2, TK2, DGUOK และอื่นๆ1) 5)
การขาดหายหลายตำแหน่งของ mtDNA : การกลายพันธุ์ของ nDNA ทำให้เกิดการขาดหายหลายตำแหน่งของ mtDNA ผ่านการรบกวนการจำลองและซ่อมแซม mtDNA
รูปแบบการถ่ายทอดทางพันธุกรรม : การถ่ายทอดแบบ autosomal dominant หรือ autosomal recessive การซักประวัติครอบครัวเป็นสิ่งสำคัญ
เหตุผลที่กล้ามเนื้อนอกลูกตา ได้รับผลกระทบแบบเลือกสรรคือ มีปริมาณไมโตคอนเดรียสูงกว่าและความต้องการเมแทบอลิซึมมากกว่าเมื่อเทียบกับกล้ามเนื้อโครงร่าง ทำให้ไวต่อความผิดปกติของ oxidative phosphorylation มากขึ้น
CPEO เป็นโรคทางพันธุกรรม และยังไม่มีวิธีการป้องกันที่แน่นอน โปรดคำนึงถึงประเด็นต่อไปนี้
หากมีการปิดตาไม่สนิท ให้ใช้น้ำตาเทียม หรือยาขี้ผึ้งทาตาเพื่อปกป้องกระจกตา
หากมีกล้ามเนื้ออ่อนแรงทั่วร่างกาย ให้ออกกำลังกายแบบแอโรบิกในขอบเขตที่เหมาะสมต่อไป
หากสงสัยว่าเป็น KSS ให้ตรวจคลื่นไฟฟ้าหัวใจเป็นประจำ
แนะนำให้รับคำปรึกษาทางพันธุกรรม
Q
CPEO ถ่ายทอดทางพันธุกรรมหรือไม่?
A
รูปแบบการถ่ายทอดทางพันธุกรรมแตกต่างกันไปตามยีนที่เป็นสาเหตุ กรณีประปรายของการกลายพันธุ์ mtDNA คือการกลายพันธุ์ใหม่ (de novo) และความเสี่ยงทางพันธุกรรมต่ำ กรณีการกลายพันธุ์ nDNA แสดงการถ่ายทอดแบบ autosomal dominant หรือ recessive โดยมีการเกิดในครอบครัว การกลายพันธุ์ mtDNA ก็สามารถถ่ายทอดผ่านทางมารดาได้เช่นกัน แนะนำให้รับคำปรึกษาทางพันธุกรรม
CPEO วินิจฉัยทางคลินิกเป็นหลัก แต่การตรวจต่างๆ มีประโยชน์ในการยืนยันและแยกโรค ในคลินิกเฉพาะทาง ความสนใจอาจมุ่งไปที่โรคใดโรคหนึ่ง ทำให้มองข้ามหนังตาตก หรือความผิดปกติของการเคลื่อนไหวลูกตา 6)
การตรวจเลือด : อาจพบระดับแลคเตทในซีรัม ครีเอทีนไคเนส (CK) และแลคเตทในน้ำไขสันหลังสูงขึ้น แต่ความไวและความจำเพาะไม่สูง การเพิ่มขึ้นของไพรูเวทในเลือดหรืออัตราส่วนแลคเตท/ไพรูเวทก็มีประโยชน์เช่นกันการตรวจแอนติบอดี : การยืนยันผลลบของแอนติบอดีต่อตัวรับอะเซทิลโคลีนและแอนติบอดีต่อต่อมไทรอยด์มีประโยชน์ในการแยกโรคกล้ามเนื้ออ่อนแรงชนิดไมแอสทีเนีย กราวิส และโรคตาจากต่อมไทรอยด์ ตัวบ่งชี้ทางชีวภาพ 1)
นี่คือการตรวจที่สำคัญสำหรับการวินิจฉัยที่แน่นอน
การย้อม Gomori trichrome : พบ ragged red fiber ไมโทคอนเดรียที่สะสมภายในและรอบเส้นใยกล้ามเนื้อจะติดสีเข้มการย้อมคู่ COX/SDH : พบเส้นใยที่ให้ผลลบต่อไซโตโครม ซี ออกซิเดส (COX) ปรากฏเป็นลายโมเสกกล้องจุลทรรศน์อิเล็กตรอน : พบไมโทคอนเดรียขนาดใหญ่ที่มีรูปร่างผิดปกติระหว่างเส้นใยกล้ามเนื้อ
ในการตรวจคลื่นไฟฟ้ากล้ามเนื้อของกล้ามเนื้อนอกลูกตา จะเห็นรูปแบบการแทรกสอด (interference pattern) ที่มีการปล่อยกระแสเพียงพอแม้แอมพลิจูดจะอ่อนกว่ากล้ามเนื้อปกติเล็กน้อย แม้ในขณะที่ไม่สามารถเคลื่อนไหวลูกตาได้ ซึ่งมีประโยชน์ในการแยกจากโรคของเส้นประสาท
การขาดหายของ mtDNA : วิธี Southern blot โดยใช้ตัวอย่างชิ้นเนื้อกล้ามเนื้อโครงร่างมีความน่าเชื่อถือ การใช้ long PCR อาจตรวจพบในเลือดส่วนปลายได้ในบางกรณีการกลายพันธุ์แบบจุดของ mtDNA : การวิเคราะห์ mtDNA ทั้งหมดด้วยการหาลำดับยุคถัดไป (NGS) มีประสิทธิภาพ บางครั้งตรวจไม่พบในเลือดและตรวจพบได้เฉพาะในเนื้อเยื่อกล้ามเนื้อ 2) 3) การกลายพันธุ์ของ nDNA : มีการวิเคราะห์เอ็กโซมของยีนที่เกี่ยวข้อง เช่น POLG, TWNK , SLC25A4 5) .
MRI วงโคจร : แสดงการฝ่อของกล้ามเนื้อนอกลูกตา MRI สมอง : อาจพบสัญญาณสูงในสารสีขาว, การฝ่อของคอร์เทกซ์, การฝ่อของซีรีเบลลัม, และสัญญาณสูงในก้านสมอง ในกรณีหนึ่งของ KSS มีรายงานการฝ่อของซีรีเบลลัมข้างเดียวที่ดำเนินไปตามเวลา 7) .MR spectroscopy (MRS) : สามารถตรวจพบการสะสมของแลคเตทในกล้ามเนื้อแบบไม่รุกล้ำ และอาจมีประโยชน์ในการติดตามโรค 4) .
โรคหลักที่ต้องแยกจาก CPEO แสดงไว้ด้านล่าง
โรค จุดที่ใช้แยก โรคกล้ามเนื้ออ่อนแรงชนิดร้าย (Myasthenia Gravis) มีความผันผวนระหว่างวันและอ่อนเพลียง่าย แอนติบอดีต่อ AChR เป็นบวก โรคตาจากต่อมไทรอยด์ กล้ามเนื้อนอกลูกตา โตเกิน ร่วมกับตาโปนโรคกล้ามเนื้อเสื่อมชนิดไมโอโทนิก กล้ามเนื้อลีบที่ปลายเป็นหลัก มีภาวะกล้ามเนื้อหดเกร็งเมื่อถูกเคาะ
โรคกล้ามเนื้ออ่อนแรงชนิดไมแอสทีเนีย กราวิส (Myasthenia gravis) เป็นโรคที่ต้องแยกให้สำคัญที่สุด เพราะทำให้หนังตาตก และการเคลื่อนไหวลูกตาผิดปกติ โรคกล้ามเนื้ออ่อนแรงชนิดนี้มีลักษณะเฉพาะคืออาการเปลี่ยนแปลงในแต่ละวันและอ่อนเพลียง่าย และดีขึ้นเมื่อทดสอบด้วยเทนซิลอน (Tensilon) หรือการประคบน้ำแข็ง หนังตาตก ใน CPEO จะไม่เปลี่ยนแปลงและไม่ดีขึ้นเมื่อทดสอบเหล่านี้
ยังไม่มีการรักษาที่หายขาดสำหรับ CPEO การรักษามุ่งเน้นการรักษาคุณภาพชีวิตด้วยการรักษาตามอาการ
มีการลองใช้ยาต่อไปนี้เพื่อเสริมการทำงานที่ผิดปกติของไมโทคอนเดรีย
โคเอนไซม์ Q10 (Ubidecarenone/Neukinon®) : ช่วยในการถ่ายโอนอิเล็กตรอนในกระบวนการออกซิเดทีฟฟอสโฟรีเลชัน อาจเห็นการดีขึ้นในบางกรณีวิตามินบีรวม : สนับสนุนการเผาผลาญในฐานะโคเอนไซม์วิตามินซี : ใช้ร่วมกันเพื่อฤทธิ์ต้านอนุมูลอิสระแอล-คาร์นิทีน : ช่วยในการเผาผลาญกรดไขมัน
การเลื่อนกล้ามเนื้อลิเวเตอร์ (Levator advancement)
ข้อบ่งชี้ : เมื่อการทำงานของกล้ามเนื้อลิเวเตอร์ยังคงอยู่ในระดับปานกลางขึ้นไป
วิธีการ : ทำการเลื่อนหรือตัดกล้ามเนื้อลิเวเตอร์ของหนังตาบน โดยผ่านทางผิวหนัง เลื่อนและตรึงเอพิเนวโรซิส (aponeurosis) และเพิ่มการจับกล้ามเนื้อมุลเลอร์ (Muller’s muscle) หากจำเป็น
ข้อควรระวัง : ใน CPEO การทำงานของกล้ามเนื้อลิเวเตอร์จะแย่ลงเรื่อยๆ ดังนั้นผลการรักษาอาจลดลงในระยะยาว
การแขวนกล้ามเนื้อหน้าผาก (Frontalis suspension)
ข้อบ่งชี้ : เมื่อการทำงานของกล้ามเนื้อลิเวเตอร์ไม่ดี (น้อยกว่า 4 มม.) ใน CPEO มักเลือกวิธีนี้
วิธีการ : เชื่อมต่อหนังตาบนกับกล้ามเนื้อหน้าผากโดยใช้พังผืดตนเอง (พังผืดต้นขาหรือพังผืดขมับ), แผ่น Gore-Tex®, ไนลอน, หรือแท่งซิลิโคน
ข้อควรระวัง : การแก้ไขมากเกินไปทำให้เกิดตาแห้ง (lagophthalmos) และกระจกตา เปิดรับแสง เพิ่มความเสี่ยงต่อโรคกระจกตา จากการเปิดรับแสงและแผลที่กระจกตา
จำเป็นต้องประเมินก่อนผ่าตัดอย่างรอบคอบโดยศัลยแพทย์ตกแต่งทางตาที่มีประสบการณ์ หากไม่มีปรากฏการณ์เบลล์ ควรแก้ไขน้อยเกินไป
เลนส์ปริซึม : มีประสิทธิภาพในการลดภาพซ้อน สำหรับตาเหล่ ในมุมเล็กการผ่าตัดตาเหล่ : การตัดกล้ามเนื้อที่ผิดปกติให้สั้นลงเพื่อแก้ไขในตำแหน่งแรก หากมุมมาก จะทำการเลื่อนกล้ามเนื้อคู่ตรงข้ามด้วย เนื่องจากโรคดำเนินไป อาจเกิดซ้ำได้
การประเมินการทำงานของหัวใจ : ใน KSS มีความเสี่ยงต่อความผิดปกติของการนำไฟฟ้าหัวใจ (AV block) จำเป็นต้องตรวจคลื่นไฟฟ้าหัวใจเป็นระยะและตัดสินใจใส่เครื่องกระตุ้นหัวใจความผิดปกติของต่อมไร้ท่อ : จำเป็นต้องจัดการโรคเบาหวาน ภาวะขาดฮอร์โมนการเจริญเติบโต และเตี้ยการประเมินการได้ยิน : แนะนำให้ตรวจการได้ยินเป็นระยะสำหรับการสูญเสียการได้ยินแบบประสาทรับเสียง
การแก้ไขมากเกินไปในการผ่าตัดหนังตาตก อาจทำให้เกิดตาแห้ง (หลับตาไม่สนิท) ส่งผลให้กระจกตา เปิดรับแสง แผลที่กระจกตา หรือทะลุ ใน CPEO กล้ามเนื้อ orbicularis ก็อ่อนแรงเช่นกัน ดังนั้นควรประเมินการหลับตาหลังผ่าตัดอย่างระมัดระวัง หากหลับตาไม่สนิท ≥2 มม. หลังผ่าตัด ควรพิจารณาการยึดตรึงใหม่
Q
หนังตาตกสามารถกลับมาเป็นซ้ำหลังผ่าตัดได้หรือไม่?
A
เนื่องจาก CPEO เป็นโรคที่ดำเนินไป การทำงานของกล้ามเนื้อลิเวเตอร์อาจแย่ลงเรื่อยๆ หลังผ่าตัด ทำให้หนังตาตก กลับมาเป็นซ้ำ โดยเฉพาะในเด็ก มักต้องผ่าตัดซ้ำเมื่อโตขึ้น วัสดุที่ใช้ในการผ่าตัดแขวนหนังตากับกล้ามเนื้อหน้าผากอาจสูญเสียแรงดึงในระยะยาว การติดตามผลอย่างสม่ำเสมอเป็นสิ่งสำคัญ
สาระสำคัญของ CPEO คือความผิดปกติของ oxidative phosphorylation เนื่องจากการกลายพันธุ์ของ mtDNA หรือ nDNA
ไมโทคอนเดรียมี DNA ของตัวเอง (mtDNA) ซึ่งเข้ารหัสโปรตีน 13 ชนิดที่จำเป็นสำหรับ oxidative phosphorylation การขาดหายหรือการกลายพันธุ์แบบจุดใน mtDNA ทำให้กิจกรรมของเอนไซม์ในห่วงโซ่การขนส่งอิเล็กตรอนลดลง ส่งผลให้การผลิต ATP ไม่เพียงพอ กล้ามเนื้อนอกลูกตา มีปริมาณไมโทคอนเดรียสูงกว่ากล้ามเนื้อโครงร่าง และมีความต้องการเมแทบอลิซึมมากกว่าเพื่อรักษาความต้านทานต่อความเมื่อยล้า คุณสมบัตินี้ถือเป็นสาเหตุหนึ่งที่ทำให้กล้ามเนื้อนอกลูกตา ถูกทำลายแบบเลือกสรรใน CPEO
Heteroplasmy เป็นแนวคิดทางพยาธิวิทยาที่สำคัญใน CPEO เป็นปรากฏการณ์ที่ mtDNA ปกติและ mtDNA กลายพันธุ์อยู่ร่วมกันในเซลล์เดียวกัน เมื่อสัดส่วนของ mtDNA กลายพันธุ์เกินเกณฑ์ (โดยปกติ >80%) ไมโทคอนเดรียนั้นจะทำงานผิดปกติ
Visuttijai และคณะ (2021) รายงานการกลายพันธุ์แบบจุดใหม่สองตำแหน่งในยีน MT-TN (m.5669G>A และ m.5702delA) การวิเคราะห์เส้นใยกล้ามเนื้อเดี่ยวพบว่าสัดส่วนการกลายพันธุ์เฉลี่ยในเส้นใย COX-ลบ เท่ากับ 93% ซึ่งแตกต่างอย่างมีนัยสำคัญจากเส้นใย COX-ปกติ (32% และ 57%) (P < 0.0001) เกณฑ์ความผิดปกติของ COX ในทั้งสองกรณีคือ >80%2)
Katayama Ueda และคณะ (2025) ระบุการกลายพันธุ์ใหม่ (m.14677T>C) ในยีน tRNAGlu ในผู้ป่วย CPEO ชายชาวญี่ปุ่น ค่ามัธยฐานของสัดส่วนการกลายพันธุ์ในเส้นใย ragged red คือ 88.1% ซึ่งสูงกว่าอย่างมีนัยสำคัญในเส้นใยที่ไม่ใช่ ragged red (ค่ามัธยฐาน 17.1%) (P = 0.03)3)
ในส่วนของการกลายพันธุ์ของ nDNA ยีน POLG เป็นหนึ่งในสาเหตุทางนิวเคลียร์ที่พบบ่อยที่สุดของ CPEO POLG เข้ารหัส DNA polymerase γ ที่จำเป็นสำหรับการจำลอง mtDNA และการกลายพันธุ์ของมันทำให้เกิดการขาดหายหลายตำแหน่งของ mtDNA ผ่านการบกพร่องของการจำลอง mtDNA
Liu และคณะ (2023) รายงานหญิงอายุ 38 ปีที่มีการกลายพันธุ์ที่ทราบแล้ว c.2857C>T (p.R953C) และการกลายพันธุ์ใหม่ c.2391G>C (p.M797I) ในยีน POLG มีอาการหนังตาตก นอกเหนือจากอ่อนแรงและชาที่แขนขา และการตรวจชิ้นเนื้อกล้ามเนื้อยืนยันว่ามีเส้นใย ragged red5)
ในโรคสมองและกล้ามเนื้อจากไมโทคอนเดรียที่เริ่มในวัยเด็ก การรักษาแบบผสมผสานด้วยกรด 5-aminolevulinic (5-ALA) และการเสริมธาตุเหล็กได้รับการแนะนำว่าสามารถเพิ่มการผลิต ATP และได้เริ่มมีการทดลองทางคลินิกแล้ว อย่างไรก็ตาม ประสิทธิภาพใน CPEO ยังไม่เป็นที่ทราบ
KH176 เป็นสารควบคุมรีดอกซ์ที่กำหนดเป้าหมายไมโตคอนเดรีย ลดความเสียหายของเซลล์ที่เกิดจากออกซิเจนชนิดปฏิกิริยา
การทดลองทางคลินิกระยะที่ 2 เพื่อประเมินความปลอดภัยและประสิทธิภาพของ KH176 (100 มก. วันละสองครั้ง) ในผู้ป่วย CPEO ได้เริ่มขึ้นแล้ว (NCT 04604548)5)
มีความพยายามในการนำยีนปกติเข้าสู่ร่างกายโดยใช้พาหะที่ปลอดภัย นอกจากนี้ยังมีรายงานวิธีการยับยั้ง mtDNA ที่กลายพันธุ์ด้วย oligo RNA โดยใช้ประโยชน์จากลักษณะเฮเทอโรพลาสมี
ในฐานะเทคนิคการจัดการจีโนมไมโตคอนเดรีย การกำจัด mtDNA ที่กลายพันธุ์แบบเลือกสรรโดยใช้เอนไซม์ตัดจำเพาะ TALEN, ZFN และ CRISPR กำลังอยู่ระหว่างการศึกษา1) การบำบัดทดแทนในสายสืบพันธุ์ (การย้ายนิวเคลียสก่อนปฏิสนธิ/การย้ายแกนหมุนของโอโอไซต์) อยู่ในขั้นตอนของแบบจำลองสัตว์และการทดลองทางคลินิก
Fan และคณะ (2021) ตรวจพบยอดคู่ที่ 1-2 ppm (บ่งชี้การสะสมของแลคเตท) ในการตรวจสเปกโทรสโกปีด้วยคลื่นแม่เหล็กไฟฟ้าของกล้ามเนื้อในผู้ป่วยกลุ่มอาการ CPEO-plus พบได้เด่นชัดกว่าในกล้ามเนื้อที่มีอาการบวมน้ำ ซึ่งบ่งชี้ถึงศักยภาพในการเป็นตัวบ่งชี้ทางชีวภาพ สำหรับการติดตามโรค4)
Ali A, Esmaeil A, Behbehani R. Mitochondrial Chronic Progressive External Ophthalmoplegia. Brain Sci. 2024;14(2):135.
Visuttijai K, Hedberg-Oldfors C, Lindgren U, et al. Progressive external ophthalmoplegia associated with novel MT-TN mutations. Acta Neurol Scand. 2021;143(1):103-108.
Katayama Ueda N, Mimaki M, Ito S, et al. A novel m.14677 T > C variant in mitochondrial tRNAGlu gene causes chronic progressive external ophthalmoplegia. J Hum Genet. 2025;70:537-540.
Fan SP, Hsueh HW, Huang HC, et al. Lactate peak in muscle disclosed by magnetic resonance spectroscopy in a patient with CPEO-plus syndrome. eNeurologicalSci. 2021;24:100360.
Liu H, Gao M, Sun Q, et al. A case of mitochondrial myopathy and chronic progressive external ophthalmoplegia. J Cent South Univ (Med Sci). 2023;48(11):1760-1768.
Karagiannis D, Kontomichos L, Tzimis V, et al. Progressive External Ophthalmoplegia Diagnosed in the Glaucoma Clinic: The Importance of a Complete Clinical Examination. Clin Optom. 2021;13:335-339.
Zhao H, Shi M, Yang F, Yang X. Kearns-Sayre syndrome with rare imaging finding of SLC25A4 Mutation. Neurosciences. 2022;27(2):111-115.