mtDNA突变
单一大片段缺失:最常见原因,占病例的60-80%。大多数缺失范围为1.3-1.9 kb。散发病例提示新生突变。
点突变:tRNA基因是热点。至少35种点突变可表现为孤立性CPEO。MT-TN基因(tRNAAsn)是散发性PEO的热点,11种突变中有7种呈现PEO表型2)。
遗传方式:母系遗传。异质性(正常mtDNA和突变mtDNA混合存在)是其特征,当突变比例超过80%时,细胞水平的功能障碍会显现出来2)3)。

慢性进行性眼外肌麻痹(CPEO)是一种由线粒体功能障碍引起的全身性疾病(线粒体脑肌病)的一种类型。它选择性损害眼外肌,导致缓慢进展的双侧上睑下垂和眼球运动受限。
它是线粒体病中最常见的表型。根据英国队列数据库,患病率约为1/30,000,发病率为1~2/100,000 1)。
CPEO的历史始于1868年von Graefe的首次描述。1958年,Kearns和Sayre描述了CPEO、视网膜色素变性和心脏传导阻滞三联征。1972年,肌肉活检发现破碎红纤维,1988~1989年检测到mtDNA缺失。2000年,发现了首个与多发性mtDNA缺失相关的核DNA(nDNA)突变 1)。
临床上,CPEO大致分为以下两种类型。
部分病例在青春期前后发病,由于缺乏全身性临床体征,常首诊于眼科。
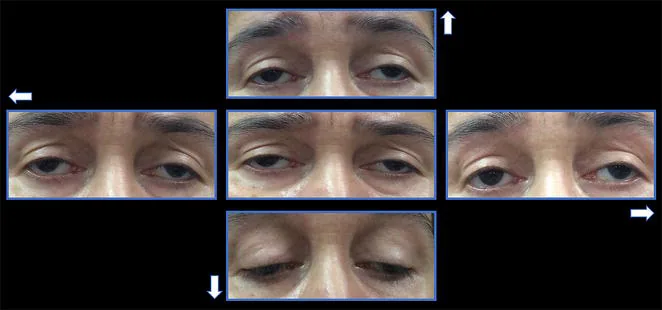
CPEO的症状出现极为缓慢。首发症状多为上睑下垂。
无痛是CPEO的特征。眼痛、眼球突出或瞳孔异常提示其他病因。
由于CPEO双眼对称且缓慢受累,左右眼球运动差异小,不易产生复视。此外,进展极为缓慢,中枢适应发生。仅约1/3患者出现持续性或间歇性复视。
CPEO的原因大致分为线粒体DNA(mtDNA)突变和核DNA(nDNA)突变。
mtDNA突变
单一大片段缺失:最常见原因,占病例的60-80%。大多数缺失范围为1.3-1.9 kb。散发病例提示新生突变。
点突变:tRNA基因是热点。至少35种点突变可表现为孤立性CPEO。MT-TN基因(tRNAAsn)是散发性PEO的热点,11种突变中有7种呈现PEO表型2)。
遗传方式:母系遗传。异质性(正常mtDNA和突变mtDNA混合存在)是其特征,当突变比例超过80%时,细胞水平的功能障碍会显现出来2)3)。
nDNA突变
mtDNA维持相关基因:已报道POLG(DNA聚合酶γ)、TWNK(Twinkle)、SLC25A4(ANT1)、POLG2、RRM2B、RNASEH1、MGME1、DNA2、TK2、DGUOK等基因的突变1)5)。
多发性mtDNA缺失:nDNA突变通过损害mtDNA复制和修复导致多发性mtDNA缺失。
遗传方式:常染色体显性或常染色体隐性遗传。询问家族史很重要。
外眼肌选择性受累的原因在于,与骨骼肌相比,其线粒体含量更高、代谢需求更大,因此对氧化磷酸化障碍的脆弱性更高。
遗传方式因致病基因而异。mtDNA突变的散发案例为新发突变,遗传风险较低。nDNA突变案例表现为常染色体显性或隐性遗传,可见家族内发病。mtDNA突变也可能通过母系遗传传播。建议进行遗传咨询。
CPEO主要基于临床诊断,但各种检查对确诊和鉴别诊断很有帮助。在专科诊所,注意力可能集中在特定疾病上,从而忽略眼睑下垂或眼球运动障碍6)。
这是确诊的关键检查。
眼外肌肌电图检查显示,即使眼球不能运动,仍可见干扰波形,其振幅略低于正常肌肉但放电充分。这有助于与神经源性疾病的鉴别。
需要与CPEO鉴别的主要疾病如下所示。
| 疾病 | 鉴别要点 |
|---|---|
| 重症肌无力 | 有日内波动和易疲劳性。抗AChR抗体阳性 |
| 甲状腺眼病 | 眼外肌肥大。伴有眼球突出 |
| 强直性肌营养不良 | 以远端肌为主的肌萎缩。叩击性肌强直 |
重症肌无力是最重要的鉴别诊断,因为它会导致上睑下垂和眼球运动障碍。重症肌无力的特点是日间波动和易疲劳性,腾喜龙试验或冰袋试验可改善。CPEO的上睑下垂是非波动性的,这些试验不会改善。
CPEO尚无根治性治疗方法。对症治疗以维持生活质量(QOL)是治疗的核心。
为补充线粒体功能异常,可尝试使用以下药物。
提肌前徙术
适应症:提肌功能中等以上保留时。
方法:进行上睑提肌前徙术或切除术。经皮入路前徙固定腱膜,必要时加做Müller肌折叠术。
注意:CPEO中提肌功能进行性恶化,因此长期效果可能减弱。
额肌悬吊术
适应症:提上睑肌功能不良(小于4mm)。CPEO通常选择此术式。
方法:使用自体筋膜(阔筋膜、颞筋膜)、Gore-Tex®片、尼龙线、硅胶棒等将上眼睑连接到额肌。
注意:过度矫正会导致兔眼和角膜暴露,有引起暴露性角膜病变和角膜溃疡的风险。
必须由经验丰富的眼整形外科医生进行仔细的术前评估。如果Bell现象缺失,应保持欠矫。
CPEO是进展性疾病,术后提上睑肌功能可能逐渐恶化,导致眼睑下垂复发。尤其在儿童病例中,随着生长发育常需再次手术。额肌悬吊术使用的材料长期可能减弱牵引力。定期随访很重要。
CPEO的本质是由于mtDNA或nDNA突变导致的氧化磷酸化障碍。
线粒体拥有自己的DNA(mtDNA),编码氧化磷酸化所需的13种蛋白质。mtDNA的缺失或点突变会降低电子传递链酶的活性,导致ATP生成不足。与骨骼肌相比,眼外肌的线粒体含量更高,为维持抗疲劳性需要更大的代谢需求。这一特性被认为是CPEO中选择性累及眼外肌的原因之一。
异质性(heteroplasmy)是CPEO的重要病理概念。正常mtDNA和突变mtDNA共存于同一细胞内,当突变mtDNA的比例超过阈值(通常80%以上)时,线粒体功能就会发生障碍。
Visuttijai等人(2021)报道了MT-TN基因的两个新发点突变(m.5669G>A和m.5702delA)。单肌纤维分析显示,COX阴性纤维中的突变比例平均为93%,与COX正常纤维(32%和57%)相比有显著差异(P < 0.0001)。两例的COX功能障碍阈值均在80%以上2)。
Katayama Ueda等人(2025)在一例日本男性CPEO病例中鉴定出tRNAGlu基因的新发突变(m.14677T>C)。破碎红纤维(ragged red fiber)中的突变比例中位数为88.1%,显著高于非破碎红纤维(中位数17.1%)(P = 0.03)3)。
关于nDNA突变,POLG基因是CPEO最常见的核基因原因之一。POLG编码mtDNA复制所需的DNA聚合酶γ,其突变通过损害mtDNA复制导致多发性mtDNA缺失。
Liu等人(2023)报道了一名38岁女性,携带POLG基因已知突变c.2857C>T(p.R953C)和新发突变c.2391G>C(p.M797I)。她出现肢体无力和麻木,随后出现上睑下垂,肌肉活检显示破碎红纤维5)。
在儿童期发病的线粒体脑肌病中,5-氨基乙酰丙酸(5-ALA)与铁剂的联合治疗被认为可提高ATP生成,并已开始临床试验。然而,其在CPEO中的疗效尚不清楚。
KH176是一种线粒体靶向的氧化还原调节剂,可减少活性氧介导的细胞损伤。
一项评估KH176(100mg,每日两次)在CPEO患者中的安全性和有效性的II期临床试验已启动(NCT04604548)5)。
正在尝试使用安全载体导入正常基因。此外,利用异质性特性,通过寡核苷酸RNA抑制突变mtDNA的方法也有报道。
作为线粒体基因组操作技术,使用限制性内切酶、TALEN、ZFN和CRISPR选择性去除突变mtDNA的研究正在进行中1)。生殖系替代疗法(原核移植、卵母细胞纺锤体移植)也处于动物模型和临床试验阶段。
Fan等人(2021)在CPEO-plus综合征患者的肌肉MR波谱中检测到1-2ppm的双峰(提示乳酸积累)。在水肿肌肉中更为明显,表明其作为疾病监测生物标志物的潜力4)。