副肿瘤性

眼球阵挛-肌阵挛综合征
一目了然的要点
Section titled “一目了然的要点”1. 什么是视阵挛-肌阵挛综合征
Section titled “1. 什么是视阵挛-肌阵挛综合征”视阵挛-肌阵挛综合征(OMS)是一种罕见且异质性的神经综合征,由Marcel Kinsbourne于1962年首次报道,也称为Kinsbourne综合征或舞蹈眼综合征。
眼阵挛-肌阵挛综合征是一种自身免疫性疾病,主要症状包括眼阵挛、肌阵挛、小脑性共济失调、认知障碍以及行为和睡眠障碍。
流行病学
- 年发病率:每500万人中1例
- 患病率:全球人口中约每100万人中1例
- 儿童发病率:0.18/100万人/年,平均发病年龄1.5岁9)
- 儿童典型发病年龄:1~3岁(12~36个月)
- 成人发病年龄范围广泛,从青春期至80多岁
- 无明显家族性、遗传性、性别或种族倾向
年发病率为500万分之一,患病率为100万分之一,是一种极为罕见的疾病。儿童和成人均可发病,但成人发病估计更为罕见4)。
2. 主要症状与临床所见
Section titled “2. 主要症状与临床所见”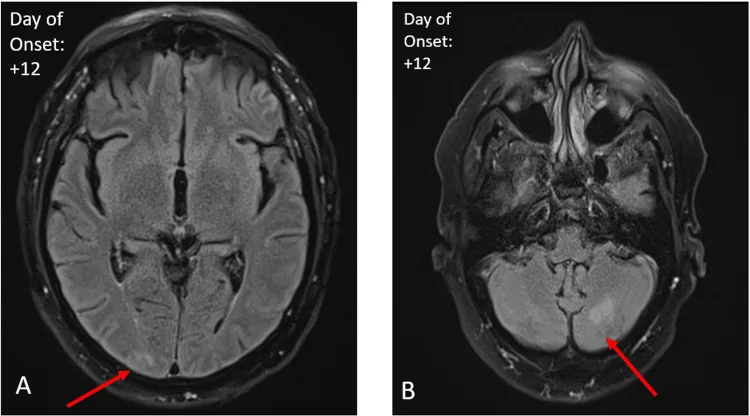
儿童和成人的首发症状不同。
儿童的主要症状
- 急性/亚急性共济失调和跌倒:表现为姿势或身体活动障碍,且进展迅速。
- 易激惹和睡眠障碍:神经症状伴随行为改变,早期即可出现。
- 发育倒退:包括性格改变、言语或语言能力丧失等倒退表现。
成人的主要症状
- 眩晕和平衡感丧失:最常见的主诉。
- 前驱症状:可能先出现恶心、呕吐、睡眠障碍、情绪障碍、震颤等4)。
OMS的诊断特征包括4项:①眼阵挛,②共济失调和/或肌阵挛,③行为改变或睡眠障碍,④副肿瘤性时诊断为神经母细胞瘤。
眼阵挛
眼阵挛是扫视嵌入(saccadic intrusion)的一种,表现为无扫视间隔的多方向、不规则、自发的共轭扫视爆发。它干扰固视,表现为全方向、高频、高振幅的无序眼球运动。初期评估时可能不明显,有时在运动症状出现数周后才显现。
肌阵挛
肌阵挛性质多样,可影响全身任何部位。情绪压力或尝试运动时加重。在COVID-19相关病例中,已报道有全身性刺激敏感性肌阵挛和动作性肌阵挛1)。
小脑性共济失调(ataxia)
表现为步态障碍、躯干共济失调、宽基步态。
其他
可能伴有构音障碍(dysarthria)、四肢及下颌震颤、声音震颤1, 5, 8)。
下表展示眼阵挛与类似眼球运动异常的鉴别要点。
| 表现 | 慢相 | 方向 | 特征 |
|---|---|---|---|
| 眼震 | 有 | 固定方向 | 慢相+快相 |
| 眼球扑动 | 无 | 仅水平 | 纯水平方向 |
| 方波跳动 | 无 | 水平 | 有正常扫视间隔 |
| 眼阵挛 | 无 | 多方向 | 全方向的无序眼球运动 |
3. 原因与风险因素
Section titled “3. 原因与风险因素”确切病因不明,但感染性或副肿瘤性过程导致的自身免疫性炎症是主要假说。涉及细胞和体液免疫机制,大多数患者对已知的抗神经抗体呈血清阴性。
病因大致分为三类。
感染后/感染伴随性
毒性/代谢性
苯妥英钠过量、高渗性非酮症糖尿病昏迷、可卡因中毒等也可能诱发。
4. 诊断与检查方法
Section titled “4. 诊断与检查方法”OMS是基于临床发现的临床诊断,没有确定的检查或生物标志物。诊断延迟很常见,从症状出现到诊断的中位时间为11周4)。
与眼震、眼球扑动、矩形波律动的鉴别请参考“临床表现”一节。还需与前庭神经炎、良性阵发性位置性眩晕、脑卒中、脑肿瘤、自身免疫性脑炎、多发性硬化症、眼球运动失用症(oculomotor apraxia)进行鉴别4, 7)。眼球运动失用症是扫视运动受损的疾病,与眼阵挛不同,在转向新目标时表现出特征性的头部代偿运动,以此区分。
主要诊断检查
Section titled “主要诊断检查”脑影像学检查(MRI)
目的是排除原发性CNS疾病。许多OMS病例的MRI正常。部分病例报告有T2-FLAIR高信号(小脑、颞叶)3, 2),慢性期可能出现小脑萎缩9)。
脑脊液(CSF)分析
用于排除CNS疾病。多数病例正常至轻度异常。部分病例可见寡克隆带阳性、蛋白轻度升高2, 4)。CSF中CD19+ B细胞扩增(最高29%)作为疾病活动性生物标志物候选正在研究中4)。
恶性肿瘤筛查
- 儿童:所有病例考虑评估神经母细胞瘤。
- 成人:进行CT、PET-CT检查7, 8)。若未发现肿瘤,则每6个月随访一次,最长4年2)。
抗神经抗体 panel
检测anti-Ri(ANNA-2)、anti-Hu、anti-Yo、anti-Ma、anti-NMDA受体等。但许多患者抗体阴性。
PNS-Care评分系统(2021年国际专家组)考虑临床表型、抗体类型、有无癌症及随访时间,分为definite(>8分)、probable(6-7分)、possible(4-5分)7)。
5. 标准治疗方法
Section titled “5. 标准治疗方法”治疗的主要手段是免疫调节疗法。对于副肿瘤性病例,肿瘤靶向治疗必不可少,需同时进行肿瘤治疗和免疫调节疗法。诊断延迟与神经、心理和行为预后恶化相关,因此早期治疗至关重要。
免疫调节疗法
Section titled “免疫调节疗法”肾上腺皮质激素(corticosteroids)
甲泼尼龙静脉冲击疗法(1g/日×3~5天)是标准方案2, 6, 7)。
ACTH(促肾上腺皮质激素)
被定位为儿童和成人的标准治疗。
IVIG(静脉注射免疫球蛋白)
总剂量2g/kg,分3~5天给药是常见做法1, 6)。有报告显示COVID-19相关病例在1周后开始改善、4周后完全恢复1),West Nile病毒相关病例在给药5天后改善3)。
利妥昔单抗(rituximab)
用于类固醇和IVIG治疗不充分的病例。有报道称,在卵巢畸胎瘤相关OMS中,给予1g×2次后,在第6个月和第12个月追加给药,30个月无复发6)。提示多药联合免疫抑制可能比单药更有效。
其他免疫抑制剂
可使用硫唑嘌呤、吗替麦考酚酯8, 7)、环磷酰胺等。
减轻肌阵挛可使用以下药物。
- 氯硝西泮:从睡前0.5mg开始1)
- 丙戊酸钠:1000mg/日1)
- 左乙拉西坦:从500mg×2次/日开始逐渐加量1)
副肿瘤性OMS的治疗
Section titled “副肿瘤性OMS的治疗”肿瘤靶向治疗(手术、化疗、放疗)是不可或缺的。肿瘤切除不一定能改善神经症状,有报告称切除后1个月发生OMS6)。小细胞肺癌采用卡铂+依托泊苷化疗8),乳腺癌采用新辅助化疗+利妥昔单抗有改善报告7)。
6. 病理生理学与详细发病机制
Section titled “6. 病理生理学与详细发病机制”OMS的发病机制主要有两种理论:脑干假说和小脑假说。
脑干假说
小脑假说
小脑尾侧顶核的去抑制:功能异常的浦肯野细胞无法抑制顶核。
发病机制:室顶核加强对全向暂停神经元的抑制→扫视爆发神经元自由振动→眼阵挛。支持性发现包括小脑蚓部胶质增生和炎症、急性期小脑血流增加、慢性期低灌注和萎缩9)。
自身免疫性炎症是强有力的假说,细胞免疫和体液免疫均参与其中。
- 脑脊液中CD19+ B细胞扩增(最高达29%)与神经学严重程度相关4)
- 肿瘤微环境中的免疫反应引发对神经抗原的交叉反应7)
- anti-Ri抗体与Nova-1、Nova-2(中枢神经系统中广泛表达的RNA结合蛋白)发生交叉反应7)
- 仅约25%的患者可检测到onconeuronal抗体2)
眼阵挛本身无论是否治疗通常都会消失。但缓解后可能复发,眼阵挛消失后平滑追踪眼球运动异常仍长期存在。60-80%的患者残留行为障碍和精神运动障碍,长期神经学预后往往不良。
7. 最新研究与未来展望(研究阶段报告)
Section titled “7. 最新研究与未来展望(研究阶段报告)”COVID-19相关OMS的认识
Section titled “COVID-19相关OMS的认识”Emamikhah等人(2021)的7例系列研究中,COVID-19呼吸道症状出现后2天至3周发生OMS,经IVIG治疗后改善1)。成人综述中约1/3有流感样前驱症状,40%出现IgG指数升高或寡克隆带。
COVID-19后的OMS作为一种不伴脑病的独立免疫性副感染综合征,其认识正在加深。
西尼罗河病毒相关OMS的MRI表现
Section titled “西尼罗河病毒相关OMS的MRI表现”Yang等人(2024)报告了初始MRI正常→10天后出现T2-FLAIR高信号→4个月后完全消失的病程3)。提示症状出现与MRI异常检测之间可能存在特定的时间窗。
Anti-Ri谱系的重新定义
Section titled “Anti-Ri谱系的重新定义”传统上被认为是OMS+共济失调的anti-Ri综合征,正被重新定义为更复杂的多系统疾病。
Freydl等人(2024)提出步态障碍+眼球运动障碍+下颌肌张力障碍三联征作为特征性综合征2)。症状诊断后4~6个月内,约80%的PNS患者被诊断出肿瘤。
CSF B细胞生物标志物
Section titled “CSF B细胞生物标志物”Pranzatelli研究(Lawrence 2025引用)提出,CSF中CD19+ B细胞扩增可作为OMS疾病活动性的候选生物标志物4)。尚未达到标准化。
迟发性OMS与免疫检查点抑制剂
Section titled “迟发性OMS与免疫检查点抑制剂”肿瘤切除后因抗原暴露引发免疫反应而导致的迟发性OMS已被认识6)。此外,有报道称免疫检查点抑制剂作为免疫相关不良事件可能诱发或加重OMS及脑干脑炎5),对于PD-L1高表达肿瘤,有时需要判断是否避免使用该药物。
8. 参考文献
Section titled “8. 参考文献”- Emamikhah M, Babadi M, Mehrabani M, et al. Opsoclonus-myoclonus syndrome, a post-infectious neurologic complication of COVID-19: case series and review of literature. J Neurovirol. 2021;27(1):26-34.
- Freydl E, Tinchon A, Blauensteiner K, Oberndorfer S. Anti-Ri paraneoplastic neurological syndrome presenting with bilateral cranial nerve VI palsy and jaw dystonia. Wien Med Wochenschr. 2024;174(1-2):16-21.
- Yang JC, Zekavaty S, Rossi RD, Mahmoud SY. Unique Magnetic Resonance Imaging Findings in Opsoclonus-Myoclonus Syndrome Secondary to the West Nile Virus. Cureus. 2024;16(8):e67932.
- Lawrence JS. Challenges in Diagnosing Opsoclonus-Myoclonus Syndrome in Adults. Cureus. 2025;17(5):e84780.
- Costa PA, Costa BMLA, Rozenbaum G, Barreto-Coelho P. Anti-Ma paraneoplastic opsoclonus-myoclonus syndrome. BMJ Case Rep. 2021;14(5):e243136.
- Jones AA, Chen T. Delayed Opsoclonus-Myoclonus Syndrome After Ovarian Teratoma Resection. J Neuro-Ophthalmol. 2022;42(3):e450-e451.
- Soares R, Mittapalli A, Ramakrishnan M, Farooq U. Breast Cancer Presenting As Onconeural Antibody Negative Opsoclonus-Myoclonus Syndrome. Cureus. 2022;14(8):e28417.
- Moreira I, Vilas-Boas I, Cassiano Neves M. Paraneoplastic Opsoclonus-Myoclonus Syndrome as a Rare Presentation of Small-Cell Lung Cancer. Cureus. 2022;14(11):e32066.
- Takenaka J, Hirata K, Watanabe S, Shiraishi H, Kudo K. Neuroblastoma-related severe hypoperfusion in the cerebellum of an infant: A case of opsoclonus-myoclonus syndrome. Asia Ocean J Nucl Med Biol. 2023;11(1):93-96.
