副腫瘤性

眼球震顫-肌陣攣症候群
一目瞭然的要點
Section titled “一目瞭然的要點”1. 什麼是視性眼陣攣-肌陣攣症候群
Section titled “1. 什麼是視性眼陣攣-肌陣攣症候群”視性眼陣攣-肌陣攣症候群(Opsoclonus-Myoclonus Syndrome; OMS)是1962年由Marcel Kinsbourne首次報告的一種罕見且異質性的神經症候群,也稱為Kinsbourne症候群或跳舞眼症候群。
視性眼陣攣、肌陣攣、小腦性共濟失調、認知障礙、行為及睡眠障礙為主要症狀的自體免疫性疾病。
流行病學
- 年發生率:每500萬人中有1人
- 盛行率:約每100萬全球人口中有1人
- 兒童發生率為0.18/百萬人/年,平均發病年齡1.5歲9)
- 兒童典型發病年齡:1~3歲(12~36個月)
- 成人則從青春期至80多歲各年齡層皆可能發病
- 無明顯家族性、遺傳性、性別或種族差異
年發生率為每500萬人1例,盛行率為每100萬人1例,是極為罕見的疾病。雖然兒童和成人皆可能發病,但成人發病被認為更為罕見4)。
2. 主要症狀與臨床表現
Section titled “2. 主要症狀與臨床表現”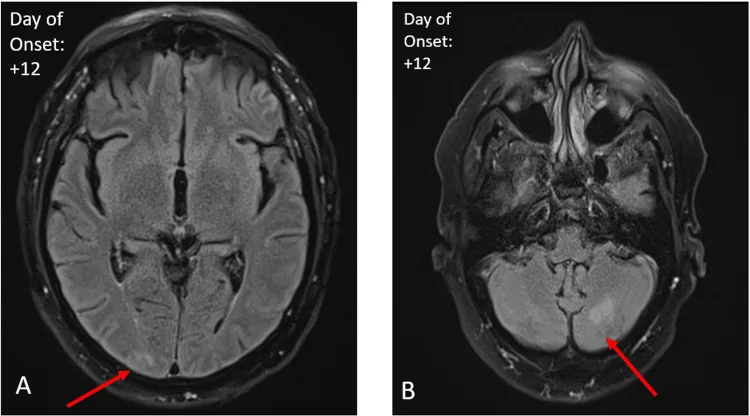
兒童與成人的初始症狀不同。
兒童的主要症狀
- 急性/亞急性失調與跌倒:出現姿勢或身體活動障礙,且快速進展。
- 易怒與睡眠障礙:神經症狀伴隨行為改變,早期即出現。
- 發展退化:包括性格改變、語言能力喪失等退化現象。
成人的主要症狀
- 眩暈與平衡感喪失:最常見的主訴。
- 前驅症狀:可能先出現噁心、嘔吐、睡眠障礙、情緒障礙、顫抖等4)。
OMS的診斷特徵包括四項:①眼球陣攣、②失調及/或肌陣攣、③行為改變或睡眠障礙、④若為副腫瘤性,則診斷神經母細胞瘤。
眼球陣攣
為一種跳視嵌入(saccadic intrusion),是無跳視間隔、多方向、不規則、自發性的共同性跳視群發。它干擾固視,表現為全方向、高頻率、高振幅的混亂眼球運動。初期評估時可能未被發現,有時在運動症狀出現後數週才顯現。
肌陣攣
具有多樣性質,影響全身各部位。情緒壓力或嘗試運動時會惡化。在COVID-19相關病例中,已報告有全身性刺激敏感性肌陣攣和動作性肌陣攣1)。
小腦性共濟失調(ataxia)
表現為步態障礙、軀幹共濟失調、寬基步態。
其他
可能伴隨構音障礙(dysarthria)、四肢及下巴震顫、聲音震顫1, 5, 8)。
下表顯示視性眼陣攣與類似眼球運動異常的鑑別要點。
| 所見 | 慢速相 | 方向 | 特徵 |
|---|---|---|---|
| 眼震 | 有 | 固定方向 | 慢速相+快速相 |
| 眼球撲動 | 無 | 僅水平方向 | 純粹水平方向 |
| 方波震顫 | 無 | 水平 | 有正常掃視間隔 |
| 眼球陣攣 | 無 | 多方向 | 全方向無序的眼球運動 |
眼震有慢相(緩慢運動),但眼球陣攣沒有。此外,眼球撲動也沒有慢相,僅為水平方向的快速眼球運動,而眼球陣攣則涉及多個方向,可藉此區分。矩形波律動為快速掃視運動,但保持正常掃視間隔,與之不同。
3. 原因與風險因素
Section titled “3. 原因與風險因素”確切病因不明,但感染性或副腫瘤過程引起的自體免疫性炎症是主要假說。涉及細胞及體液免疫機制,大多數患者對已知抗神經抗體呈血清陰性。
病因大致可分為三大類。
感染後/感染相關性
毒性與代謝性
苯妥英過量給藥、高滲透壓非酮症糖尿病昏迷、古柯鹼中毒等也可能引發。
4. 診斷與檢查方法
Section titled “4. 診斷與檢查方法”OMS是基於臨床表現的臨床診斷,沒有確定的檢查或生物標記。診斷延遲很常見,從症狀出現到診斷的中位時間為11週4)。
與眼震、眼球撲動、矩形波律動的鑑別請參閱「臨床表現」一節。鑑別診斷還包括前庭神經炎、良性陣發性姿勢性眩暈、腦中風、腦腫瘤、自體免疫性腦炎、多發性硬化症、眼球運動失用症(oculomotor apraxia)4, 7)。眼球運動失用症是影響掃視運動的疾病,與眼球陣攣不同,其特點是在轉換視線至新目標時出現特徵性的頭部代償運動。
主要診斷檢查
Section titled “主要診斷檢查”腦部影像檢查(MRI)
目的是排除原發性中樞神經系統疾病。許多OMS病例的MRI正常。部分病例報告有小腦或顳葉的T2-FLAIR高信號3, 2),慢性期可能出現小腦萎縮9)。
腦脊髓液(CSF)分析
用於排除CNS疾病。多數病例正常至輕度異常。部分病例可見oligoclonal bands陽性及蛋白質輕度升高2, 4)。CSF中CD19+ B細胞擴增(最高29%)正被研究作為疾病活動性的生物標誌物候選4)。
惡性腫瘤篩查
- 兒童:所有病例應考慮評估神經母細胞瘤。
- 成人:進行CT、PET-CT檢查7, 8)。若未發現腫瘤,則每6個月進行一次追蹤,最長達4年2)。
抗神經抗體檢測
檢測anti-Ri(ANNA-2)、anti-Hu、anti-Yo、anti-Ma、anti-NMDA受體等。但許多患者抗體為陰性。
PNS-Care評分系統(2021年國際專家小組)考量臨床表現型、抗體類型、有無癌症及追蹤時間,分為definite(>8分)、probable(6-7分)、possible(4-5分)7)。
5. 標準治療方法
Section titled “5. 標準治療方法”治療主軸為免疫調節療法。若為副腫瘤性,則腫瘤標靶治療不可或缺,需同時進行腫瘤治療與免疫調節療法。診斷延遲與神經、心理及行為預後惡化相關,因此早期治療至關重要。
免疫調節療法
Section titled “免疫調節療法”腎上腺皮質類固醇(corticosteroids)
methylprednisolone靜脈注射脈衝療法(1g/日×3〜5天)為標準療程2, 6, 7)。
ACTH(促腎上腺皮質激素)
被定位為兒童與成人的標準治療。
IVIG(靜脈注射免疫球蛋白)
總劑量2g/kg,分3〜5天給藥為常見做法1, 6)。有報告指出COVID-19相關病例在治療後1週開始改善、4週完全恢復1);West Nile病毒相關病例在5天給藥後改善3)。
利妥昔單抗(rituximab)
用於類固醇及IVIG治療效果不佳的病例。在卵巢畸胎瘤相關OMS中,有報告指出給予1g×2次後,於6個月及12個月追加給藥,30個月無復發6)。多種藥物聯合免疫抑制可能比單一藥物更有效。
其他免疫抑制藥物
可使用硫唑嘌呤、黴酚酸酯8, 7)、環磷醯胺等。
減輕肌陣攣可使用以下藥物:
- 氯硝西泮:睡前0.5mg開始1)
- 丙戊酸鈉:1000mg/日1)
- 左乙拉西坦:從500mg×2次/天開始逐漸增加1)
副腫瘤性OMS的治療
Section titled “副腫瘤性OMS的治療”腫瘤標靶治療(手術、化學治療、放射治療)是不可或缺的。腫瘤切除不一定能改善神經學症狀,有報告指出切除後1個月才發生OMS6)。小細胞肺癌患者使用卡鉑+依託泊苷化學治療8),乳癌患者使用新輔助化學治療+利妥昔單抗後有改善的報告7)。
治療期間因病因、嚴重度和治療反應而異。有些病例在IVIG治療後數週至數個月內改善3, 4),但為了預防復發,可能需要長期免疫抑制治療,如rituximab6)。副腫瘤性OMS通常比特發性更嚴重且更具治療抵抗性8)。
6. 病理生理學・詳細發病機制
Section titled “6. 病理生理學・詳細發病機制”OMS的發病機制有兩個主要理論:腦幹說和小腦說。
腦幹說
小腦說
小腦尾側頂核的去抑制:功能異常的浦肯野細胞無法抑制頂核。
發病機制:室頂核加強對全向暫停神經元的抑制→跳視爆發神經元自由振盪→眼陣攣。支持性發現包括小腦蚓部神經膠質增生與發炎、急性期小腦血流增加、慢性期低灌流與萎縮9)。
自體免疫性發炎是主要假說,細胞免疫與體液免疫皆參與其中。
- 腦脊髓液中CD19+ B細胞擴增(最高29%)與神經學嚴重度相關4)
- 腫瘤微環境中的免疫反應引發對神經抗原的交叉反應7)
- anti-Ri抗體與Nova-1、Nova-2(中樞神經系統中廣泛表現的RNA結合蛋白)產生交叉反應7)
- 腫瘤神經抗體僅在約25%的患者中檢測到2)
眼球震顫本身通常會自行消失,無論是否接受治療。然而,緩解後仍可能復發,且在眼球震顫消失後,追蹤眼球運動(smooth pursuit)異常可能長期存在。60%至80%的患者會殘留行為障礙及精神運動障礙,長期神經學預後通常不佳。
7. 最新研究與未來展望(研究階段報告)
Section titled “7. 最新研究與未來展望(研究階段報告)”COVID-19相關OMS的認識
Section titled “COVID-19相關OMS的認識”Emamikhah等人(2021)的7例系列報告中,COVID-19呼吸道症狀後2天至3週出現OMS,經IVIG治療後改善1)。成人回顧中約1/3有類流感前驅症狀,40%有IgG指數升高或寡克隆帶。
COVID-19後的OMS被認為是一種不伴隨腦病的獨立免疫性副感染症候群。
西尼羅病毒相關OMS的MRI發現
Section titled “西尼羅病毒相關OMS的MRI發現”Yang等人(2024)報告了初始MRI正常→10天後出現T2-FLAIR高信號→4個月後完全消失的過程3)。這提示症狀出現與MRI異常檢測之間可能存在特定的時間窗口。
Anti-Ri譜系的重新定義
Section titled “Anti-Ri譜系的重新定義”傳統上被認為是OMS加上失調的anti-Ri症候群,正被重新定義為更複雜的多系統疾病。
Freydl等人(2024)提出步態障礙、眼球運動障礙和下巴張力不全的三聯徵作為特徵性症候群2)。據報導,約80%的PNS患者在症狀診斷後4至6個月內被診斷出腫瘤。
CSF B細胞生物標記
Section titled “CSF B細胞生物標記”Pranzatelli研究(引用於Lawrence 2025)提出,CSF中的CD19+ B細胞擴增可作為OMS疾病活動性的候選生物標記4),但目前尚未標準化。
遲發性OMS與免疫檢查點抑制劑
Section titled “遲發性OMS與免疫檢查點抑制劑”腫瘤切除後因抗原暴露引發免疫反應而導致的遲發性OMS已被認識6)。此外,免疫檢查點抑制劑可能作為免疫相關不良反應引發或惡化OMS及腦幹腦炎5),因此在PD-L1高表達腫瘤中,有時需要考慮避免使用該類藥物。
8. 參考文獻
Section titled “8. 參考文獻”- Emamikhah M, Babadi M, Mehrabani M, et al. Opsoclonus-myoclonus syndrome, a post-infectious neurologic complication of COVID-19: case series and review of literature. J Neurovirol. 2021;27(1):26-34.
- Freydl E, Tinchon A, Blauensteiner K, Oberndorfer S. Anti-Ri paraneoplastic neurological syndrome presenting with bilateral cranial nerve VI palsy and jaw dystonia. Wien Med Wochenschr. 2024;174(1-2):16-21.
- Yang JC, Zekavaty S, Rossi RD, Mahmoud SY. Unique Magnetic Resonance Imaging Findings in Opsoclonus-Myoclonus Syndrome Secondary to the West Nile Virus. Cureus. 2024;16(8):e67932.
- Lawrence JS. Challenges in Diagnosing Opsoclonus-Myoclonus Syndrome in Adults. Cureus. 2025;17(5):e84780.
- Costa PA, Costa BMLA, Rozenbaum G, Barreto-Coelho P. Anti-Ma paraneoplastic opsoclonus-myoclonus syndrome. BMJ Case Rep. 2021;14(5):e243136.
- Jones AA, Chen T. Delayed Opsoclonus-Myoclonus Syndrome After Ovarian Teratoma Resection. J Neuro-Ophthalmol. 2022;42(3):e450-e451.
- Soares R, Mittapalli A, Ramakrishnan M, Farooq U. Breast Cancer Presenting As Onconeural Antibody Negative Opsoclonus-Myoclonus Syndrome. Cureus. 2022;14(8):e28417.
- Moreira I, Vilas-Boas I, Cassiano Neves M. Paraneoplastic Opsoclonus-Myoclonus Syndrome as a Rare Presentation of Small-Cell Lung Cancer. Cureus. 2022;14(11):e32066.
- Takenaka J, Hirata K, Watanabe S, Shiraishi H, Kudo K. Neuroblastoma-related severe hypoperfusion in the cerebellum of an infant: A case of opsoclonus-myoclonus syndrome. Asia Ocean J Nucl Med Biol. 2023;11(1):93-96.
