กลุ่มอาการออปโซโคลนัส-ไมโอโคลนัส (OMS ) เป็นกลุ่มอาการทางภูมิคุ้มกันตนเองทางระบบประสาทที่พบได้ยากมาก โดยพบประมาณ 1 รายต่อประชากร 5 ล้านคนต่อปี
ออปโซโคลนัสคือการเคลื่อนไหวของลูกตาที่ไม่เป็นระเบียบหลายทิศทางโดยไม่มีช่วงระหว่างการกลอกตา ซึ่งแตกต่างจากอาตา
ในเด็กประมาณ 50% มีนิวโรบลาสโตมา ซ่อนอยู่ ส่วนในผู้ใหญ่ มะเร็งปอดชนิดเซลล์เล็กและมะเร็งเต้านมเป็นเนื้องอกที่เกี่ยวข้องหลัก
ไม่มีการตรวจหรือตัวบ่งชี้ทางชีวภาพ ที่แน่ชัดสำหรับการวินิจฉัย โดยระยะเวลาตั้งแต่อาการเริ่มแรกจนถึงการวินิจฉัยเฉลี่ย 11 สัปดาห์
การรักษาหลักคือการปรับภูมิคุ้มกันด้วย IVI G, สเตียรอยด์ พัลส์ และริทูซิแมบ ส่วนในกรณีที่เกี่ยวข้องกับเนื้องอก การรักษาที่จำเพาะต่อเนื้องอกเป็นสิ่งจำเป็น
การวินิจฉัยที่ล่าช้าสัมพันธ์กับผลลัพธ์ทางระบบประสาทและพฤติกรรมที่แย่ลง โดยผู้ป่วย 60-80% มีความผิดปกติทางพฤติกรรมและจิตใจที่คงอยู่ระยะยาว
กลุ่มอาการออปโซโคลนัส-ไมโอโคลนัส (Opsoclonus-Myoclonus Syndrome; OMS ) เป็นกลุ่มอาการทางระบบประสาทที่พบได้ยากและมีความหลากหลาย ซึ่ง Marcel Kinsbourne รายงานครั้งแรกในปี 1962 เรียกอีกชื่อว่า Kinsbourne syndrome หรือ dancing eyes syndrome
เป็นโรคภูมิคุ้มกันทำลายตนเองที่มีอาการหลัก ได้แก่ อาตา กระตุก (opsoclonus) กล้ามเนื้อกระตุก (myoclonus) การทำงานของสมองน้อยผิดปกติ (cerebellar ataxia) ความบกพร่องทางสติปัญญา และความผิดปกติทางพฤติกรรมและการนอนหลับ
ระบาดวิทยา
อุบัติการณ์รายปี: 1 ใน 5 ล้านคน
ความชุก: ประมาณ 1 ใน 1 ล้านคนของประชากรโลก
ในเด็ก อุบัติการณ์ 0.18/1 ล้านคนต่อปี อายุเฉลี่ยที่เริ่มป่วย 1.5 ปี9)
อายุที่เริ่มป่วยโดยทั่วไปในเด็ก: 1–3 ปี (12–36 เดือน)
ในผู้ใหญ่ เริ่มป่วยได้ตั้งแต่วัยรุ่นจนถึงอายุ 80 ปี
ไม่มีความชัดเจนเกี่ยวกับความสัมพันธ์ทางครอบครัว พันธุกรรม เพศ หรือเชื้อชาติ
Q
กลุ่มอาการออปโซโคลนัส-ไมโอโคลนัสเป็นโรคที่พบได้ยากเพียงใด?
A
เป็นโรคที่พบได้ยากมาก โดยมีอัตราการเกิดใหม่ต่อปี 1 รายต่อประชากร 5 ล้านคน และความชุก 1 รายต่อประชากร 1 ล้านคน โรคนี้เกิดได้ทั้งในเด็กและผู้ใหญ่ แต่ในผู้ใหญ่พบได้น้อยกว่า4)
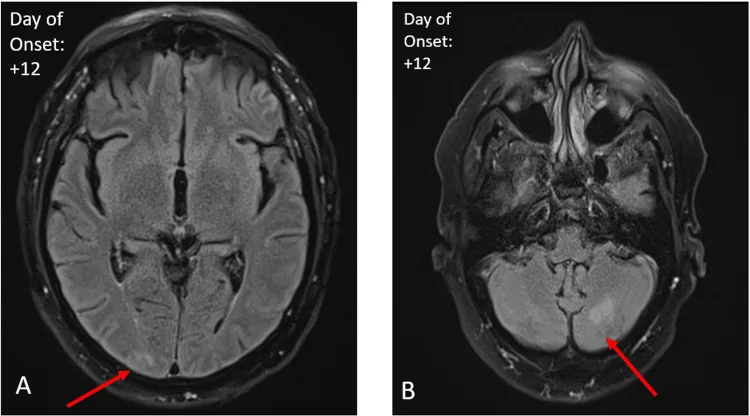
ภาพ MRI สมองของกลุ่มอาการออปโซโคลนัส-ไมโอโคลนัส Yang JC, et al. Unique Magnetic Resonance Imaging Findings in Opsoclonus-Myoclonus Syndrome Secondary to the West Nile Virus. Cureus. 2024. Figure 2. PM
CI D: PMC11426305. License: CC BY.
ภาพ MRI ด้วยเทคนิค FLAIR (Fluid Attenuated Inversion Recovery) ลูกศรในภาพ A และ B แสดงสัญญาณผิดปกติ ซึ่งสอดคล้องกับรอยโรคในสมองที่กล่าวถึงในหัวข้อ “2. อาการหลักและอาการแสดงทางคลินิก”
อาการเริ่มแรกในเด็กและผู้ใหญ่แตกต่างกัน
อาการหลักในเด็ก
การสูญเสียการทรงตัวและการล้มแบบเฉียบพลัน/กึ่งเฉียบพลัน : แสดงความผิดปกติของท่าทางและการเคลื่อนไหวร่างกาย ซึ่งดำเนินไปอย่างรวดเร็วอาการหงุดหงิดง่ายและความผิดปกติของการนอนหลับ : การเปลี่ยนแปลงทางพฤติกรรมปรากฏขึ้นตั้งแต่ระยะแรกพร้อมกับอาการทางระบบประสาทการถดถอยของพัฒนาการ : พบการถดถอยรวมถึงการเปลี่ยนแปลงบุคลิกภาพและการสูญเสียการพูดหรือภาษา
อาการหลักในผู้ใหญ่
อาการเวียนศีรษะและการสูญเสียการทรงตัว : เป็นอาการนำที่พบบ่อยที่สุดอาการนำ : อาจมีอาการคลื่นไส้ อาเจียน ความผิดปกติของการนอนหลับ ความผิดปกติทางอารมณ์ และอาการสั่นนำมาก่อน4)
ลักษณะเฉพาะทางวินิจฉัยของ OMS มี 4 ข้อ: ① ภาวะตากระตุก ผิดปกติ (opsoclonus) ② การสูญเสียการทรงตัวและ/หรืออาการกล้ามเนื้อกระตุก (myoclonus) ③ การเปลี่ยนแปลงทางพฤติกรรมหรือความผิดปกติของการนอนหลับ ④ ในกรณีที่เป็น paraneoplastic จะมีการวินิจฉัย neuroblastoma
ออปโซโคลนัส
เป็นชนิดหนึ่งของ saccadic intrusion คือการเกิด saccade ร่วมกันหลายทิศทาง ไม่สม่ำเสมอ และเกิดขึ้นเอง โดยไม่มีช่วงว่างระหว่าง saccade รบกวนการจ้องมอง และสังเกตได้เป็นการเคลื่อนไหวตาที่ไม่เป็นระเบียบ ความถี่สูง แอมพลิจูดสูงในทุกทิศทาง อาจไม่พบในการประเมินครั้งแรก และอาจปรากฏช้ากว่าอาการทางการเคลื่อนไหวหลายสัปดาห์
ไมโอโคลนัส
มีลักษณะหลากหลาย ส่งผลต่อทุกส่วนของร่างกาย อาการแย่ลงเมื่อมีความเครียดทางอารมณ์หรือพยายามเคลื่อนไหว ในผู้ป่วยที่เกี่ยวข้องกับ COVID-19 มีรายงานไมโอโคลนัสที่ไวต่อสิ่งกระตุ้นทั่วร่างกายและไมโอโคลนัสขณะเคลื่อนไหว1)
ภาวะเสียการทรงตัวจากสมองน้อย (ataxia)
แสดงอาการเดินลำบาก เสียการทรงตัวของลำตัว และเดินแยกขากว้าง
อื่นๆ
อาจมีอาการพูดไม่ชัด (dysarthria) อาการสั่นของแขนขาและขากรรไกร และอาการสั่นของเสียงร่วมด้วย1, 5, 8)
ตารางด้านล่างแสดงความแตกต่างระหว่าง opsoclonus และความผิดปกติของการเคลื่อนไหวของลูกตาที่คล้ายคลึงกัน
ลักษณะ ระยะช้า ทิศทาง ลักษณะเด่น อาตา มี ทิศทางคงที่ ระยะช้า + ระยะเร็ว การกระตุกของลูกตา ไม่มี แนวนอนเท่านั้น แนวนอนล้วน การเคลื่อนไหวแบบคลื่นสี่เหลี่ยม ไม่มี แนวนอน มีระยะห่างของแซคเคดปกติ ออปโซโคลนัส ไม่มี หลายทิศทาง การเคลื่อนไหวของลูกตาที่ไม่เป็นระเบียบในทุกทิศทาง
Q
จะแยกออปโซโคลนัสออกจากอาตาได้อย่างไร?
A
อาตา มีระยะช้า (การเคลื่อนไหวช้า) แต่ออปโซโคลนัสไม่มี นอกจากนี้ อาการกระตุกของลูกตา (ocular flutter) ก็ไม่มีระยะช้าเช่นกัน แต่เป็นการเคลื่อนไหวของลูกตาอย่างรวดเร็วในแนวราบเท่านั้น ในขณะที่ออปโซโคลนัสเกิดขึ้นในหลายทิศทาง ซึ่งเป็นจุดที่แตกต่างกัน การเคลื่อนไหวแบบคลื่นสี่เหลี่ยม (square-wave jerks) เป็นการเคลื่อนไหวแบบแซคเคดที่รวดเร็ว แต่แตกต่างตรงที่ยังคงรักษาช่วงเวลาของแซคเคดปกติไว้
ไม่ทราบสาเหตุที่แน่ชัด แต่สมมติฐานที่ได้รับการยอมรับคือการอักเสบจากภูมิต้านทานตนเองที่เกิดจากกระบวนการติดเชื้อหรือพารานีโอพลาสติก กลไกภูมิคุ้มกันแบบเซลล์และแบบฮิวโมรอลมีส่วนเกี่ยวข้อง และผู้ป่วยส่วนใหญ่มีผลลบต่อซีรั่มสำหรับแอนติบอดีต่อระบบประสาทที่รู้จัก
สาเหตุแบ่งออกเป็น 3 ประเภทใหญ่
พารานีโอพลาสติก
เด็ก : ผู้ป่วย OMS ประมาณ 50% มีนิวโรบลาสโตมา ที่ซ่อนอยู่ เด็กที่มีนิวโรบลาสโตมา ประมาณ 2% จะเกิด OMS
ผู้ใหญ่ : 20–40% ของผู้ป่วย OMS เป็นพารานีโอพลาสติก มะเร็งปอดชนิดเซลล์เล็ก (SCLC) พบบ่อยที่สุด รองลงมาคือมะเร็งเต้านมชนิดอะดีโนคาร์ซิโนมา8) ในผู้หญิงอายุต่ำกว่า 30 ปี เนื้องอกรังไข่ชนิดเทอราโตมามีความเกี่ยวข้อง6)
แอนติบอดีที่เกี่ยวข้อง : anti-Ri (ANNA-2) เป็นแบบฉบับมากที่สุด2) anti-Hu, anti-Ma เป็นต้น นอกจากนี้ยังมี OMS แบบพารานีโอพลาสติกที่ตรวจไม่พบแอนติบอดี7)
หลังการติดเชื้อ/ร่วมกับการติดเชื้อ
เชื้อก่อโรคหลักที่เกี่ยวข้อง : โรคไลม์ , EB V, HIV (กลุ่มอาการฟื้นฟูภูมิคุ้มกัน), Mycoplasma pneumoniae, โรตาไวรัส
ที่เกี่ยวข้องกับ COVID-19 : เกิดอาการ 2 วันถึง 3 สัปดาห์หลังจากมีอาการทางระบบหายใจ1)
ที่เกี่ยวข้องกับไวรัสเวสต์ไนล์ : มีรายงานผู้ป่วยที่อาการดีขึ้นหลังได้รับ IVI G 3)
หลังการฉีดวัคซีน : มีรายงานการเกิดโรคหลังการฉีดวัคซีนอีสุกอีใส โรคหัด และวัคซีน DPT
พิษและเมแทบอลิซึม
การได้รับฟีนิโทอินเกินขนาด ภาวะโคม่าเบาหวานชนิดไม่คีโตนจากภาวะออสโมลาร์สูง และพิษโคเคนก็สามารถทำให้เกิดโรคได้
Q
สาเหตุในเด็กและผู้ใหญ่แตกต่างกันหรือไม่?
A
ในเด็กประมาณ 50% มีเนื้องอกนิวโรบลาสโตมา ซ่อนอยู่ ดังนั้นในเด็ก OMS ทุกรายจำเป็นต้องประเมินหานิวโรบลาสโตมา 9) ในผู้ใหญ่ 20-40% ของผู้ป่วย OMS เป็นพารานีโอพลาสติก โดยมะเร็งปอดชนิดเซลล์เล็กและมะเร็งเต้านมเป็นมะเร็งที่เกี่ยวข้องบ่อย ทุกช่วงอายุสามารถเกิดโรคหลังการติดเชื้อได้
OMS เป็นการวินิจฉัยทางคลินิกโดยอาศัยอาการแสดงทางคลินิก ไม่มีการตรวจหรือตัวบ่งชี้ทางชีวภาพ ที่แน่ชัด การวินิจฉัยล่าช้าเป็นเรื่องปกติ โดยระยะเวลามัธยฐานจากอาการจนถึงการวินิจฉัยคือ 11 สัปดาห์4)
สำหรับการแยกโรคจากอาตา (nystagmus) ภาวะลูกตากระตุก (ocular flutter) และคลื่นสี่เหลี่ยม (square-wave jerks) โปรดดูหัวข้อ “อาการแสดงทางคลินิก” โรคที่ต้องพิจารณาแยกโรคอื่นๆ ได้แก่ โรคประสาทอักเสบเวสติบูลาร์ (vestibular neuritis) โรคบ้านหมุนจากตำแหน่ง (benign paroxysmal positional vertigo) โรคหลอดเลือดสมอง เนื้องอกสมอง สมองอักเสบจากภูมิคุ้มกัน (autoimmune encephalitis) โรคปลอกประสาทเสื่อมแข็ง (multiple sclerosis) และภาวะเสียการเคลื่อนไหวลูกตา (oculomotor apraxia)4, 7) ภาวะเสียการเคลื่อนไหวลูกตาเป็นโรคที่การเคลื่อนไหวลูกตาแบบกระตุก (saccadic eye movement) บกพร่อง ซึ่งแตกต่างจาก opsoclonus ตรงที่ผู้ป่วยจะแสดงการเคลื่อนไหวชดเชยของศีรษะเมื่อเปลี่ยนการมองไปยังเป้าหมายใหม่
การตรวจภาพสมอง (MRI)
มีวัตถุประสงค์เพื่อแยกโรคของระบบประสาทส่วนกลางปฐมภูมิ ในผู้ป่วย OMS ส่วนใหญ่ MRI จะปกติ ในบางรายอาจพบสัญญาณ T2-FLAIR สูง (ในสมองน้อยและกลีบขมับ)3, 2) และในระยะเรื้อรังอาจพบการฝ่อของสมองน้อย9)
การวิเคราะห์น้ำไขสันหลัง (CSF)
ใช้เพื่อแยกโรค CNS ในผู้ป่วยส่วนใหญ่ผลปกติถึงผิดปกติเล็กน้อย ในบางรายพบ oligoclonal bands บวกและโปรตีนเพิ่มขึ้นเล็กน้อย2, 4) การขยายตัวของ B cell ที่มี CD19+ ใน CSF (สูงสุด 29%) กำลังถูกศึกษาเป็นตัวบ่งชี้ทางชีวภาพ ของกิจกรรมโรค4)
การตรวจคัดกรองมะเร็ง
เด็ก: พิจารณาประเมินหา neuroblastoma ในทุกราย
ผู้ใหญ่: ทำ CT, PET-CT7, 8) หากไม่พบเนื้องอก ให้ติดตามทุก 6 เดือนนานสูงสุด 4 ปี2)
ชุดตรวจแอนติบอดีต่อเส้นประสาท
ตรวจหา anti-Ri (ANNA-2), anti-Hu, anti-Yo, anti-Ma, anti-NMDA receptor เป็นต้น อย่างไรก็ตาม ผู้ป่วยจำนวนมากมีผลแอนติบอดีเป็นลบ
ระบบคะแนน PNS-Care (คณะผู้เชี่ยวชาญนานาชาติปี 2021) พิจารณาลักษณะทางคลินิก ชนิดแอนติบอดี การมีหรือไม่มีมะเร็ง และระยะเวลาติดตาม แบ่งเป็น definite (มากกว่า 8 คะแนน), probable (6–7 คะแนน), possible (4–5 คะแนน)7)
แกนหลักของการรักษาคือการบำบัดด้วยการปรับภูมิคุ้มกัน ในกรณีที่เกิดจากเนื้องอก การรักษาแบบมุ่งเป้าไปที่เนื้องอกเป็นสิ่งจำเป็น และต้องทำควบคู่กับการบำบัดด้วยการปรับภูมิคุ้มกัน การวินิจฉัยที่ล่าช้าสัมพันธ์กับผลลัพธ์ทางระบบประสาท จิตวิทยา และพฤติกรรมที่แย่ลง ดังนั้นการรักษาตั้งแต่เนิ่นๆ จึงมีความสำคัญ
คอร์ติโคสเตียรอยด์ (corticosteroids)
การให้ methylprednisolone ทางหลอดเลือดดำแบบพัลส์ (1 กรัม/วัน × 3–5 วัน) เป็นโปรโตคอลมาตรฐาน2, 6, 7)
ACTH (ฮอร์โมนกระตุ้นต่อมหมวกไต)
ถือเป็นการรักษามาตรฐานในเด็กและผู้ใหญ่
IVI G (อิมมูโนโกลบูลินทางหลอดเลือดดำ)
โดยทั่วไปจะให้ขนาดรวม 2 กรัม/กก. แบ่งให้ใน 3–5 วัน1, 6) มีรายงานผู้ป่วยที่เกี่ยวข้องกับ COVID-19 เริ่มดีขึ้นหลังจาก 1 สัปดาห์และฟื้นตัวเต็มที่หลังจาก 4 สัปดาห์1) และผู้ป่วยที่เกี่ยวข้องกับไวรัส West Nile ดีขึ้นหลังจากให้ยา 5 วัน3)
ริตูซิแมบ (rituximab)
ใช้เพิ่มเติมในกรณีที่การรักษาด้วยสเตียรอยด์ และ IVI G ไม่เพียงพอ มีรายงานใน OMS ที่เกี่ยวข้องกับ teratoma รังไข่ หลังให้ยา 1 กรัม 2 ครั้ง แล้วให้เพิ่มเติมที่ 6 เดือนและ 12 เดือน ไม่มีการกลับเป็นซ้ำนาน 30 เดือน 6) มีข้อบ่งชี้ว่าการกดภูมิคุ้มกันด้วยยาหลายชนิดอาจมีประสิทธิภาพมากกว่าการใช้ยาเดี่ยว
ยากดภูมิคุ้มกันอื่นๆ
มีการใช้ azathioprine, mycophenolate mofetil 8, 7) , cyclophosphamide เป็นต้น
ยาต่อไปนี้ใช้เพื่อลดอาการกล้ามเนื้อกระตุก (myoclonus):
clonazepam : เริ่มต้น 0.5 มก. ก่อนนอน 1) sodium valproate : 1000 มก./วัน 1) เลเวติราเซแทม : เริ่มจาก 500 มก. วันละ 2 ครั้ง แล้วค่อยๆ เพิ่มขนาด1)
การรักษาที่มุ่งเป้าไปที่เนื้องอก (การผ่าตัด เคมีบำบัด รังสีรักษา) เป็นสิ่งจำเป็น การผ่าเนื้องอกอาจไม่ทำให้อาการทางระบบประสาทดีขึ้นเสมอไป มีรายงานว่า OMS เกิดขึ้น 1 เดือนหลังการผ่า6) ในมะเร็งปอดชนิดเซลล์เล็ก มีรายงานว่าการใช้เคมีบำบัด carboplatin + etoposide8) และในมะเร็งเต้านม การใช้เคมีบำบัดแบบ neoadjuvant + rituximab ทำให้อาการดีขึ้น7)
การผ่าเนื้องอกไม่ได้รับประกันว่าอาการทางระบบประสาทจะดีขึ้น การรักษาเนื้องอกร่วมกับการปรับภูมิคุ้มกันเป็นสิ่งสำคัญ
ยาที่ยับยั้งจุดตรวจภูมิคุ้มกันอาจทำให้อาการทางระบบประสาทจากพารานีโอพลาสติกแย่ลง จำเป็นต้องพิจารณาข้อบ่งชี้อย่างรอบคอบ5)
การแลกเปลี่ยนพลาสมา ในทางทฤษฎีอาจกำจัดแอนติบอดีออนโคนิวรอนได้ยากเนื่องจากอยู่ในเซลล์ แต่อาจใช้ก่อนการวินิจฉัยที่แน่ชัด2)
Q
การรักษาต้องใช้ระยะเวลาเท่าใด?
A
ระยะเวลาการรักษาขึ้นอยู่กับสาเหตุ ความรุนแรง และการตอบสนองต่อการรักษา บางรายอาจดีขึ้นภายในไม่กี่สัปดาห์ถึงไม่กี่เดือนด้วย IVI G 3, 4) แต่บางรายอาจต้องได้รับการรักษาด้วยภูมิคุ้มกันระยะยาว เช่น rituximab เพื่อป้องกันการกลับเป็นซ้ำ 6) OMS ที่เกิดจากเนื้องอกมักรุนแรงกว่าและดื้อต่อการรักษามากกว่า OMS ที่ไม่ทราบสาเหตุ 8)
มีทฤษฎีหลักสองทฤษฎีเกี่ยวกับกลไกการเกิด OMS ได้แก่ ทฤษฎีก้านสมองและทฤษฎีสมองน้อย
ทฤษฎีก้านสมอง
ความผิดปกติของเซลล์สร้างสัญญาณกระตุกตา (saccadic burst cells) : โดยปกติเซลล์ burst จะถูกยับยั้งอย่างต่อเนื่องจากเซลล์ omnipause (เซลล์หยุดนิ่งตลอดเวลา)
กลไกการเกิดโรค : การเปลี่ยนแปลงคุณสมบัติของเยื่อหุ้มเซลล์ทำให้เซลล์ burst เกิดการกระตุ้นมากเกินไป หรือการยับยั้งจากเซลล์ omnipause ลดลง → ทำให้เกิดการสั่นของลูกตา
ทฤษฎีสมองน้อย
การสูญเสียการยับยั้งของนิวเคลียสฟาสติเจียลส่วนหางของสมองน้อย : เซลล์เพอร์คินจีที่ทำงานผิดปกติไม่สามารถยับยั้งนิวเคลียสฟาสติเจียลได้
กลไกการเกิดโรค : นิวเคลียสฟาสติจิไอ (fastigial nucleus) เพิ่มการยับยั้งต่อ omni-pause neurons → saccadic burst neurons สั่นสะเทือนอย่างอิสระ → เกิด opsoclonus หลักฐานสนับสนุน ได้แก่ gliosis และการอักเสบใน cerebellar vermis, การเพิ่มขึ้นของการไหลเวียนเลือดในสมองน้อยในระยะเฉียบพลัน และการไหลเวียนเลือดต่ำและการฝ่อในระยะเรื้อรัง9)
สมมติฐานที่ได้รับการยอมรับคือการอักเสบจากภูมิต้านตนเอง ซึ่งเกี่ยวข้องกับทั้งภูมิคุ้มกันแบบเซลล์และแบบฮิวโมรอล
การขยายตัวของ CD19+ B cells ในน้ำไขสันหลัง (สูงสุด 29%) สัมพันธ์กับความรุนแรงทางระบบประสาท4)
ปฏิกิริยาภูมิคุ้มกันในสภาพแวดล้อมจุลภาคของเนื้องอกกระตุ้นให้เกิดปฏิกิริยาข้ามกับแอนติเจนของระบบประสาท7)
แอนติบอดี anti-Ri ทำปฏิกิริยาข้ามกับ Nova-1 และ Nova-2 (โปรตีนจับ RNA ที่แสดงออกอย่างกว้างขวางในระบบประสาทส่วนกลาง)7)
ตรวจพบ onconeuronal antibodies ในผู้ป่วยเพียงประมาณ 25% เท่านั้น2)
โดยทั่วไปแล้วอาการ opsoclonus มักจะหายไปเองไม่ว่าจะได้รับการรักษาหรือไม่ก็ตาม แต่อาจกลับมาเป็นซ้ำได้หลังจากทุเลา และความผิดปกติของการเคลื่อนไหวตามลูกตาแบบ smooth pursuit อาจคงอยู่เป็นเวลานานแม้ opsoclonus จะหายไปแล้ว ผู้ป่วย 60-80% จะมีความผิดปกติทางพฤติกรรมและจิตใจที่หลงเหลืออยู่ และการพยากรณ์โรคทางระบบประสาทในระยะยาวมักไม่ดี
OMS ที่เกิดจาก paraneoplastic มักรุนแรงกว่าและตอบสนองต่อการรักษาได้ไม่ดีเท่า OMS ที่ไม่ทราบสาเหตุ8)
OMS หลังการติดเชื้อหรือไม่ทราบสาเหตุตอบสนองต่อการรักษาด้วยยากดภูมิคุ้มกันได้ดีและมีแนวโน้มที่ดีกว่า8)
OMS ที่ไม่ทราบสาเหตุในผู้ใหญ่มักมีผลลัพธ์ที่ไม่รุนแรง4)
เนื้อหาต่อไปนี้เป็นข้อมูลที่อยู่ในระยะวิจัยหรือระหว่างการทดลองทางคลินิกเท่านั้น ไม่ใช่การรักษามาตรฐานที่สามารถรับได้ในโรงพยาบาลทั่วไป เป็นข้อมูลอ้างอิงสำหรับผู้เชี่ยวชาญเกี่ยวกับการพัฒนาทางการแพทย์ในอนาคต
ในรายงานผู้ป่วย 7 รายของ Emamikhah และคณะ (2021) พบว่า OMS เกิดขึ้นภายใน 2 วันถึง 3 สัปดาห์หลังจากมีอาการทางระบบหายใจจาก COVID-19 และอาการดีขึ้นหลังการรักษาด้วย IVI G 1) ในการทบทวนผู้ใหญ่ พบว่าประมาณ 1 ใน 3 มีอาการคล้ายไข้หวัดใหญ่ก่อนเกิดโรค และร้อยละ 40 มีค่า IgG index สูงขึ้นหรือพบ oligoclonal bands
OMS หลัง COVID-19 กำลังได้รับการยอมรับว่าเป็นกลุ่มอาการพาราติดเชื้อทางภูมิคุ้มกันที่แยกออกจากกันโดยไม่มีภาวะสมองเสื่อมร่วมด้วย
Yang และคณะ (2024) รายงานกรณีที่ MRI ครั้งแรกปกติ ต่อมาหลังจาก 10 วันพบสัญญาณ T2-FLAIR สูง และหลังจาก 4 เดือนสัญญาณหายไปโดยสมบูรณ์3) ซึ่งชี้ให้เห็นว่าอาจมีช่วงเวลาที่เฉพาะเจาะจงระหว่างการเริ่มมีอาการและการตรวจพบความผิดปกติใน MRI
กลุ่มอาการ anti-Ri ซึ่งเดิมถือว่าเป็น OMS ร่วมกับภาวะเสียการทรงตัว กำลังถูกนิยามใหม่ว่าเป็นโรคหลายระบบที่ซับซ้อนมากขึ้น
Freydl และคณะ (2024) เสนอให้กลุ่มอาการสามอย่าง ได้แก่ ความผิดปกติในการเดิน + ความผิดปกติของการเคลื่อนไหวของลูกตา + ภาวะขากรรไกรเกร็ง เป็นกลุ่มอาการที่มีลักษณะเฉพาะ 2) หลังจากวินิจฉัยอาการแล้วประมาณ 4-6 เดือน ผู้ป่วย PNS ประมาณ 80% จะได้รับการวินิจฉัยว่าเป็นเนื้องอก
การศึกษา Pranzatelli (อ้างถึงใน Lawrence 2025) เสนอว่าการเพิ่มขึ้นของเซลล์ CD19+ B ในน้ำไขสันหลังเป็นตัวบ่งชี้ทางชีวภาพ ที่มีศักยภาพของกิจกรรมโรคใน OMS 4) ยังไม่มีการกำหนดมาตรฐาน
OMS ที่เกิดช้าซึ่งเกิดจากการกระตุ้นภูมิคุ้มกันจากการสัมผัสแอนติเจนหลังการผ่าตัดเนื้องอกเป็นที่รู้จัก 6) นอกจากนี้ มีรายงานว่าสารยับยั้งจุดตรวจภูมิคุ้มกันอาจกระตุ้นหรือทำให้ OMS และสมองอักเสบก้านสมอแย่ลงในฐานะผลข้างเคียงที่เกี่ยวข้องกับภูมิคุ้มกัน 5) และอาจจำเป็นต้องพิจารณาหลีกเลี่ยงการใช้ยาในเนื้องอกที่มีการแสดงออกของ PD-L1 สูง
Emamikhah M, Babadi M, Mehrabani M, et al. Opsoclonus-myoclonus syndrome, a post-infectious neurologic complication of COVID-19: case series and review of literature. J Neurovirol. 2021;27(1):26-34.
Freydl E, Tinchon A, Blauensteiner K, Oberndorfer S. Anti-Ri paraneoplastic neurological syndrome presenting with bilateral cranial nerve VI palsy and jaw dystonia. Wien Med Wochenschr. 2024;174(1-2):16-21.
Yang JC, Zekavaty S, Rossi RD, Mahmoud SY. Unique Magnetic Resonance Imaging Findings in Opsoclonus-Myoclonus Syndrome Secondary to the West Nile Virus. Cureus. 2024;16(8):e67932.
Lawrence JS. Challenges in Diagnosing Opsoclonus-Myoclonus Syndrome in Adults. Cureus. 2025;17(5):e84780.
Costa PA, Costa BMLA, Rozenbaum G, Barreto-Coelho P. Anti-Ma paraneoplastic opsoclonus-myoclonus syndrome. BMJ Case Rep. 2021;14(5):e243136.
Jones AA, Chen T. Delayed Opsoclonus-Myoclonus Syndrome After Ovarian Teratoma Resection. J Neuro-Ophthalmol. 2022;42(3):e450-e451.
Soares R, Mittapalli A, Ramakrishnan M, Farooq U. Breast Cancer Presenting As Onconeural Antibody Negative Opsoclonus-Myoclonus Syndrome. Cureus. 2022;14(8):e28417.
Moreira I, Vilas-Boas I, Cassiano Neves M. Paraneoplastic Opsoclonus-Myoclonus Syndrome as a Rare Presentation of Small-Cell Lung Cancer. Cureus. 2022;14(11):e32066.
Takenaka J, Hirata K, Watanabe S, Shiraishi H, Kudo K. Neuroblastoma-related severe hypoperfusion in the cerebellum of an infant: A case of opsoclonus-myoclonus syndrome. Asia Ocean J Nucl Med Biol. 2023;11(1):93-96.