حثل القرنية
حثل مرتبط بـ BIGH3: النوع الحبيبي I و II (بما في ذلك أفيلينو)، الشبكي، Reis-Bücklers، Thiel-Behnke.
حثل القرنية القطروي الغرواني: إزالة النتوءات على القرنية بالكشط أو PTK.
حثل القرنية البقعي: يُستخدم لإزالة العتامة السطحية.

استئصال القرنية العلاجي (phototherapeutic keratectomy: PTK) هو إجراء يستخدم ليزر الإكسيمر (طول موجي 193 نانومتر) لإزالة العتامات وعدم الانتظام والرواسب من سطح القرنية. يعتبر جسرًا بين العلاج الطبي والجراحي لأمراض القرنية، ويستخدم لأغراض علاجية وتصحيحية للانكسار.
في أواخر الثمانينيات وأوائل التسعينيات، تم تطبيق ليزر الإكسيمر على استئصال القرنية الانكساري (PRK) و LASIK. تمت الموافقة على PTK من قبل إدارة الغذاء والدواء الأمريكية (FDA) في عام 1995 لعلاج أمراض القرنية في الجزء الأمامي.
يعمل ليزر الإكسيمر على مبدأ الاستئصال الضوئي (photoablation)، حيث يكسر الروابط الجزيئية ويبخر أنسجة القرنية. تتم إزالة حوالي 0.25 ميكرومتر من الأنسجة لكل نبضة، مما يسمح بالتحكم الدقيق في عمق الاستئصال. يمكن إزالة العتامات حتى عمق 150 ميكرومتر من السطح بما في ذلك الظهارة (حوالي 50 ميكرومتر). بالمقارنة مع الاستئصال اليدوي للقرنية، ينتج عنه انحراف أقل ويستغرق وقت علاج أقصر.
PTK هو إجراء علاجي لإزالة العتامات وعدم الانتظام في سطح القرنية. PRK هو إجراء يهدف إلى تغيير انحناء القرنية الطبيعية لتصحيح الأخطاء الانكسارية. يستخدم كلاهما نفس ليزر الإكسيمر (193 نانومتر)، لكن ملفات تشعيع الليزر والأهداف مختلفة.
العلاج الضوئي للقرنية (PTK) هو الأنسب للحالات التي يوجد فيها عتامة في الجزء الأمامي 10-20% من القرنية دون ترقق ملحوظ 1).
حثل القرنية
حثل مرتبط بـ BIGH3: النوع الحبيبي I و II (بما في ذلك أفيلينو)، الشبكي، Reis-Bücklers، Thiel-Behnke.
حثل القرنية القطروي الغرواني: إزالة النتوءات على القرنية بالكشط أو PTK.
حثل القرنية البقعي: يُستخدم لإزالة العتامة السطحية.
تنكس القرنية وغيره
تنكس القرنية الشريطي: بعد استخلاب الكالسيوم بـ EDTA، يتم تشكيل المنطقة بـ PTK 1).
تنكس عقدة سالتزمان: فعال لتنعيم التليف تحت الظهاري 1).
تآكل ظهارة القرنية المتكرر: يعتبر خيارًا حاسمًا للحالات المقاومة للعلاج المحافظ.
اعتلال القرنية الفقاعي: يُستخدم لتخفيف الألم عندما لا يمكن استعادة الوظيفة البصرية.
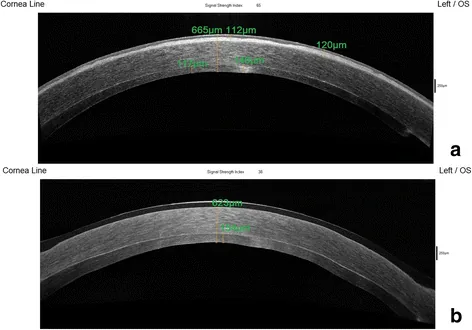
العتامات السطحية المحدودة في الجزء الأمامي 10-20% من القرنية (ضمن حوالي 150 ميكرومتر من السطح) هي الأنسب. الندبات العميقة في السدى تتطلب استئصالًا أكبر مما يؤدي إلى الضبابية وفرط التصحيح، وبالتالي لا تعتبر مناسبة. يشترط أن يكون سمك السدى المتبقي 250 ميكرومترًا على الأقل.
فيما يلي اختيار العلاج الجراحي حسب عمق العتامة1).
| طبقة الآفة | الأمراض النموذجية | ملاءمة PTK |
|---|---|---|
| الظهارة | ظهارة غير منتظمة | × (استئصال الظهارة) |
| تحت الظهارة | تنكس عقدة سالتزمان | ○ |
| غشاء بومان | تنكس القرنية الشريطي و Reis-Bücklers | ○ |
| السدى الأمامي إلى الأوسط | الحثل الحبيبي | ○ (ALK/DALK ممكن أيضًا) |
| الحمة الوسطى إلى الخلفية | ندبة | × (رأب القرنية الطبقي العميق [DALK] / رأب القرنية كامل السمك [PK]) |
يتم إجراؤه تحت التخدير الموضعي بالقطرات (ليدوكائين 4% أو بروباراكايين هيدروكلوريد 0.5%). قد يتطلب الأمر تخديرًا عامًا عند الأطفال. يتم تركيب جفن مفتوح وبدء الإجراء.
يتم إجراؤه إما عن طريق التقشير اليدوي باستخدام سكين على شكل عصا الهوكي، أو عن طريق التقشير عبر الظهارة باستخدام ليزر الإكسيمر (transepithelial PTK).
يُطلب من المريض تثبيت النظر على ضوء التثبيت، أو يتم ضبط مركز الليزر يدويًا لإجراء الاستئصال. إذا كان السطح خشنًا، يتم وضع عامل إخفاء (هيدروكسي بروبيل ميثيل سيلولوز [HPMC] 0.7-2%) لتنعيمه، بحيث يصيب الليزر الأجزاء البارزة فقط.
عند الوصول إلى 70-80% من كمية الاستئصال المستهدفة، يتم إجراء الفحص باستخدام المجهر الحيوي (المصباح الشقي).
تتحسن حدة البصر المصححة بانخفاض كثافة العتامة وتقليل اللابؤرية غير المنتظمة. عند الجمع بين إنشاء السديلة وPTK، تتحسن حدة البصر المصححة بشكل ملحوظ في 2 و6 و12 شهرًا بعد الجراحة1).
ومع ذلك، فإن الاستئصال المركزي يؤدي إلى تسطيح القرنية ويسبب تحولًا بعيد النظر (hyperopic shift). يؤدي شعاع بقطر 6 مم وعمق 100 ميكرومتر إلى تحول بعيد النظر بحوالي 1.5 ديوبتر.
عند إجراء شعاع بقطر 6 مم وعمق 100 ميكرومتر، يُقدر حدوث تحول بعيد النظر بحوالي 1.5 ديوبتر. كلما زاد عمق الاستئصال، زادت درجة التحول البعيد النظر. في بعض الحالات، يمكن الجمع بين PTK وPRK لضبط التغير الانكساري.
ليزر الإكسيمر (ليزر ArF، طول موجي 193 نانومتر) هو ليزر في منطقة الأشعة فوق البنفسجية البعيدة. طاقة الفوتون عند هذا الطول الموجي تتجاوز طاقة تفكك الروابط بين الكربون والكربون أو الكربون والنيتروجين، مما يؤدي إلى قطع الروابط بين الجزيئات في أنسجة القرنية مباشرة وتبخيرها. الضرر الحراري ضئيل جدًا، ويتم تقليل التأثير على الأنسجة المحيطة إلى الحد الأدنى.
سبب فعالية PTK الفريدة في الحثل الشريطي للقرنية هو أن ترسبات الكالسيوم تُزال بسرعة أكبر من أنسجة القرنية المحيطة1). ومع ذلك، قد يؤدي هذا الاستئصال التفاضلي إلى ظهور تفاوتات على السطح، مما يجعل الاستخدام المناسب لعوامل التمويه أمرًا مهمًا.
| المضاعفات | الإجراءات/الملاحظات |
|---|---|
| تكرار المرض الأساسي | شائع بشكل خاص في حثل القرنية |
| الضبابية (عتامة القرنية) | يمكن السيطرة عليها بوضع MMC1) |
| تمدد القرنية (Ectasia) | عند استئصال أكثر من الثلث الأمامي أو سمك متبقي <250 ميكرومتر1) |
| إعادة تنشيط فيروس الهربس البسيط | في حالات تاريخ الهربس، إعطاء مضادات الفيروسات الوقائية1) |
| تأخر التئام الظهارة | يُعالج بقطرات مصل الدم الذاتي أو الغشاء الأمنيوسي1) |
| التهاب القرنية المعدي | خطر مرتبط بفقدان حاجز الظهارة |
| تحول نحو طول النظر | لا مفر منه مع الاستئصال المركزي. يمكن تقليله بتصحيح حافة الاستئصال |
يتطلب الربط المتصالب للقرنية (CXL) إزالة الظهارة، ويُعتبر الاستئصال الضوئي للقرنية عبر الظهارة (transepithelial PTK) تقنية واعدة تُستخدم مع الربط المتصالب2).
تمت مقارنة استخدام PTK لإزالة الظهارة أثناء الربط المتصالب (بروتوكول كريتي) مع الإزالة الميكانيكية، وأظهرت مجموعة PTK نتائج بصرية وانكسارية أفضل2). لا يقتصر PTK على إزالة الظهارة فحسب، بل له أيضًا تأثير في إعادة تشكيل عدم انتظام سطح القرنية الأمامي.
هناك تقارير تفيد بأن الاستخدام المتزامن (PTK/PRK + الربط المتصالب) أكثر فعالية من الاستخدام المتسلسل (الربط المتصالب يليه PRK بعد 6 أشهر)2)، ومن المتوقع تراكم المزيد من الأدلة في المستقبل.