각막 이영양증
BIGH3 관련 이영양증: 과립형 I형·II형(Avellino 포함), 격자형, Reis-Bücklers, Thiel-Behnke.
교양적 방울 각막 이영양증: 각막 돌기를 소파 또는 PTK로 제거합니다.
반점 각막 이영양증: 표층 혼탁 제거에 사용됩니다.

치료적 각막 절제술(phototherapeutic keratectomy: PTK)은 엑시머 레이저(파장 193 nm)를 사용하여 각막 표층의 혼탁, 불규칙, 침착물을 절제하는 시술입니다. 각막 질환에서 내과적 치료와 외과적 치료의 가교 역할을 하며, 치료적 및 굴절 교정적 목적으로 사용됩니다.
1980년대 후반부터 1990년대 초반까지 엑시머 레이저는 굴절 교정 각막 절제술(PRK) 및 LASIK에 적용되었습니다. PTK는 1995년 미국 FDA에서 전안부 각막 질환의 치료로 승인되었습니다.
엑시머 레이저는 광절제(photoablation) 원리로 작동하며, 분자 간 결합을 절단하여 각막 조직을 증발시킵니다. 1펄스당 약 0.25 µm의 조직이 제거되므로 절제 깊이를 정밀하게 제어할 수 있습니다. 상피(약 50 µm)를 포함하여 표면에서 150 µm까지의 혼탁이 제거 대상이 됩니다. 수동 각막 절제와 비교하여 불규칙 난시가 적고 치료 시간도 짧습니다.
PTK는 각막 표층의 혼탁이나 불규칙을 제거하는 치료 목적의 시술입니다. PRK는 정상 각막의 곡률을 변경하여 굴절 이상을 교정하는 목적의 시술입니다. 둘 다 동일한 엑시머 레이저(193 nm)를 사용하지만, 레이저 조사 프로파일과 목적이 다릅니다.
PTK는 각막 전방 10~20%에 혼탁이 있고 현저한 얇아짐이 없는 경우에 가장 적합한 적응증입니다1).
각막 이영양증
BIGH3 관련 이영양증: 과립형 I형·II형(Avellino 포함), 격자형, Reis-Bücklers, Thiel-Behnke.
교양적 방울 각막 이영양증: 각막 돌기를 소파 또는 PTK로 제거합니다.
반점 각막 이영양증: 표층 혼탁 제거에 사용됩니다.
각막 변성 및 기타
대상 각막 변성: 칼슘 침착 부위를 EDTA 킬레이션 후 PTK로 성형합니다1).
Salzmann 결절 변성: 상피하 섬유화의 평활화에 효과적입니다1).
재발성 각막 상피 미란: 보존적 치료에 저항하는 난치성 증례의 마지막 수단입니다.
수포성 각막증: 시기능 회복이 기대되지 않는 경우 통증 완화 목적으로 사용됩니다.
각막 전방 10~20%(표면에서 약 150 µm 이내)에 국한된 표층 혼탁이 최적의 대상입니다. 깊은 실질 반흔은 절제량이 많아져 헤이즈나 원시화를 초래하므로 적응증이 아닙니다. 잔여 실질이 250 µm 이상 확보될 수 있는 것이 조건입니다.
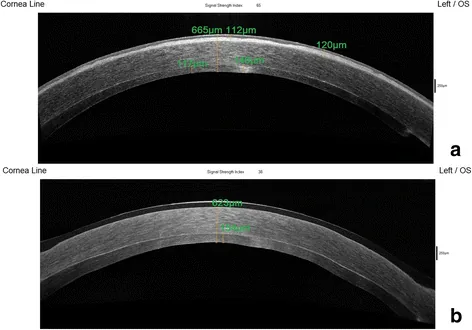
혼탁의 깊이에 따른 외과적 치료 선택은 다음과 같습니다1).
| 병변층 | 대표 질환 | PTK 적응증 |
|---|---|---|
| 상피 | 불규칙 상피 | × (상피 제거술) |
| 상피하 | Salzmann 결절 변성 | ○ |
| Bowman막 | 대상 각막 변성, Reis-Bücklers | ○ |
| 전부~중부 실질 | 과립형 이영양증 | ○ (ALK/DALK도 가능) |
| 중후부 실질 | 반흔 | × (DALK/PK) |
점안 마취(4% 자일로카인 또는 0.5% 프로파라카인 염산염) 하에 시행한다. 소아의 경우 전신 마취를 하기도 한다. 개검기를 장착하고 수기를 시작한다.
하키스틱 나이프를 이용한 수동 제거 또는 엑시머 레이저를 이용한 경상피 PTK 중 하나로 시행한다.
환자가 주시등을 주시하게 하거나 수동으로 레이저 중심을 맞춰 절제를 시행한다. 표면이 거친 경우 마스킹제(히드록시프로필메틸셀룰로오스[HPMC] 0.7~2%)를 도포하여 평활화하고, 돌출부에만 레이저가 조사되도록 한다.
목표 절제량의 70~80%를 조사한 시점에서 세극등 현미경으로 확인한다.
교정 시력은 혼탁 밀도 감소와 불규칙 난시 감소로 개선됩니다. 플랩 생성과 PTK를 병용한 경우, 교정 시력은 수술 후 2, 6, 12개월 시점에서 유의하게 개선됩니다1).
그러나 중심부 절제는 각막을 편평하게 만들어 원시화(hyperopic shift)를 초래합니다. 직경 6 mm, 깊이 100 µm의 조사로 약 1.5 D의 원시화가 발생합니다.
엑시머 레이저(ArF 레이저, 파장 193 nm)는 원자외선 영역의 레이저입니다. 이 파장의 광자 에너지는 탄소-탄소 결합 및 탄소-질소 결합의 해리 에너지를 초과하므로 각막 조직의 분자간 결합을 직접 절단하여 증발시킵니다. 열 손상이 매우 적고 주변 조직에 미치는 영향이 최소화됩니다.
PTK가 대상 각막 변성에서 독특한 효과를 발휘하는 이유는 칼슘 침착물이 주변 각막 조직보다 더 빠르게 절제되기 때문입니다 1). 그러나 이러한 차등 절제로 인해 표면에 요철이 생길 수 있으므로 마스킹제의 적절한 사용이 중요합니다.
| 합병증 | 대책/비고 |
|---|---|
| 원질환 재발 | 특히 각막 이영양증에서 흔함 |
| 헤이즈(각막 혼탁) | MMC 도포로 억제 가능 1) |
| 각막 확장증 | 전방 1/3 초과 절제 또는 잔여 두께 <250 µm 시 1) |
| 단순 포진 바이러스 재활성화 | 포진 병력이 있는 경우 항바이러스제 예방 투여 1) |
| 상피 치유 지연 | 자가혈청 점안액 또는 양막으로 대응1) |
| 감염성 각막염 | 상피 장벽 소실에 따른 위험 |
| 원시화 | 중앙 절제로 불가피. 절삭 가장자리 보정으로 감소 가능 |
각막 크로스링킹(CXL)은 상피 제거가 필요하며, PTK를 이용한 경상피 상피 제거(transepithelial PTK)는 각막 크로스링킹과의 병용 기술로 주목받고 있습니다2).
각막 크로스링킹 시행 시 상피 제거에 PTK를 사용하는 방법(Cretan protocol)과 기계적 상피 제거를 비교한 연구에서 PTK군이 더 나은 시력 및 굴절 결과를 보였다고 보고되었습니다2). PTK는 단순한 상피 제거에 그치지 않고 각막 전면의 불규칙을 정형하는 효과도 함께 가집니다.
동시 병용(PTK/PRK+각막 크로스링킹)이 순차 병용(각막 크로스링킹 시행 6개월 후 PRK)보다 효과적이라는 보고도 있으며2), 향후 추가적인 증거 축적이 기대됩니다.