شبيه بالتوت
النمط التوتي النموذجي: النمط الأكثر شيوعًا.
وسط القرنية: آفات مرتفعة رمادية-بيضاء متجمعة تشبه شكل التوت.
الأميلويد تحت الظهاري: نتوءات هلامية شبه شفافة بلون أبيض حليبي تزداد من المركز إلى المحيط.

حثل القرنية القطيري الشكل (GDLD) هو مرض قرنية وراثي يسبب ترسب الأميلويد تحت ظهارة القرنية، مما يؤدي إلى انخفاض ملحوظ في حدة البصر في كلتا العينين.
تم الإبلاغ عن هذا المرض لأول مرة في عام 1914 من قبل ناكايزومي، وفي عام 1932 أطلق عليه كيوزاوا اسم “التنكس القرني القطيري الشكل”، ومنذ ذلك الحين يُعرف بهذا الاسم. في تصنيف IC3D (اللجنة الدولية لتصنيف حثل القرنية)، يُصنف ضمن حثل الظهارة، واختصاره GDLD.
تم تحديد الجين المسبب في عام 1999 من قبل تسوجيكاوا وآخرين، وهو جين TACSTD2 (محول الإشارة الكالسيومي المرتبط بالورم 2)، وهو جين أحادي الإكسون يقع على الكروموسوم 1p324).
في عام 2019، تم تصنيفه كمرض نادر محدد “الحثل القرني القطيري” وأصبح مؤهلاً للإعانات الطبية 2). تم وضع معايير التشخيص وتصنيف الشدة من قبل مشروع أبحاث سياسات الأمراض المستعصية بوزارة الصحة والعمل والرعاية الاجتماعية 2).
تم الإبلاغ عن GDLD في جميع أنحاء العالم، لكنه أكثر شيوعًا في اليابان. لا توجد حالات تقريبًا في أوروبا وأمريكا الشمالية. تم الإبلاغ عن أكثر من 20 طفرة في جين TACSTD2، مما يدل على عدم التجانس الوراثي. في اليابان، طفرة Q118X الموجودة على 1p32 هي طفرة مؤسسة شائعة، وتشكل أكثر من 80% من الكروموسومات المسببة للمرض لدى المرضى اليابانيين.
غالبًا ما يبدأ قبل سن العشرين. يشكو المرضى من الأعراض التالية منذ الطفولة المبكرة.
مع تقدم العمر، يزداد عدد وحجم رواسب الأميلويد. تصبح الرواسب رمادية-بيضاء إلى صفراء، وتغطي في النهاية معظم القرنية حول الشق الجفني 2). يؤدي ذلك إلى غزو الأوعية الدموية من المحيط، وانخفاض ملحوظ في حدة البصر، وألم في العين، بالإضافة إلى مشاكل تجميلية، مما يقلل بشكل كبير من جودة حياة المريض.
يتم تصنيف عتامة القرنية إلى أربعة أنواع بناءً على شكلها. يمكن تمييز هذه الأنواع باستخدام الفحص المجهري للجزء الأمامي من العين بمصباح الشق 2,3).
شبيه بالتوت
النمط التوتي النموذجي: النمط الأكثر شيوعًا.
وسط القرنية: آفات مرتفعة رمادية-بيضاء متجمعة تشبه شكل التوت.
الأميلويد تحت الظهاري: نتوءات هلامية شبه شفافة بلون أبيض حليبي تزداد من المركز إلى المحيط.
النمط الشريطي للتنكس القرني
النمط الشريطي للتنكس القرني: قد يُرى في المراحل المبكرة.
بين الجفنين: عتامة في الطبقات السطحية. تظهر علامات مشابهة للتنكس القرني الشريطي.
آفات الملتحمة: قد تظهر آفات في الملتحمة أيضًا.
شبيه بالكمكوات
النمط الشبيه بالكمكوات: شائع في الحالات المتقدمة.
رواسب صفراء-بيضاء منتشرة: تصبح القرنية بأكملها صفراء وتظهر مثل الكمكوات.
غزو الأوعية الدموية: قد يصاحبه أوعية دموية سطحية جديدة.
نوع العتامة الحُفَيصية
نوع عتامة السدى: مرحلة أكثر تقدمًا.
امتداد إلى السدى: يمتد الورم إلى سدى القرنية.
غزو الأوعية الدموية: يصاحبه غزو وعائي لنتوءات هلامية بيضاء حليبية إلى صفراء.
أبلغ Ide وآخرون عن الطيف السريري التفصيلي لـ 34 حالة في اليابان، وأظهروا أنه حتى مع نفس طفرة جين TACSTD2 (متغاير الزيجوت Q118X) يمكن أن تختلط أربعة أنماط ظاهرية 3).
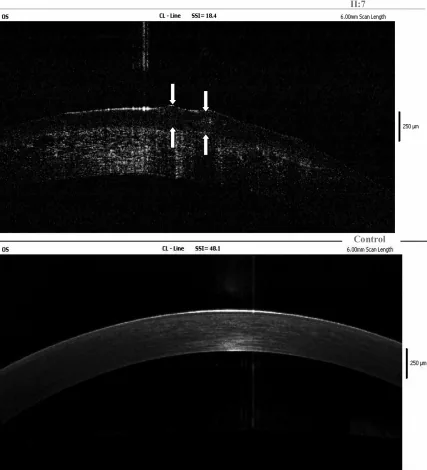
بالإضافة إلى ذلك، هناك النتائج المميزة التالية:
ينجم GDLD عن طفرات فقدان الوظيفة في جين TACSTD2 4).
بسبب خلل في جين TACSTD2، يفقد كلودين-1 وكلودين-7، وهما بروتينان مكونان للوصلات المحكمة في ظهارة القرنية، توطينهما الخلوي الطبيعي، مما يقلل من وظيفة الحاجز الظهاري 5). ونتيجة لذلك، تتسرب بروتينات مثل اللاكتوفيرين من الدموع إلى القرنية، وتشكل ألياف أميلويد تترسب تحت الظهارة. أظهر ناكاتسوكا وآخرون من خلال التحليل الجزيئي لعائلات يابانية أن TACSTD2 ضروري للتوطين الطبيعي للكلودين، وأوضحوا أن الفيزيولوجيا المرضية لـ GDLD ناتجة عن خلل في وظيفة الوصلات المحكمة 5).
تم وضع معايير تشخيص GDLD من قبل فريق دراسة مشروع أبحاث سياسات الأمراض المستعصية بوزارة الصحة والعمل والرفاهية “تطوير إرشادات الممارسة السريرية لأمراض الجزء الأمامي من العين المستعصية ونشرها وتوعية الجمهور” 2). إذا تم تصنيف الحالة على أنها مؤكدة (Definite) وفقًا لهذه المعايير، فإنها تصبح مؤهلة كمرض نادر محدد.
أ. الأعراض (وجود أي مما يلي)
ب. النتائج المخبرية
ج. التشخيص التفريقي: استبعاد الداء النشواني القرني الثانوي واعتلال القرنية القطيري المناخي
د. المضاعفات خارج العين: لا يوجد
هـ. الفحص الجيني: وجود خلل في جين TACSTD2
يتم استيفاء شرط Definite إذا تحقق أحد الشروط التالية2).
ب1 (الرواسب الشبيهة بالتوت) هو عرض مميز جدًا، وفي الحالات النموذجية لا يكون التشخيص صعبًا. في الحالات غير النمطية، يتم التشخيص من خلال الجمع بين أ-ج والفحص الجيني (هـ)2).
تصنف الشدة إلى درجات I-IV بناءً على حدة البصر المصححة في العين الأفضل2).
| الشدة | المعيار | دعم التكاليف الطبية |
|---|---|---|
| الدرجة الأولى | إصابة عين واحدة فقط، والعين الأخرى سليمة | × |
| الدرجة الثانية | إصابة كلتا العينين، حدة الإبصار المصححة في العين الأفضل ≥ 0.3 | × |
| الدرجة الثالثة | إصابة كلتا العينين، حدة الإبصار المصححة في العين الأفضل ≥ 0.1 وأقل من 0.3 | ○ |
| الدرجة الرابعة | إصابة كلتا العينين، حدة الإبصار المصححة في العين الأفضل أقل من 0.1 | ○ |
عند تشخيص الحالة على أنها Definite، تصبح مؤهلة كمرض نادر محدد، ويمكن الحصول على دعم التكاليف الطبية إذا كانت شدة المرض من الدرجة الثالثة أو أعلى2). إذا كان هناك تضيق في المجال البصري (المجال البصري المتبقي المركزي ≤ 20 درجة بمحفز Goldmann I/4) في العين الأفضل بسبب الجلوكوما الثانوية أو غيرها، يتم الانتقال إلى درجة شدة أعلى.
تم تغطية اختبار جين TACSTD2 بالتأمين الصحي منذ عام 2020 كـ “اختبار جيني لحثل القرنية (D006-20)”. ومع ذلك، يجب أن يكون لدى المنشأة نظام يمكنها من إجراء الاختبار والحصول على اعتماد المنشأة. جين TACSTD2 هو جين أحادي الإكسون، مما يسهل البحث عنه، وأكثر من 80% من المرضى اليابانيين لديهم طفرة المؤسس Q118X، مما يجعله مفيدًا بشكل خاص في تشخيص الحالات غير النمطية 2).
يتم اختيار علاج حثل القرنية الهلامي الشكل (GDLD) وفقًا لمدى العتامة ودرجة ضعف البصر. نظرًا لأنه مرض وراثي، فإن التحدي الأكبر هو معدل التكرار المرتفع جدًا مع أي علاج 2). ليس من النادر أن تؤدي المضاعفات الناتجة عن زراعة القرنية المتكررة والزرق الثانوي إلى فقدان البصر.
يُعتبر الارتداء المستمر للعدسات اللاصقة اللينة العلاجية كعلاج تحفظي ومساعد 6). أظهرت دراسة مستقبلية أجراها Maeno وآخرون في عام 2020 على مجموعة من مرضى GDLD أن ارتداء العدسات اللاصقة العلاجية يثبط بشكل ملحوظ تكرار الآفات المرتفعة الجيلاتينية ذات اللون الرمادي إلى الأصفر 7). ويوصى به أيضًا للوقاية من التكرار بعد الجراحة.
استئصال القرنية الضوئي العلاجي (PTK)
استئصال القرنية السطحي بالليزر الإكسيمري العلاجي: الخيار الأول للعتامة السطحية.
المؤشرات: الآفات المرتفعة الجيلاتينية السطحية المبكرة إلى المتوسطة. يُدمج مع الكشط اليدوي. نتائج طويلة الأمد 8,9).
زرع القرنية
زرع القرنية السطحي، العميق (DALK)، والكامل (PKP): يُستخدم في الحالات المتقدمة.
معدل التكرار: التكرار بعد زرع القرنية الكامل يصل إلى 97% خلال 4 سنوات. في DALK، هناك ميزة الحفاظ على البطانة.
زرع الحوف القرني
زرع الخلايا الجذعية الحوفية وتكوين ظهارة القرنية: يُستخدم مع زرع القرنية.
الهدف: تغطية سطح العين بظهارة القرنية المشتقة من الطعم ومنع إعادة غزو ظهارة المضيف 10,11).
تم الإبلاغ عن نتائج طويلة الأمد لـ PTK من اليابان. أظهر Ōura وآخرون النتائج طويلة الأمد لـ PTK في حالات GDLD، وأبلغوا عن فائدته في إطالة الفترة حتى التكرار 8). قام Hieda وآخرون بتحليل مفصل لتوقيت التكرار والنتائج السريرية بعد PTK في دراسة متعددة المراكز في اليابان 9).
يُعتبر دمج زرع الخلايا الجذعية الحوفية (LSCT) نهجًا يابانيًا يُقدر عالميًا. أبلغ Shimazaki وآخرون في عام 2002 عن فعالية زرع القرنية مع LSCT في GDLD، وأظهروا أنه يمكن إطالة الفترة حتى التكرار عن طريق منع إعادة غزو خلايا ظهارة المضيف 10). كما أبلغ Movahedan وآخرون لاحقًا عن نهج مماثل 11).
لتغطية سطح العين بظهارة القرنية المشتقة من الطعم، يتم إزالة ظهارة القرنية للمضيف ثم إجراء زرع الحوف. بعد الجراحة، يستمر ارتداء العدسات اللاصقة العلاجية بشكل مستمر، مما يؤخر أيضًا الانتكاس.
في السنوات الأخيرة، يتم النظر أيضًا في استخدام القرنية الاصطناعية (Boston type I Kpro). من الناحية النظرية، يمكن تجنب إعادة ترسب الأميلويد لأنها لا تمر عبر ظهارة القرنية للمضيف، ولكن هناك خطر حدوث مضاعفات ما بعد الجراحة مثل العدوى والغشاء الخلفي للقرنية الاصطناعية.
في GDLD، معدل الانتكاس بعد زرع القرنية مرتفع للغاية. تم الإبلاغ عن انتكاس حوالي 97٪ في غضون 4 سنوات بعد زرع القرنية النافذ (PKP). السبب الرئيسي هو استبدال ظهارة الخلايا المستقبلة بظهارة الطعم. كإجراء ياباني، يتم تأخير الانتكاس باستخدام زرع الخلايا الجذعية الحوفية للقرنية 10) والارتداء المستمر للعدسات اللاصقة العلاجية 7). في الإدارة طويلة الأمد، يكون الهدف هو الحفاظ على الوظيفة البصرية وإطالة الفترات بين العمليات الجراحية، مع افتراض الانتكاس.
جين TACSTD2، المسؤول عن GDLD، هو جين أحادي الإكسون يقع على الكروموسوم 1p32. تم تحديده كجين مسبب في عام 1999 بواسطة تسوجيكاوا وآخرين من خلال تحليل الارتباط في عائلات يابانية 4). يلعب بروتين TACSTD2 دورًا أساسيًا في الحفاظ على وظيفة حاجز ظهارة القرنية.
عند حدوث طفرات فقدان الوظيفة في جين TACSTD2، يتعطل التوطين الخلوي الطبيعي لبروتينات الوصلات المحكمة Claudin 1 و Claudin 7. أظهر ناكاتسوكا وآخرون، من خلال تحليل خلايا ظهارة القرنية المزروعة وعائلات يابانية، أن فقدان وظيفة TACSTD2 يؤدي إلى فقدان توطين Claudin في الوصلات القمية الجانبية وانخفاض وظيفة حاجز الظهارة 5). علاوة على ذلك، في عام 2011، أبلغوا عن طفرات جديدة في TACSTD2 في 3 عائلات وتوطينها الخلوي غير الطبيعي 12).
بسبب انخفاض وظيفة حاجز الظهارة، تتسرب بروتينات مثل اللاكتوفيرين من الدموع إلى القرنية. يشكل اللاكتوفيرين المتسرب ألياف أميلويد ويترسب تحت ظهارة القرنية. تحتوي رواسب الأميلويد على اللاكتوفيرين، لكن هذا المرض ليس بسبب خلل في جين اللاكتوفيرين.
نسيجيًا، تظهر العتامة البيضاء الحليبية تحت الظهارة باللون البرتقالي المحمر عند صبغها بالكونغو الأحمر، وتظهر انكسارًا مزدوجًا أخضر تفاحي تحت المجهر المستقطب. تحت المجهر الإلكتروني، يُلاحظ أن الوصلات المحكمة للظهارة قد استُبدلت بمساحات شفافة إلكترونيًا. تتسرب الرواسب أيضًا إلى الصفائح القرنية، مما يؤدي إلى تنكس ألياف الكولاجين والبروتيوغليكان.
تم الإبلاغ عن أكثر من 20 طفرة في جين TACSTD212). في اليابان، تشكل طفرة Q118X (طفرة غير منطقية، وظيفية فارغة) أكثر من 80% من الكروموسومات المسببة للمرض كطفرة مؤسسة2). يحدث المرض عادةً في الحالات متماثلة اللواقح، ولكنه يحدث أيضًا في الحالات متغايرة اللواقح المركبة نتيجة زواج بين عائلات مختلفة. ومن المثير للاهتمام، أنه حتى في الحالات متماثلة اللواقح لطفرة Q118X، تُلاحظ الأنماط الأربعة للمرض (التوتي، الشريطي، الكمكواتي، والعتمي الحُجري) مختلطة3).
يُصنف داء النشواني القرني إلى أولي أو ثانوي، وجهازي أو موضعي. يُصنف حثل القرنية القطروي الجيلاتيني (GDLD) ضمن داء النشواني الموضعي الأولي إلى جانب حثل القرنية الشبكي. أما التنكس النشواني الموضعي الثانوي فيحدث نتيجة لشتر رمشي، القرنية المخروطية، الصدمات، أو ارتداء العدسات اللاصقة لفترة طويلة، وهو ما يجب تمييزه تشخيصيًا.
GDLD هو مرض نادر، وكان هناك نقص في الأطباء ذوي الخبرة السريرية في كل منشأة، بالإضافة إلى عدم وجود طرق تشخيص وعلاج موحدة. قامت مجموعة أبحاث المسح الوبائي لأمراض القرنية النادرة والمستعصية التابعة لوزارة الصحة والعمل والرعاية الاجتماعية، ومجموعة أبحاث تطوير ونشر المبادئ التوجيهية السريرية لأمراض الجزء الأمامي المستعصية، بوضع معايير التشخيص وتصنيف الشدة2). في عام 2019، تم الاعتراف بـ “حثل القرنية القطروي الجيلاتيني” كمرض نادر محدد، ويجري حاليًا إعداد مبادئ توجيهية سريرية متوافقة مع Minds2).
على المدى الطويل، يمثل التكرار والعلاجات المتعددة مشكلة. يمكن أن يؤدي الجمع بين العدسات اللاصقة العلاجية وزرع الحوف إلى تأخير التكرار وإطالة الفترات بين العمليات، مما يحسن التشخيص مدى الحياة6, 7, 10).
أبلغ Maeno وآخرون عن حالة سريرية غير نمطية تظهر ترسبًا نشوانيًا متكررًا في عين واحدة فقط، مما يوضح تنوع النمط الظاهري لـ GDLD13). يلعب اختبار جين TACSTD2 دورًا حاسمًا في تشخيص مثل هذه الحالات غير النمطية2).
في مجال الأبحاث الأساسية، من المتوقع التوصل إلى فهم تفصيلي لديناميكيات جزيئات الوصلات المحكمة أسفل TACSTD2 وتطوير علاجات تستهدف تثبيت الكلودين. على الصعيد السريري، يتم دراسة توسيع نطاق تطبيق الأساليب التجديدية مثل القرنية الاصطناعية، وزرع صفائح الظهارة القرنية، والظهارة القرنية المشتقة من خلايا iPS.