LSCD的臨床所見

活體親屬結膜輪部同種移植術(lr-CLAL)
一目了然的要點
Section titled “一目了然的要點”1. 什麼是活體親屬結膜輪部同種移植術(lr-CLAL)?
Section titled “1. 什麼是活體親屬結膜輪部同種移植術(lr-CLAL)?”活體親屬結膜輪部同種移植術(living-related conjunctival limbal allograft: lr-CLAL)是輪部幹細胞缺乏症(limbal stem cell deficiency: LSCD)的一種眼表面幹細胞移植術(OSST)。從相容的活體親屬獲取含杯狀細胞的結膜和輪部組織,移植到患者的眼表面。
角膜上皮的幹細胞存在於輪部,它們向心性移動,分化增殖為基底上皮細胞,然後移向表層1)。在LSCD中,這些幹細胞受損,角膜上皮被結膜上皮取代。結果導致角膜透明性喪失和視力下降1)。單獨角膜移植無法重建LSCD的眼表面,會導致上皮癒合不全和移植片失敗2)。輪部幹細胞移植(LSCT)可以恢復正常的上皮表現型,重建穩定的角膜表面2)。
對於單眼LSCD,可以從健眼進行自體移植(CLAu),但雙眼LSCD需要同種移植。CLAL與KLAL(來自屍體捐贈者)相比,組織相容性更高,手術成績更優3)。自Kenyon和Rapoza於1995年首次報告lr-CLAL以來,隨著捐贈者選擇方案的改進,手術方式不斷發展。
lr-CLAL的主要適應症如下:
2. 主要症狀與臨床所見
Section titled “2. 主要症狀與臨床所見”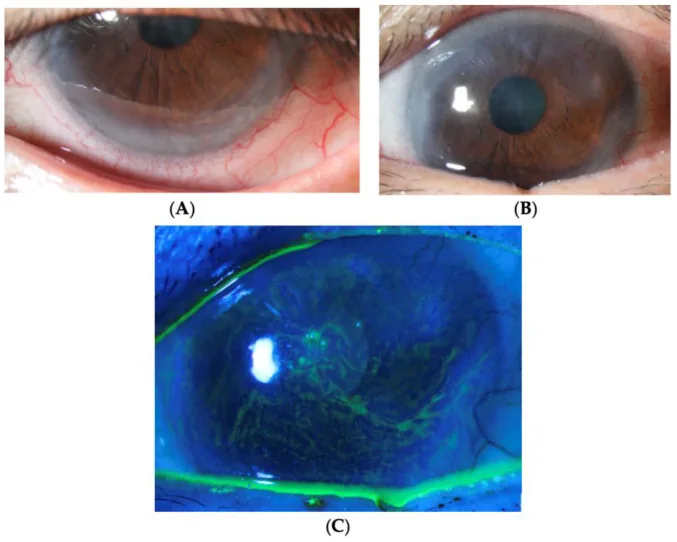
作為lr-CLAL候選者的LSCD患者主訴眼痛、畏光、流淚和視力下降3)。隨著結膜化的進展,視力障礙加重。單眼病例中,患側視力下降是主要主訴。
嚴重度分類
3. 原因與風險因素
Section titled “3. 原因與風險因素”| 原因類別 | 代表性疾病 |
|---|---|
| 外傷性 | 化學傷、隱形眼鏡使用 |
| 免疫介導性 | SJS、GVHD、黏膜類天皰瘡 |
| 遺傳性 | 無虹膜症 |
一項單中心738隻眼的研究報告,無虹膜症佔30.9%,化學/熱燒傷佔20.6%,隱形眼鏡相關佔16.8%,SJS佔10.4%1)。單眼LSCD中,化學傷是最常見的原因1)。
其他原因包括青光眼手術(合併絲裂黴素C/5-FU)1)、放射照射1)、感染性角膜炎1)和春季角結膜炎1)等。
lr-CLAL的相對禁忌症包括明顯的結膜發炎/疤痕、黏蛋白顯著減少、水層淚液減少和眼表面角化。這些情況下OSST預後不良。全身免疫抑制的醫學禁忌症也是相對禁忌症。
4. 診斷與檢查方法
Section titled “4. 診斷與檢查方法”LSCD的診斷
Section titled “LSCD的診斷”LSCD的診斷基於臨床發現和影像學檢查的結合1)。
臨床診斷要點:
| 檢查方法 | 優點 |
|---|---|
| 印跡細胞學 | 可識別杯狀細胞1) |
| 共聚焦顯微鏡 | 可進行全層細胞評估1) |
| 眼前段光學同調斷層掃描(OCT) | 非接觸、快速評估1) |
印跡細胞學檢查中,結膜杯狀細胞的存在表示結膜化1)。細胞角蛋白3(角膜上皮標記物)和細胞角蛋白19(結膜上皮標記物)的免疫組織化學染色可用於鑑別1)。
捐贈者選擇(辛辛那提方案)
Section titled “捐贈者選擇(辛辛那提方案)”捐贈者選擇對於lr-CLAL的成功至關重要。辛辛那提捐贈者選擇方案按以下步驟進行評估。
- 確定一級親屬候選者
- 進行ABO血型鑑定
- 進行群體反應性抗體(PRA)和捐贈者特異性抗體(DSA)檢測
- 進行HLA分型和虛擬交叉配對
- 進行HIV、肝炎和巨細胞病毒的血清學檢測
- 對捐贈者眼睛進行詳細檢查,以排除輕微的幹細胞缺乏
理想的捐贈者是ABO血型相容、HLA相容性高的一級親屬。捐贈者眼睛無長期隱形眼鏡佩戴史或手術史,且無眼表疾病。根據辛辛那提方案,逐步進行血型、抗體檢測、HLA分型和感染篩查,以選擇最合適的捐贈者。
5. 標準治療方法
Section titled “5. 標準治療方法”lr-CLAL手術分兩階段進行:捐贈組織的採集與移植到受體眼。
捐贈組織採集:從12點和6點位置各採集約2個鐘點的結膜與角膜緣組織。總採集量應少於6個鐘點,以防止捐贈眼發生LSCD。以BSS注射抬高結膜,在角膜緣外1mm處進行鈍性剝離以包含幹細胞。
受體眼準備:做360度結膜切開,將結膜後退2-3mm。切除增厚的Tenon囊,去除異常角膜上皮與纖維血管性角膜翳。可同時使用羊膜促進上皮化與抑制發炎。
捐贈組織放置:以10-0尼龍縫線將採集的組織固定在12點和6點位置。以組織黏合劑將基底黏附在鞏膜上,並佩戴大直徑繃帶型角膜接觸鏡。
可能同時進行的手術包括疤痕分離(最常見)、羊膜移植與全層角膜移植術3)。CLAL後的角膜移植術應考慮發炎風險,建議術後等待至少12個月3)。
免疫抑制治療
Section titled “免疫抑制治療”lr-CLAL術後長期移植物存活需要全身免疫抑制。
辛辛那提OSST免疫抑制方案:
- 他克莫司4mg每日兩次+黴酚酸酯(MMF)1g每日兩次,術前1-2週開始
- 術後加用潑尼松1mg/kg/日,1-3個月內逐漸減量
- 使用纈更昔洛韋和TMP/SMX 6個月以預防伺機性感染
眼表穩定後,他克莫司在術後12-18個月開始減量,MMF在術後3年開始減量。如有排斥反應史,則無限期維持低劑量免疫抑制。據報導,環孢素A和MMF長期使用耐受性良好3)。
術後局部治療:使用莫西沙星0.5%、氯替潑諾1%、環孢素A 1%眼藥水以及不含防腐劑的人工淚液3)。
聯合OSST手術
併發症與處理
當眼表足夠穩定時,他克莫司在術後12~18個月開始減量,MMF在術後3年開始減量。但是,如果有移植片排斥反應史,則需要無限期地繼續低劑量免疫抑制。免疫抑制劑的管理應與器官移植專家協作,並定期進行血液檢查以監測副作用。
透過將捐贈眼的採集量限制在每個結膜/角膜輪部段2~2.5鐘點,總計少於5鐘點,捐贈眼發生LSCD的風險較低。術後使用抗生素眼藥水約一週。捐贈眼發生嚴重併發症的可能性較低,但術前需要充分的解釋和同意。
6. 病理生理學與詳細發病機制
Section titled “6. 病理生理學與詳細發病機制”lr-CLAL的目標疾病LSCD的病理本質是角膜輪部幹細胞功能障礙導致的角膜上皮恆定性破壞。
角膜上皮是複層鱗狀上皮,不斷再生1)。1921年Vogt描述的柵欄結構(palisades of Vogt, POV)位於角膜輪部,是具有動靜脈成分的放射狀結構1)。角膜輪部幹細胞存在於POV的基底層,作為角膜上皮再生的來源1)。
當發生LSCD時,角膜上皮被結膜上皮取代,杯細胞出現在角膜上1)。結膜化導致角膜透明性喪失和視力下降2)。如果角膜幹細胞殘留7%,現代外科技術可以再生角膜上皮1)。
lr-CLAL的治療原理是,從捐贈者移植的健康角膜緣幹細胞在受體角膜上恢復正常的上皮表型2)。移植的幹細胞在角膜緣著床,並向心移動,再生角膜上皮。由於lr-CLAL同時移植結膜,因此可以彌補結膜缺損並提供杯狀細胞。
LSCD的嚴重程度因病因不同而異。化學傷不僅損傷角膜緣,還廣泛損傷結膜和角膜基質,因此需要更具侵入性的治療3)。無虹膜症是由於PAX6基因突變導致的先天性角膜緣幹細胞功能障礙,病程呈慢性進行性。
7. 最新研究與未來展望
Section titled “7. 最新研究與未來展望”關於lr-CLAL的臨床數據正在累積中。
Kasikci等人分析了19隻眼的CLAL病例,報告術後1年成功率為52.6%3)。術前LSCD分期越低,成功率顯著越高(p=0.04);在化學傷病例中,從受傷到手術的時間越長,結果越好(p=0.001)3)。化學傷的嚴重程度與手術成功率呈負相關(p=0.001)3)。捐贈者與受體之間的親緣關係(一級或二級)對成功率無顯著影響3)。
Shanbhag等人的系統性回顧顯示,CLET平均追蹤2.9年時眼表穩定率為61.4%(581眼中357眼),BCVA改善2行或以上的比例為51.5%(425眼中219眼)2)。化學傷佔LSCD病因的90%2)。
LSCD診斷技術的進步:前眼部OCT作為一種基於角膜上皮厚度測量的非接觸式LSCD診斷方法正在研究中1)。與印跡細胞學和共聚焦顯微鏡相比,它具有快速和微創的優勢1)。
未來挑戰:
8. 參考文獻
Section titled “8. 參考文獻”
- Hu JCW, Trief D. A narrative review of limbal stem cell deficiency & severe ocular surface disease. Ann Eye Sci. 2023;8:13.
- Shanbhag SS, Nikpoor N, Rao Donthineni P, Singh V, Chodosh J, Basu S. Autologous limbal stem cell transplantation: a systematic review of clinical outcomes with different surgical techniques. Br J Ophthalmol. 2020;104:247-53.
- Kasikci M, Korkmaz I, Palamar M, Egrilmez S, Yagci A, Barut Selver O. Evaluation of the factors that influence surgical outcome in conjunctival-limbal allograft transplantation. Eye. 2023;37:2192-2196.
