การปลูกถ่ายเยื่อบุตา และลิมบัส จากญาติที่มีชีวิต (lr-CLAL ) เป็นการปลูกถ่ายเซลล์ต้นกำเนิดผิวตาชนิดหนึ่งสำหรับภาวะพร่องเซลล์ต้นกำเนิดลิมบัส (LSCD ) โดยนำเนื้อเยื่อเยื่อบุตา และลิมบัส ที่มีเซลล์กุณโฑจากญาติที่มีชีวิตที่เข้ากันได้มาปลูกบนผิวตาของผู้ป่วย
เซลล์ต้นกำเนิดของเยื่อบุกระจกตา อยู่ที่ลิมบัส และเคลื่อนที่เข้าสู่ศูนย์กลางขณะที่แยกตัวและเพิ่มจำนวนเป็นเซลล์เยื่อบุฐาน จากนั้นเคลื่อนที่สู่ผิว 1) ใน LSCD เซลล์ต้นกำเนิดเหล่านี้ถูกทำลาย และเยื่อบุกระจกตา ถูกแทนที่ด้วยเยื่อบุตา ส่งผลให้กระจกตา สูญเสียความใสและการมองเห็น ลดลง 1) การปลูกถ่ายกระจกตา เพียงอย่างเดียวไม่สามารถสร้างผิวตาขึ้นใหม่ใน LSCD และนำไปสู่ความล้มเหลวในการหายของเยื่อบุและความล้มเหลวของ graft 2) การปลูกถ่ายเซลล์ต้นกำเนิดลิมบัส สามารถฟื้นฟูฟีโนไทป์ของเยื่อบุปกติและสร้างผิวกระจกตา ที่มั่นคง 2)
ใน LSCD ข้างเดียว สามารถปลูกถ่าย自体จากตาข้างดีได้ แต่ใน LSCD สองตา จำเป็นต้องปลูกถ่ายจากผู้อื่น CLAL มีความเข้ากันได้ของเนื้อเยื่อสูงกว่าและผลการผ่าตัดดีกว่า KLAL (จากผู้บริจาคที่เสียชีวิต) 3) นับตั้งแต่ Kenyon และ Rapoza รายงาน lr-CLAL ครั้งแรกในปี 1995 เทคนิคก็พัฒนาขึ้นพร้อมกับการปรับปรุงโปรโตคอลการคัดเลือกผู้บริจาค
ข้อบ่งชี้หลักของ lr-CLAL มีดังนี้:
LSCD สองตาLSCD ข้างเดียวที่ตาอีกข้างไม่เหมาะสมเป็นผู้บริจาค (ประวัติการใช้คอนแทคเลนส์ การผ่าตัดก่อนหน้า ฯลฯ)LSCD ร่วมกับความบกพร่องหรือโรคของเยื่อบุตา
Q
lr-CLAL กับ KLAL ต่างกันอย่างไร?
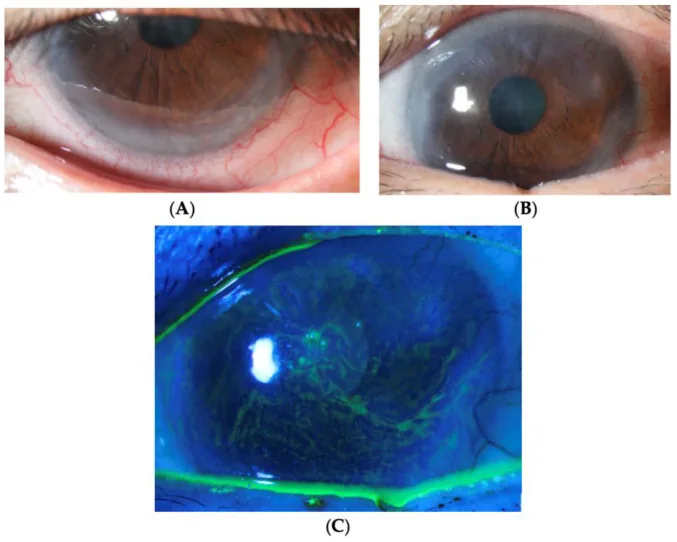
ภาพการปลูกถ่ายเยื่อบุตาลิมบัสจากผู้มีชีวิตเกี่ยวข้องกัน (lr-CL) Yhu Fhei Lee, Dayna Wei Wei Yong, Ray Manotosh A Review of Contact Lens-Induced Limbal Stem Cell Deficiency 2023 Dec 5 Biology (Basel). 2023 Dec 5; 12(12):1490 Figure 2. PM
CI D: PMC10740976. License: CC BY.
A และ B แสดงการรุกรานของเยื่อบุตา จากขอบตาเข้าสู่กลางกระจกตา การสร้างเส้นเลือดใหม่ และการเกิดพานนัส ในการย้อมฟลูออเรสซีน C พบการย้อมเป็นจุดตามแนวเยื่อบุผิวแบบเกลียว ซึ่งบ่งบอกถึงความไม่เสถียรของเยื่อบุผิว
ผู้ป่วย LSCD ที่เป็นกลุ่มเป้าหมายของ lr-CLAL มักมีอาการปวดตา กลัวแสง น้ำตาไหล และการมองเห็น ลดลง 3) การมองเห็น แย่ลงเมื่อเยื่อบุตา ลุกลามมากขึ้น ในกรณีที่เป็นข้างเดียว การมองเห็น ลดลงในข้างที่ได้รับผลกระทบเป็นอาการหลัก
อาการแสดงทางคลินิกของ LSCD
โรคเยื่อบุผิวแบบเกลียว (whorl-like epitheliopathy) : การย้อมฟลูออเรสซีน แสดงรูปแบบความเสียหายของเยื่อบุผิวเป็นเกลียว เป็นอาการเริ่มต้นของ LSCD ระดับเล็กน้อย 1)
การหายไปของ Palisades of Vogt (POV) : โครงสร้างแนวรั้วที่ลิมบัส หายไป เป็นพื้นฐานของการวินิจฉัยทางคลินิกของ LSCD
การกลายเป็นเยื่อบุตา (conjunctivalization) : เยื่อบุผิวกระจกตา ถูกแทนที่ด้วยเยื่อบุผิวเยื่อบุตา สามารถยืนยันได้โดยการปรากฏของเซลล์กอบเล็ตบนกระจกตา 1)
เส้นเลือดใหม่ที่กระจกตา : หลอดเลือดผิวเผินและพานนัสปรากฏขึ้นตั้งแต่ระดับปานกลางขึ้นไป 1)
การจำแนกความรุนแรง
LSCD บางส่วนกระจกตา บางส่วนกลายเป็นเยื่อบุตา ยังมีสเต็มเซลล์ลิมบัส เหลืออยู่ 1)
LSCD ทั้งหมดกระจกตา ทั้งหมดกลายเป็นเยื่อบุตา สเต็มเซลล์ลิมบัส หายไปหมด 1)
การแบ่งระยะโดย Limbal Stem Cell Working Group : ระยะที่ 1 (ส่วนกลาง 5 มม. ใส), ระยะที่ 2 (ส่วนกลาง 5 มม. เกี่ยวข้อง), ระยะที่ 3 (พื้นผิวกระจกตา ทั้งหมดเกี่ยวข้อง) 3)
การแบ่งประเภทย่อยตามการเกี่ยวข้องของลิมบัส : A (≤50%), B (>50% ถึง <100%), C (100%) แบ่งย่อยเพิ่มเติม3)
สาเหตุของ LSCD ที่เป็นข้อบ่งชี้สำหรับ lr-CLAL มีหลากหลาย
ประเภทสาเหตุ โรคที่เป็นตัวแทน การบาดเจ็บ การบาดเจ็บจากสารเคมี การใช้คอนแทคเลนส์ ภูมิคุ้มกันเป็นสื่อกลาง SJS , GVHD, เพมฟิกอยด์ของเยื่อเมือกพันธุกรรม ภาวะไม่มีม่านตา
ในการศึกษาตา 738 ตาจากศูนย์เดียว รายงานว่าภาวะไม่มีม่านตา พบ 30.9%, การบาดเจ็บจากสารเคมี/ความร้อน 20.6%, ที่เกี่ยวข้องกับคอนแทคเลนส์ 16.8% และ SJS 10.4%1) ใน LSCD ข้างเดียว การบาดเจ็บจากสารเคมีเป็นสาเหตุที่พบบ่อยที่สุด1)
สาเหตุอื่นๆ ได้แก่ การผ่าตัดต้อหิน (ร่วมกับ mitomycin C และ 5-FU)1) , การฉายรังสี1) , กระจกตา อักเสบติดเชื้อ1) และเยื่อบุตาอักเสบจากภูมิแพ้ ตามฤดูกาล1)
ข้อห้ามสัมพัทธ์สำหรับ lr-CLAL ได้แก่ การอักเสบและแผลเป็นของเยื่อบุตา อย่างมีนัยสำคัญ การลดลงของเมือกอย่างชัดเจน การลดลงของชั้นน้ำตา และการกลายเป็นเคราตินของผิวตา ในภาวะเหล่านี้ การพยากรณ์โรคของ OSST ไม่ดี ข้อห้ามทางการแพทย์สำหรับการกดภูมิคุ้มกันทั่วร่างกายก็เป็นข้อห้ามสัมพัทธ์เช่นกัน
การวินิจฉัย LSCD ขึ้นอยู่กับการรวมกันของผลการตรวจทางคลินิกและการตรวจภาพ1)
ประเด็นสำคัญในการวินิจฉัยทางคลินิก:
ยืนยันการหายไปของ POV และการเปลี่ยนเป็นเยื่อบุตา ด้วยกล้องจุลทรรศน์ชนิดกรีด
ประเมิน vortex epitheliopathy ด้วยการย้อมฟลูออเรสซีน 1)
สังเกตขอบเขตและความลึกของเส้นเลือดใหม่ที่กระจกตา และพานนัส
วิธีการตรวจ ข้อดี เซลล์วิทยาแบบประทับ สามารถระบุเซลล์กุณโฑได้1) กล้องจุลทรรศน์คอนโฟคัล สามารถประเมินเซลล์ทุกชั้นได้1) เครื่องตรวจวัดชั้นหน้าด้วยแสง (OCT ) การประเมินแบบไม่สัมผัสและรวดเร็ว 1)
ในการตรวจเซลล์วิทยาแบบประทับ การมีเซลล์กุณโฑของเยื่อบุตา บ่งชี้ถึงการเปลี่ยนเป็นเยื่อบุตา 1) การย้อมอิมมูโนฮิสโตเคมีสำหรับไซโตเคราติน 3 (เครื่องหมายของเยื่อบุกระจกตา ) และไซโตเคราติน 19 (เครื่องหมายของเยื่อบุตา ) ใช้ในการวินิจฉัยแยกโรค 1)
การคัดเลือกผู้บริจาคมีความสำคัญอย่างยิ่งต่อความสำเร็จของ lr-CLAL โปรโตคอลการคัดเลือกผู้บริจาคของซินซินเนติจะประเมินตามขั้นตอนต่อไปนี้
ระบุผู้สมัครที่เป็นญาติสายตรงลำดับที่หนึ่ง
ตรวจหมู่เลือด ABO
ตรวจ Panel Reactive Antibody (PRA) และ Donor Specific Antibody (DSA)
ทำ HLA typing และ virtual crossmatch
ตรวจทางซีรั่มวิทยาสำหรับ HIV, ไวรัสตับอักเสบ และไซโตเมกาโลไวรัส
ตรวจตาผู้บริจาคอย่างละเอียดเพื่อแยกการขาดสเต็มเซลล์เล็กน้อย
Q
ผู้บริจาคแบบใดที่เหมาะสม?
A
ผู้บริจาคในอุดมคติคือญาติสายตรงลำดับที่หนึ่งที่มีหมู่เลือด ABO เข้ากันได้และมีความเข้ากันได้ของ HLA สูง ตาผู้บริจาคต้องไม่มีประวัติการใส่คอนแทคเลนส์เป็นเวลานานหรือการผ่าตัดมาก่อน และไม่มีโรคผิวตา ตามโปรโตคอลซินซินเนติ จะทำการตรวจหมู่เลือด ตรวจแอนติบอดี HLA typing และคัดกรองการติดเชื้อเป็นขั้นตอนเพื่อเลือกผู้บริจาคที่เหมาะสมที่สุด
การผ่าตัด lr-CLAL ดำเนินการในสองขั้นตอน: การเก็บส่วนเนื้อเยื่อจากตาผู้บริจาคและการปลูกถ่ายไปยังตาผู้รับ
การเก็บส่วนเนื้อเยื่อจากตาผู้บริจาค : เก็บส่วนของเยื่อบุตา และลิมบัส จากตำแหน่ง 12 นาฬิกาและ 6 นาฬิกา แต่ละส่วนประมาณ 2 ชั่วโมงนาฬิกา ปริมาณรวมน้อยกว่า 6 ชั่วโมงนาฬิกาเพื่อป้องกันการเกิด LSCD ในตาผู้บริจาค ยกเยื่อบุตา ขึ้นด้วยการฉีด BSS และทำการผ่าแบบทื่อผ่านลิมบัส เข้าไปในกระจกตา 1 มม. เพื่อรวมเซลล์ต้นกำเนิด
การเตรียมตาผู้รับ : กรีดเยื่อบุตา 360 องศา และร่นเยื่อบุตา ลง 2-3 มม. ตัด Tenon capsule ที่หนาออก และนำเยื่อบุกระจกตา ที่ผิดปกติและพานนัสที่มีเส้นเลือดและเนื้อเยื่อเส้นใยออก อาจใช้เยื่อหุ้มน้ำคร่ำเพื่อส่งเสริมการสร้างเยื่อบุผิวใหม่และลดการอักเสบ
การวางเนื้อเยื่อผู้บริจาค : ยึดส่วนเนื้อเยื่อที่เก็บไว้ที่ตำแหน่ง 12 นาฬิกาและ 6 นาฬิกาด้วยไหมไนลอน 10-0 ติดฐานกับตาขาว ด้วยกาวเนื้อเยื่อ และใส่คอนแทคเลนส์ปิดแผลขนาดเส้นผ่านศูนย์กลางใหญ่
อาจทำการผ่าตัดร่วม เช่น การปลดพังผืด (พบบ่อยที่สุด) การปลูกถ่ายเยื่อหุ้มน้ำคร่ำ และการปลูกถ่ายกระจกตา แบบทะลุ 3) แนะนำให้รออย่างน้อย 12 เดือนหลัง CLAL ก่อนปลูกถ่ายกระจกตา เนื่องจากความเสี่ยงต่อการอักเสบ 3)
การกดภูมิคุ้มกันทั่วร่างกายมีความจำเป็นต่อการอยู่รอดของเนื้อเยื่อปลูกถ่ายในระยะยาวหลัง lr-CLAL
โปรโตคอลการกดภูมิคุ้มกัน OSST ของซินซินเนติ :
Tacrolimus 4 มก. วันละสองครั้ง + mycophenolate mofetil (MMF) 1 กรัม วันละสองครั้ง เริ่ม 1-2 สัปดาห์ก่อนผ่าตัด
Prednisone 1 มก./กก./วัน เพิ่มหลังผ่าตัด แล้วค่อยๆ ลดลงใน 1-3 เดือน
Valganciclovir และ TMP/SMX เป็นเวลา 6 เดือนเพื่อป้องกันการติดเชื้อฉวยโอกาส
หลังจากผิวตาคงที่ ให้เริ่มลด tacrolimus หลังผ่าตัด 12-18 เดือน และ MMF หลังจาก 3 ปี หากมีประวัติการปฏิเสธ ให้กดภูมิคุ้มกันขนาดต่ำต่อไปอย่างไม่มีกำหนด Cyclosporine A และ MMF รายงานว่าทนได้ดีแม้ใช้ในระยะยาว 3)
การรักษาเฉพาะที่หลังผ่าตัด : ใช้ moxifloxacin 0.5%, loteprednol 1%, cyclosporine A 1% ยาหยอดตา และน้ำตาเทียม ที่ไม่มีสารกันเสีย 3)
ขั้นตอน OSST แบบผสมผสาน
วิธีซินซินเนติ (KLAL /lr-CLAL ) : บ่งชี้ในกรณีตาทั้งสองข้างที่มีโรคเยื่อบุตา เป็นแผลเป็นรุนแรงและลิมบัส ขาดทั้งหมด วางส่วน lr-CLAL ที่ตำแหน่ง 12 นาฬิกาและ 6 นาฬิกา และเพิ่มเนื้อเยื่อ KLAL ที่ตำแหน่ง 3 นาฬิกาและ 9 นาฬิกาเพื่อสร้างลิมบัส ใหม่เกือบ 360 องศา
การใช้ lr-CLAL /CLAu ร่วมกัน : บ่งชี้สำหรับ LSCD รุนแรงข้างเดียวร่วมกับโรคร่วมของลิมบัส และเยื่อบุตา มีเป้าหมายเพื่อลดภาระแอนติเจนให้น้อยที่สุด ขณะเดียวกันก็เพิ่มสเต็มเซลล์ลิมบัส ที่แข็งแรงและปริมาณเยื่อบุตา ให้สูงสุด
ภาวะแทรกซ้อนและการจัดการ
การปฏิเสธแบบเฉียบพลัน : เกิดขึ้นใน 10–40% ของกรณี มีอาการปวด แดง บวมของ graft และเส้นปฏิเสธเยื่อบุผิว รักษาโดยการเพิ่มขนาดยาสเตียรอยด์ เฉพาะที่และทั่วร่างกาย
การปฏิเสธแบบเรื้อรัง : ทำให้เกิดความล้มเหลวของผิวตาอย่างช้าๆ และ graft บางลง การเพิ่มยากดภูมิคุ้มกันทั่วร่างกายได้ผล
ต้อหินทุติยภูมิ สเตียรอยด์ เป็นเวลานานหรือโรคพื้นเดิม 3) หากยาหยอดตาไม่ได้ผล อาจต้องผ่าตัด trabeculectomy หรือผ่าตัด shunt แบบท่อ 3)
Q
ต้องกดภูมิคุ้มกันนานแค่ไหน?
A
เมื่อผิวตาคงที่เพียงพอ ให้เริ่มลด tacrolimus ตั้งแต่ 12–18 เดือนหลังผ่าตัด และลด MMF ตั้งแต่ 3 ปีหลังผ่าตัด อย่างไรก็ตาม หากมีประวัติการปฏิเสธ graft ต้องให้ยากดภูมิคุ้มกันขนาดต่ำต่อไปอย่างไม่มีกำหนด การจัดการยากดภูมิคุ้มกันทำโดยร่วมมือกับผู้เชี่ยวชาญด้านการปลูกถ่ายอวัยวะ โดยติดตามผลข้างเคียงด้วยการตรวจเลือดเป็นประจำ
Q
มีผลต่อตาผู้บริจาคหรือไม่?
A
โดยการจำกัดปริมาณเนื้อเยื่อที่นำจากตาผู้บริจาคให้อยู่ที่ 2–2.5 ชั่วโมงนาฬิกาต่อส่วนของเยื่อบุตา /ลิมบัส รวมน้อยกว่า 5 ชั่วโมง ความเสี่ยงในการทำให้เกิด LSCD ในตาผู้บริจาคต่ำ หลังผ่าตัดใช้ยาหยอดตาปฏิชีวนะประมาณหนึ่งสัปดาห์ โอกาสเกิดภาวะแทรกซ้อนร้ายแรงในตาผู้บริจาคต่ำ แต่จำเป็นต้องอธิบายและได้รับความยินยอมอย่างเพียงพอก่อนผ่าตัด
แก่นแท้ของพยาธิสภาพของ LSCD ซึ่งเป็นเป้าหมายของการผ่าตัด lr-CLAL คือความผิดปกติของสเต็มเซลล์ลิมบัส ที่นำไปสู่การเสียสมดุลของสภาวะธำรงดุลของเยื่อบุผิวกระจกตา
เยื่อบุผิวกระจกตา เป็นเยื่อบุผิวสความัสแบบหลายชั้นที่สร้างใหม่ตลอดเวลา 1) โครงสร้าง palisades of Vogt (POV) ที่ Vogt บรรยายไว้ในปี 1921 อยู่ที่ลิมบัส และเป็นโครงสร้างแนวรัศมีที่มีส่วนประกอบของหลอดเลือดแดงและหลอดเลือดดำ 1) สเต็มเซลล์ลิมบัส อยู่ในชั้นเบซัลของ POV และทำหน้าที่เป็นแหล่งสร้างใหม่ของเยื่อบุผิวกระจกตา 1)
เมื่อเกิด LSCD เยื่อบุผิวกระจกตา จะถูกแทนที่ด้วยเยื่อบุผิวเยื่อบุตา และเซลล์กุณโฑจะปรากฏบนกระจกตา 1) การกลายเป็นเยื่อบุตา ทำให้กระจกตา สูญเสียความใสและการมองเห็น ลดลง 2) หากสเต็มเซลล์กระจกตา เหลืออยู่ 7% เทคนิคการผ่าตัดสมัยใหม่เชื่อว่าสามารถสร้างเยื่อบุผิวกระจกตา ขึ้นใหม่ได้ 1)
หลักการรักษาของ lr-CLAL คือเซลล์ต้นกำเนิดลิมบัส ที่แข็งแรงซึ่งปลูกถ่ายจากผู้บริจาคจะฟื้นฟูฟีโนไทป์ของเยื่อบุผิวปกติบนกระจกตา ของผู้รับ 2) เซลล์ต้นกำเนิดที่ปลูกถ่ายจะฝังตัวที่ลิมบัส และสร้างเยื่อบุกระจกตา ขึ้นใหม่ขณะเคลื่อนที่เข้าสู่ศูนย์กลาง เนื่องจาก lr-CLAL ยังปลูกถ่ายเยื่อบุตา พร้อมกัน จึงช่วยชดเชยข้อบกพร่องของเยื่อบุตา และให้เซลล์กุณโฑ
ความรุนแรงของภาวะแตกต่างกันไปตามสาเหตุของ LSCD ในกรณีสารเคมีบาดเจ็บ ไม่เพียงแต่ลิมบัส เท่านั้น แต่เยื่อบุตา และสโตรมาของกระจกตา ยังได้รับความเสียหายอย่างกว้างขวาง จึงต้องได้รับการรักษาที่รุกรานมากขึ้น 3) ในภาวะไม่มีม่านตา สาเหตุคือความผิดปกติแต่กำเนิดของเซลล์ต้นกำเนิดลิมบัส จากการกลายพันธุ์ของยีน PAX6 โดยมีแนวทางดำเนินโรคแบบเรื้อรังและลุกลาม
การสะสมข้อมูลทางคลินิกเกี่ยวกับ lr-CLAL กำลังดำเนินไปอย่างต่อเนื่อง
Kasikci และคณะวิเคราะห์ดวงตา 19 ดวงที่ได้รับการรักษาด้วย CLAL และรายงานอัตราความสำเร็จ 52.6% ที่ 1 ปีหลังผ่าตัด 3) อัตราความสำเร็จสูงขึ้นอย่างมีนัยสำคัญเมื่อระยะ LSCD ก่อนผ่าตัดต่ำกว่า (p=0.04) และในกรณีสารเคมีบาดเจ็บ ผลลัพธ์ดีขึ้นเมื่อระยะเวลาจากการบาดเจ็บถึงการผ่าตัดนานขึ้น (p=0.001) 3) ความรุนแรงของสารเคมีบาดเจ็บมีความสัมพันธ์เชิงลบกับอัตราความสำเร็จของการผ่าตัด (p=0.001) 3) ระดับความใกล้ชิดทางสายเลือดระหว่างผู้บริจาคและผู้รับ (ระดับที่หนึ่ง/สอง) ไม่ส่งผลต่ออัตราความสำเร็จอย่างมีนัยสำคัญ 3)
ในการทบทวนอย่างเป็นระบบโดย Shanbhag และคณะ อัตราการคงสภาพพื้นผิวตาที่เสถียรโดยเฉลี่ยใน CLET ระหว่างการติดตามผลเฉลี่ย 2.9 ปีคือ 61.4% (357 จาก 581 ดวงตา) และการมองเห็น ที่ดีที่สุดที่แก้ไขแล้วดีขึ้น ≥2 แถวพบใน 51.5% (219 จาก 425 ดวงตา) 2) สารเคมีบาดเจ็บคิดเป็น 90% ของสาเหตุ LSCD 2)
ความก้าวหน้าในเทคนิคการวินิจฉัย LSCD : OCT ส่วนหน้าอยู่ระหว่างการศึกษาวิจัยในฐานะวิธีการวินิจฉัย LSCD แบบไม่สัมผัสโดยอาศัยการวัดความหนาของเยื่อบุกระจกตา 1) มีข้อได้เปรียบในด้านความรวดเร็วและการรุกรานน้อยที่สุดเมื่อเทียบกับการตรวจเซลล์วิทยาแบบประทับและกล้องจุลทรรศน์คอนโฟคอล 1)
ความท้าทายในอนาคต :
การประเมินผลลัพธ์ระยะยาวในอนาคตโดยใช้ระบบการแบ่งระยะ LSCD 3)
การกำหนดมาตรฐานและปรับปรุงโปรโตคอลการคัดเลือกผู้บริจาค
การปรับปรุงสูตรยากดภูมิคุ้มกันและลดผลข้างเคียง
การศึกษาเปรียบเทียบกับการปลูกถ่ายเยื่อบุลิมบัส ที่เพาะเลี้ยง (CLET) และการปลูกถ่ายเยื่อบุลิมบัส แบบง่าย (SLET ) 2)
บทความนี้มีวัตถุประสงค์เพื่อให้ข้อมูลแก่บุคลากรทางการแพทย์และผู้เรียน ไม่ได้ใช้แทนการวินิจฉัยหรือการรักษาเฉพาะบุคคล ในการปฏิบัติทางคลินิกจริง โปรดอ้างอิงแนวทางปฏิบัติล่าสุดและปรึกษาผู้เชี่ยวชาญเมื่อจำเป็น
Hu JCW, Trief D. A narrative review of limbal stem cell deficiency & severe ocular surface disease. Ann Eye Sci. 2023;8:13.
Shanbhag SS, Nikpoor N, Rao Donthineni P, Singh V, Chodosh J, Basu S. Autologous limbal stem cell transplantation: a systematic review of clinical outcomes with different surgical techniques. Br J Ophthalmol. 2020;104:247-53.
Kasikci M, Korkmaz I, Palamar M, Egrilmez S, Yagci A, Barut Selver O. Evaluation of the factors that influence surgical outcome in conjunctival-limbal allograft transplantation. Eye. 2023;37:2192-2196.