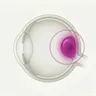
局所強膜結節(focal scleral nodule, FSN)は強膜 内に起源を持つ良性の黄白色結節性病変である。
強調深度イメージングOCT /掃引光源OCT により、かつての「脈絡膜 炎」という診断が誤りであったことが判明した。
大部分は無症状で、ルーチン眼底検査 で偶然発見されることも多い。
無色素性脈絡膜メラノーマ や脈絡膜 転移との鑑別が最重要であり、光干渉断層計 が最も有用な検査である。
活動性病変でも多くが無治療で不活化し、長期的に安定して経過する。
病因は不明であり、確立されたリスク因子は存在しない。
局所強膜結節は、強膜 内に起源を持つ黄白色の隆起した円形の非腫瘍性病変である。典型的には赤道部後方に位置し、直上の脈絡膜 が菲薄化することで眼底から黄白色の病変として観察される。
命名の歴史は以下の通りである。
1997年 :Hongらが初めて「unifocal helioid choroiditis(単一焦点性太陽状脈絡膜 炎)」として報告した。2002年 :Shieldsらが60症例を検討し「solitary idiopathic choroiditis(孤立性特発性脈絡膜 炎)」と命名した。臨床像が静止期の脈絡膜 肉芽腫に類似するが、全身性肉芽腫性疾患の証拠がなかったためである2) 。2020年 :Fungらが光干渉断層計 (OCT )の発展形である強調深度イメージング光干渉断層計 (EDI-OCT )と掃引光源光干渉断層計 (SS-OCT )の所見に基づく63名の回顧的研究を発表した。病変が脈絡膜 ではなく強膜 内に起源を持つこと、脈絡膜 炎を認めないことから「focal scleral nodule(局所強膜結節)」を提唱した1) 3) 。2021年 :Duignanらも同様の所見を報告し「idiopathic scleroma」という命名を提案した1) 。
発症年齢は3〜83歳と幅広く、女性・白人に多い可能性がある。約1/3の患者が診断時に無症状である2) 。
Q
「局所強膜結節」はなぜ以前「脈絡膜炎」と呼ばれていたのか?
A
光干渉断層計 の登場以前は病変が脈絡膜 由来と考えられていた。強調深度イメージング光干渉断層計 ・掃引光源光干渉断層計 により強膜 内起源が確認され、脈絡膜 の変化は病変による機械的圧迫に続発する菲薄化であることが判明し、2020年に改名された。
大部分の局所強膜結節は無症状であり、ルーチン眼底検査 で偶然発見される。症状がある場合は以下が多い。
飛蚊症 ・霧視 中心暗点 中心暗点 が主訴であった2) 。傍中心暗点 :34歳女性例で多発性一過性白点症候群 の合併とともに傍中心暗点 の拡大が認められた1) 。
眼底では隆起した黄色〜黄白色の網膜 下病変として観察される。病変は赤道部後方、視神経乳頭 近傍に多く、サイズは概ね1乳頭径程度である。活動性病変と非活動性病変で所見が異なる。
非活動性(大部分)
境界明瞭な黄白色病変 :輪郭が明確で安定した外観を呈する。
オレンジ色のハロー :病変周囲を囲む橙色の境界が特徴的で、部分的な脈絡膜 菲薄化を反映する1) 。
活動性
くすんだ黄色で境界不明瞭 :非活動性と比べて輪郭が不鮮明となる。
限局的網膜下液 :黄色の網膜 内滲出、網膜 血管拡張、局所的網膜 出血を伴うことがある1) 2) 。
年齢による形態差も報告されている。若年者では結節状(nodular)や火山状(volcanic)の突出性病変が多く、高齢者ではドーム状(dome-shaped)が典型的である。持続的な結節状・火山状の病変は慢性的な機械的圧迫により液体貯留や網膜色素上皮 ・網膜 の萎縮を来しやすい1) 。
Q
局所強膜結節が見つかっても視力に影響はないのか?
A
大部分は無症状であり、視力 への直接的影響は限定的である。症状がある場合も飛蚊症 ・霧視 が主であり、視力 低下は稀である。ただし、詳細は「主な症状と臨床所見」の項 を参照。
局所強膜結節の病因は不明である。以下のいくつかの仮説が存在するが、確立されたリスク因子はない。
先天性の可能性 :若年者での発症例があることから、出生前に発生する先天的状態の可能性がある。感染関連説(旧説) :コクサッキーウイルス、バルトネラ(Bartonella)感染との関連が示唆されたが、近年の文献では否定的である。異なる疾患が混在していた可能性がある1) 。非炎症性の強膜 病変 :Fung ら(2020)の研究では、活動性炎症の徴候(脈絡膜 肥厚・蛍光眼底造影 での漏出・硝子体 炎・全身性炎症所見)を認めず、非炎症性と結論付けた1) 。Duignanら(2021)も同様の結論を支持した1) 。炎症的要素の可能性 :Fengら(2021)は活動性病変において「炎症性肉芽腫反応」と記載しており、活動性病変では炎症的要素が存在する可能性も残る2) 。全身性炎症疾患との有意な関連は認められていない。
臨床診察とマルチモーダルイメージングの組み合わせで診断する。光干渉断層計 による強膜 起源の確認が最重要である。
各検査法の所見を以下に示す。
検査法 特徴的所見 強調深度イメージング光干渉断層計 / 掃引光源光干渉断層計 均一な高反射の強膜 内結節、脈絡膜 圧迫・菲薄化 光干渉断層血管造影 無血管(avascular)、脈絡膜 血流欠損 眼底自発蛍光 高自己蛍光(hyperautofluorescence) Bモード超音波 音響的充実(acoustically solid)、石灰化なし 蛍光眼底造影 早期低蛍光、後期強膜 染色
各検査の詳細を以下に示す。
強調深度イメージング光干渉断層計 / 掃引光源光干渉断層計 (最重要) :均一な高反射の結節状腫瘤が強膜 内に存在し、直上の脈絡膜 がブルッフ膜 方向へ圧縮・菲薄化する所見を確認できる1) 3) 。掃引光源光干渉断層計 では後方境界の可視化が可能である3) 。これが脈絡膜 病変との最大の鑑別点である。光干渉断層血管造影(OCTA ) :病変は無血管であり、機械的圧迫による脈絡膜 非灌流(脈絡膜 血流欠損)を反映する1) 3) 。眼底自発蛍光 脈絡膜 菲薄化により強膜 の自己蛍光が露出するためと考えられている3) 。Bモード超音波 :音響的に充実した病変として描出される2) 3) 。高エコーを示す石灰化は認めない点が強脈絡膜 石灰化との鑑別点となる。
以下の疾患との鑑別が必要である。誤診・過剰治療のリスクがあり、臨床的記載以前は無色素性メラノーマ・転移・骨腫・網膜芽細胞腫 と誤診され、不必要な治療がなされることがあった1) 。
悪性腫瘍 :無色素性脈絡膜メラノーマ 、脈絡膜 転移、脈絡膜 リンパ腫、網膜芽細胞腫 良性腫瘍 :星状細胞過誤腫、脈絡膜母斑 、脈絡膜骨腫 炎症性疾患 :脈絡膜 肉芽腫、白点症候群 、サルコイドーシス 、眼結核 、眼梅毒、真菌性脈絡網膜 炎変性 :強脈絡膜 石灰化(sclerochoroidal calcification)— 局所強膜結節より周辺部に位置し、不規則形状で、Bモード超音波で高エコーを示す点が異なる
全身検査として感染症(梅毒・結核・ライム病 ・バルトネラ・トキソカラ・トキソプラズマ)と炎症性疾患(サルコイドーシス ・多発血管炎性肉芽腫症 )の除外が必要である1) 2) 。
Q
局所強膜結節が悪性腫瘍と間違われることはあるのか?
A
無色素性脈絡膜メラノーマ ・脈絡膜 転移・脈絡膜骨腫 ・網膜芽細胞腫 と誤診されうる。光干渉断層計 による強膜 起源の確認が最重要であり、全身検査による悪性疾患の除外が必須である。
大部分の局所強膜結節は治療不要の良性疾患であり、機能的影響も限定的である。最も重要な管理のポイントは、類似した外観を呈する悪性病変(無色素性脈絡膜メラノーマ ・脈絡膜 転移など)を正確に除外することである。
非活動性病変
経過観察のみ :定期的なモニタリングを行う。積極的な介入は不要である。
活動性病変
慎重な経過観察も選択肢 :18歳男性例では無治療で6週間の経過で不活化し、網膜下液 の消退とオレンジ色ハローの出現が認められた2) 。
全身性ステロイド :試行的に提案されているが、有効性を示すエビデンスはほとんどない。
Shieldsらの60症例の後方視的研究では、6か月〜25年(平均24か月)の追跡において安定60%・改善37%・再発3%という経過が報告されている2) 。ただし27%が先行治療を受けており、活動性・非活動性の層別化はされていない。
まれな多発性一過性白点症候群 の合併例では、メチルプレドニゾロン静注80mg×3日後にプレドニゾン経口40mgを漸減するレジメンが試行された。11週後に最高矯正視力 は20/20に回復し多発性一過性白点症候群 の所見も消失したが、自然軽快との区別は困難である1) 。
Q
局所強膜結節と診断されたら手術は必要か?
A
局所強膜結節は良性疾患であり、ほとんどの場合は経過観察のみで対応する。活動性病変でも無治療で不活化した報告があり、手術適応はない。悪性疾患との鑑別が完了していれば、侵襲的な処置は不要である。
局所強膜結節の解剖学的起源は強調深度イメージング光干渉断層計 ・掃引光源光干渉断層計 により強膜 内に位置することが確認されている。以前は脈絡膜 炎と考えられていたが、脈絡膜 の関与は二次的な圧迫による菲薄化であることが明らかになった3) 。
病変による機械的圧迫が引き起こす変化の連鎖は以下の通りである。
脈絡膜 血管の非灌流強膜 内結節が脈絡膜 を圧迫し、光干渉断層血管造影で脈絡膜 血流欠損として確認できる1) 。網膜色素上皮 ポンプ機能障害脈絡膜 非灌流により網膜色素上皮 の機能が障害され、一部の症例で網膜下液 が出現する。眼底の黄白色外観 :直上の脈絡膜 菲薄化〜消失により、強膜 病変が透見されるためである。オレンジ色ハローの成因 :病変周囲の部分的な脈絡膜 菲薄化を反映すると考えられている1) 。
多発性一過性白点症候群 (multiple evanescent white dot syndrome, MEWDS )の二次発症の機序に関しては、局所強膜結節の頂部の網膜色素上皮 障害により網膜 抗原が露出し、これが免疫応答を惹起して多発性一過性白点症候群 様の反応をもたらすという仮説がSawutら(2025)によって提唱されている1) 。網膜色素上皮 破壊による網膜 抗原暴露が多発性一過性白点症候群 の基礎機序であるとする既報と一致する考え方である。
病理組織学的には十分に解明されていない。Fengら(2021)は炎症性肉芽腫反応と記載しており2) 、今後のさらなる調査が求められている。
局所強膜結節の疾患概念は近年急速に拡大しており、以下の知見が蓄積されつつある。
Sawutら(2025)は局所強膜結節に二次的な多発性一過性白点症候群 が合併した世界初の症例を報告した1) 。局所強膜結節による網膜色素上皮 障害が多発性一過性白点症候群 の発症トリガーとなる可能性を示唆し、局所強膜結節の合併症スペクトルの広がりを示すものである。
近年の主要報告を以下に示す。
著者・年 知見 Fung & Li(2024) 局所強膜結節の経過中の成長を報告1) Park(2023) 双焦点(bifocal)の局所強膜結節を報告、スペクトルの拡大を示唆1) Yamashita ら(2022) レーザースペックルフローグラフィの所見を報告1) Stephenson ら(2024) マルチモーダルイメージングとPD-OCT 解析を報告1)
長期経過に関しては、大部分の局所強膜結節の病変が安定して経過するが、増大する例や限局性脈絡膜陥凹 (focal choroidal excavation)へ退縮する例も報告されている1) 。命名論争については、「focal scleral nodule」(Fung 2020)と「idiopathic scleroma」(Duignan 2021)が競合しているが、現時点では局所強膜結節(FSN)が広く使用されている1) 。
Sawut A, Meng Y, Lhamo T, Xiao D, Su Y, Chen C.. Multiple evanescent white dot syndrome associated with focal scleral nodule: a case report and literature review. BMC Ophthalmol. 2025;25(1):413. doi:10.1186/s12886-025-04231-4. PMID:40671005; PMCI D:PMC12265223.
Feng Y, Conrady CD, Demirci H.. The evolution of an active solitary idiopathic choroiditis (focal scleral nodule): a case report of the natural course and a review of the literature. BMC Ophthalmol. 2021;21(1):130. doi:10.1186/s12886-021-01888-5. PMID:33750335; PMCI D:PMC7942170.
Asensio-Sánchez VM, Pacheco-Carllirgos GE, Valentín-Bravo FJ.. Multimodal Imaging Features of Focal Scleral Nodule. Int Med Case Rep J. 2021;14:255-259. doi:10.2147/imcrj.s301633. PMID:33907475; PMCI D:PMC8071086.
Gao J et al. Growth of a Focal Scleral Nodule. Retinal Cases Brief Rep. 2024. PMID: 37027817
記事の全文をコピーして、お好みのAIに貼り付けて質問できます
下のAIを開いて、チャット欄に貼り付け(ペースト)してください