経過観察(手術保留)

角結膜デルモイド(類皮腫)
1. 角結膜デルモイドとは
Section titled “1. 角結膜デルモイドとは”角結膜デルモイド(limbal dermoid)は、角膜・輪部・結膜に生じる分離腫(choristoma)の一種で、外胚葉の異形成に由来する先天性良性腫瘤である。分離腫とは、本来その部位に存在しない組織が異所性に発生したものをいう。胎生期の第一および第二鰓弓の形成異常が原因とされており、眼周囲腫瘍の中で先天性腫瘤の代表的疾患である。
本症は遺伝性ではなく突発性で、出生時より片眼性にみられる。腫瘤の大きさは直径3mm程度のものから、大きいものでは10mmに達するものもある。
発生部位による分類
Section titled “発生部位による分類”| 型 | 好発部位 | 頻度 |
|---|---|---|
| 輪部デルモイド | 下耳側輪部 | 最多 |
| 角膜デルモイド | 輪部から角膜中央部に及ぶ | 輪部型より少ない |
| 結膜デルモイド | 結膜のみに生じる | 比較的稀 |
輪部デルモイドが最も多く、下耳側輪部への好発が特徴的である。角膜デルモイドは輪部から角膜中央部にかけて広がる型で、視力障害のリスクが高い。
Goldenhar症候群との関連
Section titled “Goldenhar症候群との関連”輪部デルモイドは、副耳・耳瘻孔などの耳の異常、脊柱の異常を合併することがある。これらの多発奇形の組み合わせはGoldenhar症候群(眼耳脊椎症候群; oculoauriculovertebral spectrum)として知られる。下顎骨形成不全を伴う場合もあるため、輪部デルモイドを観察したら全身検査を施行する必要がある。
Goldenhar症候群はデルモイド患者の約10〜20%に認められるとされ、眼科的所見のみで気づかれる場合も多い。耳鼻咽喉科・整形外科・口腔外科との連携が重要である。
2. 主な症状と臨床所見
Section titled “2. 主な症状と臨床所見”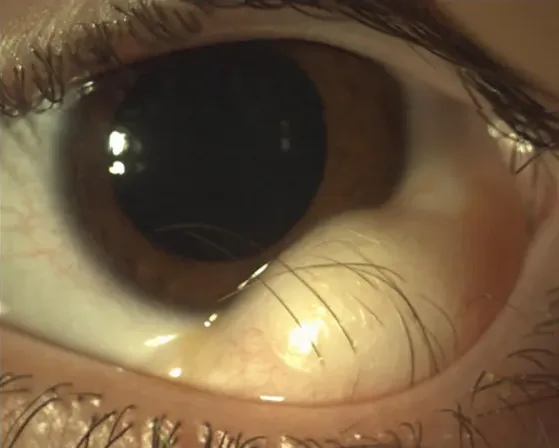
デルモイドは充実性の腫瘍である。輪部デルモイドは特に下耳側輪部に発生しやすく、半球状ないし扁平な淡黄白色の腫瘤として観察される。腫瘤の直径は3〜10mmで、出生時から存在する。
組織学的構成
Section titled “組織学的構成”分離腫であることから、以下の異種組織が混在している。
- 外胚葉由来:皮膚(角化した表皮)、毛髪、まれに歯
- 中胚葉由来:脂肪組織、軟骨組織
デルモイドの表面は皮膚組織で角化しており、涙液膜はその部位で弾かれ(break-up)、正常な眼表面被覆が形成されない。毛髪様の組織が腫瘤表面から突出して観察されることもある。
視力・屈折への影響
Section titled “視力・屈折への影響”デルモイドによって角膜形状が変化し、不正乱視・正乱視が生じる。この角膜乱視が不同視を引き起こし、弱視(amblyopia)に発展することがある。弱視は視覚発達の感受性期(生後3ヶ月〜8歳頃)に不可逆的に進行するため、乳幼児期からの定期的な視力・屈折評価が欠かせない。
角膜中央部まで進展した大型のデルモイドでは、不透明な腫瘤が視軸を遮蔽し、形態覚遮断性弱視を引き起こすこともある。
その他の眼局所所見
Section titled “その他の眼局所所見”- 眼瞼異常(小眼球症、眼瞼欠損)を合併することがある
- 結膜デルモイドは結膜の充実性腫瘤として観察される
- 角膜デルモイドは前眼部全体に広がる場合があり、輪部生殖幹細胞(limbal stem cells)への影響も懸念される
3. 原因とリスク要因
Section titled “3. 原因とリスク要因”デルモイドは、胎生期に外胚葉が角膜・結膜を形成する過程で生じた異形成に由来する。具体的には第一鰓弓(下顎弓)および第二鰓弓(舌骨弓)の形成異常が起点となり、外胚葉由来の組織が眼表面に迷入・残留すると考えられている。
本症は遺伝性疾患ではなく、突発性(散発性)に発生する。家族内集積の報告は稀であり、遺伝カウンセリングの対象となるケースは限定的である。
Goldenhar症候群:全身合併症のチェックポイント
Section titled “Goldenhar症候群:全身合併症のチェックポイント”Goldenhar症候群(眼耳脊椎症候群; oculoauriculovertebral spectrum)は、眼・耳・顎骨・脊椎の先天性奇形が多発する症候群である。輪部デルモイド、副耳、耳瘻孔、小顎症、脊椎奇形などが主な症状であり、片側性に出現することが多い。頻度は約1/5,600〜1/26,550出生とされる。眼科での輪部デルモイド発見が診断の端緒となることが多く、多職種連携による全身管理が重要である。
4. 診断と検査方法
Section titled “4. 診断と検査方法”出生時から存在する下耳側輪部の充実性腫瘤という典型的な所見で臨床診断が可能である。細隙灯顕微鏡検査では、表面の角化・毛髪構造・腫瘤の充実性を確認できる。
類皮囊胞(dermoid cyst)との鑑別が最も重要である。類皮囊胞は囊胞状で内部に分泌物(皮脂・毛髪)を貯留しているのに対し、デルモイドは充実性(solid)であるため、触診・細隙灯所見・超音波検査などで鑑別可能である。
| 鑑別疾患 | 特徴 | 鑑別のポイント |
|---|---|---|
| 類皮囊胞(dermoid cyst) | 囊胞状、内容物貯留 | 充実性(デルモイド)vs 囊胞性(類皮囊胞) |
| 翼状片(pterygium) | 三角形の血管性増殖 | 成人発症、充血性、鼻側発生が多い |
| 結膜色素性病変 | 平坦・色素沈着 | 非腫瘤性、色調の違い |
| 上皮性腫瘍(OSSN等) | 表面不整・充血 | 通常小児ではなく成人〜高齢者 |
前眼部OCTによる浸潤深度評価
Section titled “前眼部OCTによる浸潤深度評価”前眼部光干渉断層撮影(AS-OCT)は、デルモイドの角膜実質への浸潤深さを非侵襲的に評価するうえで有用な検査である。術前の浸潤深度評価は、切除と同時に行う表層角膜移植の深さ設定(板層の厚さ)を決定するために重要となる。
屈折・視力検査と弱視評価
Section titled “屈折・視力検査と弱視評価”乳幼児では視力検査が困難なため、角膜曲率測定・オートレフラクトメータ(サイクロペジア下)による屈折検査を行い、乱視の程度を定量化する。視力は片眼遮閉試験(覗き検査)・Teller視力検査・VEP(視覚誘発電位)などで評価する。
Goldenhar症候群の全身検査
Section titled “Goldenhar症候群の全身検査”- 耳鼻咽喉科:外耳・聴力検査(聴力損失合併の有無)
- 整形外科:脊柱X線(頸胸椎奇形の評価)
- 口腔外科・形成外科:顎骨・顔面骨評価
- 循環器科:心エコー(先天性心疾患除外)
- 腎泌尿器科:腎超音波(腎奇形除外)
5. 標準的な治療法
Section titled “5. 標準的な治療法”角結膜デルモイドの治療は、弱視管理と外科的切除の2本柱で構成される。
弱視管理(最優先事項)
Section titled “弱視管理(最優先事項)”- 眼鏡矯正:角膜乱視に応じた乱視矯正眼鏡を早期に処方
- コンタクトレンズ:不正乱視が強い場合はハードコンタクトレンズも考慮
- 遮閉(アイパッチ)療法:優位眼遮閉による弱視眼の視力訓練
- 薬物的遮閉(アトロピン点眼):遮閉補助として優位眼にアトロピン1%点眼液を使用
弱視の感受性期(8歳まで)を過ぎると治療効果が著しく低下するため、早期発見・早期介入が予後を左右する。
手術適応と時期の選択
Section titled “手術適応と時期の選択”早期手術(積極的介入)
美容的手術
適応:輪部限局で視力・角膜への影響が軽度だが、美容的改善を希望する場合。
時期:乳幼児期を過ぎてからが望ましい(幼少時全身麻酔のリスクを回避)。
注意:美容目的であっても、術後の偽翼状片・再発対策として表層角膜移植を併用する。
外科的手術:表層角膜移植の併用が必須
Section titled “外科的手術:表層角膜移植の併用が必須”デルモイドの単純切除(excision alone)のみでは再発や偽翼状片(pseudopterygium)が高頻度に生じる。また、輪部デルモイドは角膜実質に及んでいるため、単純切除では角膜の菲薄化(thinning)が生じ、角膜穿孔リスクとなる。このため、表層角膜移植(lamellar keratoplasty)を併用することが標準術式である。
標準術式の手順概要:
- デルモイドを輪部から角膜側へ剥離・切除
- 切除部位の角膜床の深さをAS-OCTで術前に把握
- ドナー角膜(板層ボタン)を欠損部に縫合固定
- 輪部幹細胞温存に配慮しながら縫合する
前眼部OCTを用いた術前計画により、浸潤深度に合わせた板層の厚さ設定が精度よく行える。フェムトセカンドレーザーを用いた板層切開の応用も報告されており、切開面の精度向上が期待されている。
幼少時(学童前)の手術は全身麻酔が必要で、術後も弱視訓練の継続が求められる。
単純切除のみでは再発・偽翼状片(pseudopterygium)が高頻度にみられる。表層角膜移植を併用することでこれらのリスクを大幅に低減できる。それでも輪部幹細胞の機能低下が残る場合は、長期的な角膜上皮の安定性に影響することがあり、術後は定期的な前眼部評価が必要である。
6. 病態生理学・詳細な発症機序
Section titled “6. 病態生理学・詳細な発症機序”分離腫(choristoma)としての病態
Section titled “分離腫(choristoma)としての病態”デルモイドは「分離腫(choristoma)」に分類される。分離腫とは、組織学的には正常な構造を持つ組織が、本来存在しない部位に異所性に発生したものである。奇形腫(teratoma)と異なり、多系統の組織が無秩序に混在するのではなく、正常組織(皮膚・毛嚢・脂腺・脂肪・軟骨)が組織学的に正常な構造を保ちながら、眼表面という本来存在しない場所に局在している。
胎生発生における異常
Section titled “胎生発生における異常”胎生期の第一鰓弓(下顎弓)および第二鰓弓(舌骨弓)は顔面・耳介・下顎骨の発達を担う。これらの形成異常によって神経堤細胞(neural crest cells)の移行が乱れ、外胚葉組織が眼表面に迷入・残留すると考えられている。この結果、外胚葉由来の組織(皮膚・毛髪・歯の原基)と中胚葉由来の組織(脂肪・軟骨)が混在したデルモイドが生じる。
Goldenhar症候群ではこの形成異常がより広域に及び、耳介・顎骨・脊椎にも奇形が多発する。
角膜乱視の発生機序
Section titled “角膜乱視の発生機序”デルモイドの存在は角膜形状を変化させ、角膜曲率の非対称性を引き起こす。輪部デルモイドが下耳側に付着することで、その方向の角膜が扁平化し、against-the-rule(倒乱視)ないし斜乱視が生じやすい。乱視の程度はデルモイドのサイズ・輪部への付着面積・角膜実質浸潤の深さに依存する。
高度の乱視(例:3D以上の柱状差)は視覚発達の感受性期に不同視弱視を引き起こす重要な因子であり、早期の屈折矯正介入が必要である。
術後の偽翼状片発生機序
Section titled “術後の偽翼状片発生機序”デルモイド切除後に偽翼状片が高頻度に発生する原因として、輪部幹細胞(limbal stem cells)の損傷が挙げられる。輪部には角膜上皮の再生を担う幹細胞が集積しているが、デルモイド自体が輪部に存在することで幹細胞ニッチを障害する。切除時に残存した幹細胞機能が低下している場合、術後に結膜上皮が角膜側に侵入して偽翼状片を形成する。表層角膜移植によるドナー組織の補充がこのリスクを低減する機序となっている。
7. 最新の研究と今後の展望
Section titled “7. 最新の研究と今後の展望”前眼部OCTによる術前評価の精密化
Section titled “前眼部OCTによる術前評価の精密化”高解像度前眼部OCT(AS-OCT)を用いたデルモイドの角膜実質浸潤深度の定量的評価が進んでいる。術前にデルモイドの基底面の深さ・輪部幹細胞への影響範囲を可視化することで、板層角膜移植の切開深度の設定精度が向上し、術後合併症の軽減に寄与するとされる。
フェムトセカンドレーザー応用
Section titled “フェムトセカンドレーザー応用”フェムトセカンドレーザーを用いた板層切開技術(フェムト板層角膜移植)のデルモイド切除への応用が報告されている。均一な厚さの板層ボタンを精度よく作製することで、切除後の角膜形状の規則性が高まり、術後屈折の安定性改善が期待されている。
表層板層移植 vs 深層板層移植の比較
Section titled “表層板層移植 vs 深層板層移植の比較”デルモイドが深層角膜実質に及ぶ例では、従来の表層角膜移植に加え、深層板層角膜移植(DALK: deep anterior lamellar keratoplasty)の適用が検討されている。DALKはデスメ膜直上まで実質を置換するため、深部浸潤例への対応が可能であるが、技術的難度が高く、小児例への適応は慎重に判断する必要がある。
Goldenhar症候群の分子遺伝学
Section titled “Goldenhar症候群の分子遺伝学”Goldenhar症候群の遺伝的背景として、MYT1L、FOXI3、ZIC3などの遺伝子バリアントが関与する症例の報告が蓄積している。また染色体コピー数変異(CNV)がGoldenhar症候群の一部症例に検出されている。遺伝カウンセリングや次世代シークエンシングを含む網羅的遺伝子検査の役割が今後拡大する可能性がある。
輪部幹細胞移植の応用
Section titled “輪部幹細胞移植の応用”デルモイド切除に伴う輪部幹細胞機能低下に対して、自家あるいは同種輪部幹細胞移植の応用が研究されている。輪部幹細胞欠損(LSCD)が生じた場合には、培養輪部上皮細胞移植(CLET)や培養口腔粘膜上皮移植(COMET)が選択肢となりうる。
8. 参考文献
Section titled “8. 参考文献”- Mansour AM, Wang F, Henkind P, et al. Ocular findings in the facioauriculovertebral sequence (Goldenhar-Gorlin syndrome). Am J Ophthalmol. 1985;100(4):555-559.
- Pirouzian A. Management of pediatric corneal limbal dermoids. Clin Ophthalmol. 2013;7:607-614.
- Scott JA, Tan DT. Therapeutic lamellar keratoplasty for limbal dermoids. Ophthalmology. 2001;108(10):1858-1867.
- Panton RW, Sugar J. Excision of limbal dermoids. Ophthalmic Surg. 1991;22(2):85-89.
- Robb RM. Refractive errors associated with hemangiomas of the eyelids and orbit in infancy. Am J Ophthalmol. 1977;83(1):52-58.
- Mattos J, Contreras F, O’Donnell FE Jr. Ring dermoid syndrome. A new syndrome of autosomal dominantly inherited, bilateral, annular limbal dermoids with corneal and conjunctival extension. Arch Ophthalmol. 1980;98(6):1059-1061.
- Mader TH, Stulting RD. Keratorefractive surgery in the presence of corneal dermoids. Refractive Corneal Surg. 1992;8(6):498-499.
- Liesegang TJ. Limbal dermoids revisited. Ophthalmology. 1999;106(12):2277-2279.
- Ramos M, Krueger RR, Ang E. Laser-assisted in situ keratomileusis and photorefractive keratectomy for the treatment of anisometropia. J Refract Surg. 2001;17(2):S219-S222.
- Watts P, Michaeli-Cohen A, Abdolell M, et al. Outcome of lamellar keratoplasty for limbal dermoids in children. J AAPOS. 2002;6(4):209-215.
- Baum JL, Feingold M. Ocular aspects of Goldenhar’s syndrome. Am J Ophthalmol. 1973;75(2):250-257.
- Elsas FJ, Maumenee IH, Kenyon KR, et al. Familial aniridia with preserved ocular function. Am J Ophthalmol. 1977;83(5):718-724.
- Rooijers W, Chang J, Ruggeri M, et al. High-resolution anterior segment optical coherence tomography for the assessment of limbal dermoids. Cornea. 2020;39(6):747-752.
- Gu M, Kim KH, Kim JM, et al. Femtosecond laser-assisted lamellar keratoplasty for limbal dermoid: a case report. Cornea. 2019;38(5):649-652.
- Vito Raimondi G, Gonnella P, Calzetti G, et al. Limbal dermoid excision combined with lamellar keratoplasty: a retrospective analysis of surgical outcomes. Eye (Lond). 2021;35(7):1988-1994.
