ฟีโนไทป์ 1
การกระจาย: ชนิดที่กระจุกตัวบริเวณจอประสาทตาส่วนกลาง (macula)
ความเสี่ยงของภาวะแทรกซ้อน: อุบัติการณ์โดยประมาณของ GA ใน 5 ปี เท่ากับ 12.9% ซึ่งต่ำที่สุดใน 3 ชนิด

ดรูเซนชั้นฐาน (basal laminar drusen; BLD) เป็นแนวคิดโรคที่ Gass บรรยายครั้งแรกในปี 1977 ว่ามีดรูเซนสีเหลืองขนาดเล็กจำนวนมากกระจายอยู่ทั่วจอตา รูปแบบ “ดาวบนท้องฟ้า” ในการตรวจหลอดเลือดด้วยฟลูออเรสซีน (FA) เป็นลักษณะเฉพาะ 1)
ในตอนแรกถูกเรียกว่า “ดรูเซนชั้นฐาน” (basal laminar drusen) เนื่องจากเป็นความหนาแบบปุ่มของเยื่อฐาน RPE แต่การศึกษาต่อมาพบว่าการสะสมเกิดขึ้นระหว่างเยื่อฐาน RPE และชั้นคอลลาเจนภายในเยื่อบรูค ซึ่งเป็นตำแหน่งเดียวกับดรูเซนชนิดนิ่มทั่วไป ดังนั้น ปัจจุบันจึงแนะนำชื่อ “ดรูเซนคิวติคิวลาร์” (cuticular drusen) 1)
จัดอยู่ในสเปกตรัมจอประสาทตาเสื่อมตามอายุ (AMD) แต่มีลักษณะต่อไปนี้ที่แตกต่างจาก AMD ทั่วไป:
แม้ว่าจะเป็นส่วนหนึ่งของสเปกตรัมของจอประสาทตาเสื่อมตามอายุ แต่ก็มีลักษณะเฉพาะ เช่น การเริ่มต้นในอายุที่ค่อนข้างน้อย พบในเพศหญิงมากกว่า ลักษณะการถ่ายภาพแบบ “ดาวบนฟ้า” และ “ฟันเลื่อย” และความสัมพันธ์ที่แข็งแกร่งกับการกลายพันธุ์ของยีน CFH นอกจากนี้ยังถือเป็นรอยโรคก่อนเกิดของจอประสาทตาเสื่อมตามอายุ และสามารถพัฒนาไปสู่ภาวะแทรกซ้อนที่จุดรับภาพได้เมื่อติดตามระยะยาว 1)
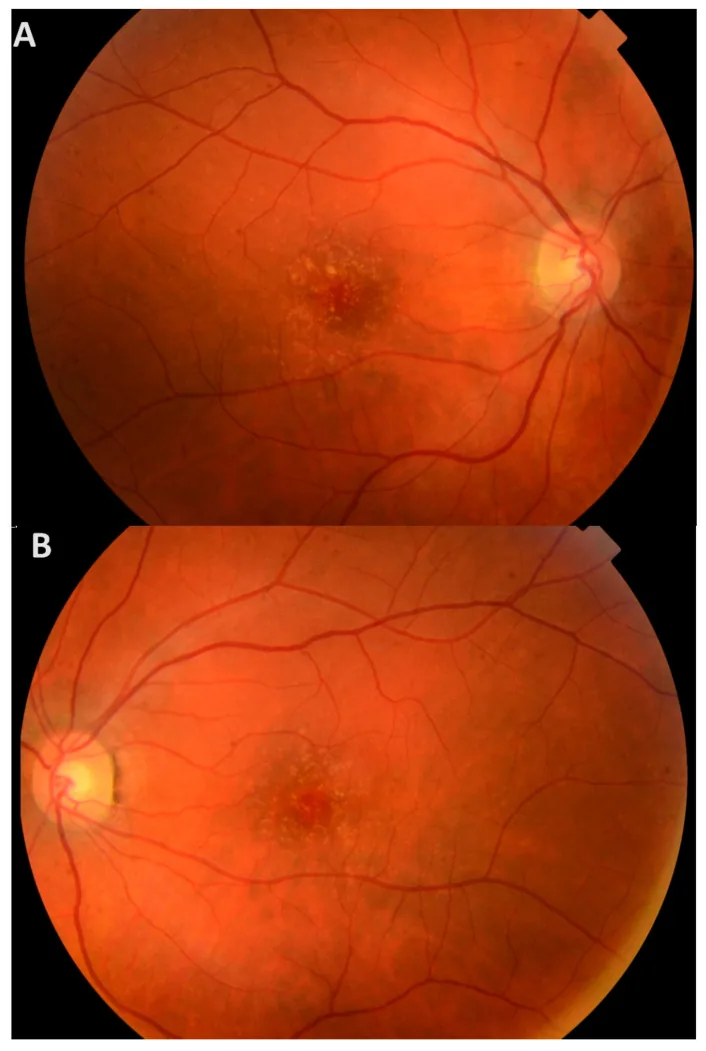
ในระยะแรก อาการที่ผู้ป่วยรับรู้ได้นั้นพบได้น้อย และผู้ป่วยส่วนใหญ่จะไม่มีอาการจนกระทั่งอายุมาก แม้ว่าจะมีดรูเซนที่จุดรับภาพ ก็จะไม่มีอาการหากไม่มีความเสียหายต่อชั้นนอกของจอประสาทตา
หากดรูเซนคงอยู่เป็นเวลานาน ความผิดปกติของเยื่อบุผิวรับแสง (RPE) อาจพัฒนาไปสู่ความเสียหายของชั้นนอกจอประสาทตา เมื่อลุกลามถึงรอยบุ๋มจอประสาทตา จะเกิดอาการต่อไปนี้
ในการตรวจจอประสาทตาภายใต้การขยายม่านตา จะสังเกตเห็นดรูเซนสีเหลืองเล็กๆ จำนวนมากกระจายทั่วจอประสาทตา ดรูเซนเหล่านี้ถูกมองว่าเป็นดรูเซนแข็ง สีขาวเหลือง นูนขึ้นมาใต้ RPE
ฟีโนไทป์ทางคลินิกแบ่งออกเป็นสามประเภท 1)
ฟีโนไทป์ 1
การกระจาย: ชนิดที่กระจุกตัวบริเวณจอประสาทตาส่วนกลาง (macula)
ความเสี่ยงของภาวะแทรกซ้อน: อุบัติการณ์โดยประมาณของ GA ใน 5 ปี เท่ากับ 12.9% ซึ่งต่ำที่สุดใน 3 ชนิด
ฟีโนไทป์ 2
การกระจาย: ชนิดที่กระจายอยู่บริเวณขั้วหลังของลูกตา (posterior pole) และขยายไปยังส่วนปลายและด้านจมูก
ความเสี่ยงของภาวะแทรกซ้อน: อุบัติการณ์โดยประมาณของ GA ใน 5 ปี เท่ากับ 38.7% ความเสี่ยงของ MNV ก็สูงเช่นกัน
ฟีโนไทป์ 3
การกระจาย: ชนิดที่มี drusen ขนาดใหญ่ (>200 μm) ปนอยู่
ความเสี่ยงของภาวะแทรกซ้อน: อุบัติการณ์โดยประมาณของ GA ใน 5 ปี เท่ากับ 43.6% ซึ่งสูงที่สุด
ผลการตรวจทางคลินิกที่สำคัญแสดงไว้ด้านล่าง
ในการตรวจ OCT แบ่งออกเป็น 3 ชนิด1)
สาเหตุของ basal drusen ยังไม่เป็นที่เข้าใจอย่างสมบูรณ์ ปัจจัยเสี่ยงที่ทราบในปัจจุบันมีดังนี้
ปัจจัยทางพันธุกรรม
ความแตกต่างทางเพศและประวัติครอบครัว
ความสัมพันธ์กับโรคทางระบบ
เนื่องจากความผิดปกติของวิถีทางเลือกคอมพลีเมนต์ (complement alternative pathway) จากการกลายพันธุ์ของยีน CFH ทำให้เกิดการสะสมที่คล้ายกันทั้งในตา (ระหว่าง RPE และเยื่อบรูช) และไต (เยื่อฐานโกลเมอรูลัส) โดยเฉพาะในผู้ป่วยอายุน้อย (5–30 ปี) แนะนำให้ตรวจคัดกรอง MPGN และกลุ่มอาการเม็ดเลือดแดงแตกยูรีมิกผิดปกติ (aHUS) 1)
การวินิจฉัยต้องใช้การถ่ายภาพหลายรูปแบบร่วมกัน แนะนำให้ยืนยันด้วยอย่างน้อยสามวิธีจาก: ภาพถ่ายจอตา (CFP), SD-OCT, การถ่ายภาพหลอดเลือดด้วยฟลูออเรสซีน (FA) และการเรืองแสงอัตโนมัติของจอตา (FAF) 1)
ผลการตรวจที่พบบ่อยของแต่ละวิธีแสดงไว้ด้านล่าง
| วิธีการตรวจ | ผลการตรวจที่พบบ่อย | ข้อสังเกตพิเศษ |
|---|---|---|
| ภาพถ่ายจอตา (CFP) | ดรูเซนสีเหลืองเล็กจำนวนมาก | กระจายจากขั้วหลังไปยังส่วนรอบนอก |
| FA | รูปแบบ “ท้องฟ้าเต็มไปด้วยดวงดาว” | จุดเรืองแสงมากมายในระยะหลอดเลือดแดง-ดำ 1) |
| FAF | การเรืองแสงอัตโนมัติต่ำตรงกลางพร้อมขอบเรืองแสงสูง | อัตราการระบุที่แม่นยำ 62% ในกรณีที่มี และ 100% ในกรณีที่ไม่มี 1) |
| SD-OCT | การยกตัวเป็นรูปสามเหลี่ยมของ RPE-BL และรูปแบบ “ฟันเลื่อย” | จำแนกเป็น 3 ประเภท 1) |
การตรวจหลอดเลือดด้วย ICG (ICGA): แสดงการเรืองแสงสูงในระยะแรก แต่ประมาณ 50% ตรวจไม่พบดรูเซน 1)
ประเด็นการวินิจฉัยแยกโรค
ยังไม่มีการรักษาที่ได้รับการยืนยันว่าสามารถทำให้ดรูเซนหายไปได้ สำหรับดรูเซนฐานเดี่ยว ไม่มีข้อบ่งชี้ในการรักษา การติดตามผลเป็นระยะอย่างสม่ำเสมอเป็นพื้นฐาน
มีรายงานอุบัติการณ์ของภาวะแทรกซ้อนดังต่อไปนี้: 1)
แผนการรักษาตามภาวะแทรกซ้อนมีดังนี้:
เมื่อมี CNV ร่วม
การฉีดยา anti-VEGF เข้าในน้ำวุ้นตา: ทางเลือกแรก ใช้ ranibizumab, aflibercept, brolucizumab เป็นต้น
การรักษาด้วยแสงไดนามิก (PDT): พิจารณาเมื่อ anti-VEGF ไม่ได้ผลหรือไม่เหมาะสม
เมื่อมี GA ร่วม
ไม่มีการรักษาที่มีประสิทธิภาพ: ไม่มีวิธีการที่ได้รับการยืนยันในการหยุดการดำเนินโรค
การติดตามผลอย่างต่อเนื่อง: ตรวจร่างกายเป็นประจำเพื่อตรวจหา CNV ตั้งแต่ระยะแรก
รอยโรคแบบไข่แดง
การเฝ้าสังเกต: อาจหายได้เอง
กรณีที่มี CNV: พิจารณาการใช้ยา anti-VEGF
เกี่ยวกับอาหารเสริม
ยังไม่มีการพิสูจน์ประสิทธิภาพของอาหารเสริม AREDS (การศึกษาโรคตาที่เกี่ยวข้องกับอายุ) ในผู้ป่วยดรูเซนชั้นฐาน ตัวอย่างใบสั่งยา AREDS ทั่วไป ได้แก่ Ocuvite PreserVision 2 (3 เม็ด แบ่งรับประทาน 3 ครั้ง) และ Sante Lutax 20+ วิตามินและแร่ธาตุ (3 เม็ด แบ่งรับประทาน 3 ครั้ง)
การติดตามตนเอง
การติดตามประจำวันโดยใช้แผ่นตาอัมสเลอร์สามารถตรวจพบการเปลี่ยนแปลงของภาพบิดเบือนและจุดบอดกลางตาได้ตั้งแต่ระยะแรก
ปัจจุบันยังไม่มีการรักษาที่ทำให้ดรูเซนหายไปเอง หากมี CNV ร่วมด้วย การฉีดยา anti-VEGF เข้าในน้ำวุ้นตา หรือการรักษาด้วยแสงไดนามิก (PDT) เป็นข้อบ่งชี้ สำหรับ GA ยังไม่มีการรักษาที่เป็นมาตรฐาน และการเฝ้าสังเกตอย่างต่อเนื่องเป็นสิ่งสำคัญ ดูรายละเอียดในหัวข้อ “การรักษามาตรฐาน”
ดรูเซนชั้นฐานเป็นสารที่มีรูปร่างหลากหลายซึ่งสะสมอยู่ระหว่างเยื่อฐานของ RPE และชั้นคอลลาเจนด้านในของเยื่อบรูค ส่วนประกอบของมันประกอบด้วยเศษเยื่อหุ้มเซลล์ คอเลสเตอรอลที่ไม่ได้ esterified คอมพลีเมนต์ และอื่นๆ
กลไกการเกิด
RPE มีหน้าที่ขับไลโปโปรตีน แต่เมื่ออายุมากขึ้น เมแทบอลิซึมจะแย่ลง สารนอกเซลล์ที่เสื่อมสภาพจะสะสม ก่อตัวเป็นฐานของดรูเซน การกระตุ้นวิถีคอมพลีเมนต์มากเกินไปจากการกลายพันธุ์ของยีน CFH (โดยเฉพาะ Tyr402His) จะเร่งกระบวนการนี้ 1)
วงจรชีวิตของดรูเซน
ดรูเซนชนิดคิติคูลาร์เป็นสิ่งที่มีการเปลี่ยนแปลงตลอดเวลา โดยมีวงจรการเจริญเติบโต การรวมตัว และการถดถอย 1)
การดำเนินของรอยโรคแบบไข่แดง
รอยโรคแบบไข่แดง (vitelliform lesion) ดำเนินไปตามลำดับต่อไปนี้ 1)
ผู้ที่มีความแปรผันของยีน CFH ที่หายาก (เช่น p.Arg1210Cys) มักมีอาการตั้งแต่อายุน้อยกว่า การกระตุ้นวิถีคอมพลีเมนต์ทางเลือกเรื้อรังมากเกินไปจากการกลายพันธุ์ของยีน CFH เชื่อว่าทำให้เกิดดรูเซนเร็วกว่า AMD ปกติ 1)
การรักษาที่มุ่งเป้าไปที่วิถีคอมพลีเมนต์
เนื่องจากความผิดปกติของวิถีคอมพลีเมนต์ทางเลือกจากการกลายพันธุ์ของยีน CFH เป็นพื้นฐานทางพยาธิวิทยา สารประกอบที่มุ่งเป้าไปที่วิถีคอมพลีเมนต์จึงอยู่ระหว่างการวิจัยอย่างแข็งขัน เนื่องจากการให้ยาทั่วร่างกายมีความเสี่ยงสูงต่อผลข้างเคียง การให้ยาเฉพาะที่ (ภายในตา) จึงเป็นแนวทางที่มีแนวโน้มดี
การพยากรณ์โรคด้วยการถ่ายภาพหลายรูปแบบ
ด้วยความก้าวหน้าของการถ่ายภาพหลายรูปแบบ ทำให้สามารถระบุผู้ป่วยที่มีความเสี่ยงสูงต่อภาวะแทรกซ้อนได้ตั้งแต่เนิ่นๆ 1) การจำแนกฟีโนไทป์ (1-3) มีประโยชน์ในการพยากรณ์โรค โดยฟีโนไทป์ 2 และ 3 เป็นกลุ่มที่มีความเสี่ยงสูงต่อ GA และ MNV ซึ่งต้องได้รับการติดตามอย่างใกล้ชิด 1)
ศักยภาพของการแพทย์เฉพาะบุคคล
ด้วยความก้าวหน้าของการวิเคราะห์ทางพันธุกรรม การแพทย์เฉพาะบุคคลตามความแปรผันของยีนที่เกี่ยวข้องกับ AMD โดยเฉพาะยีน CFH คาดว่าจะเป็นจริงได้ ผู้ที่มีความแปรผันที่หายาก (เช่น p.Arg1210Cys) อาจเป็นเป้าหมายสำหรับการคัดกรองและการแทรกแซงตั้งแต่เนิ่นๆ