Fenotipo 1
Distribuzione: tipo concentrato nella regione maculare.
Rischio di complicanze: incidenza stimata a 5 anni di GA del 12,9%, la più bassa tra i 3 tipi.

Le drusen della lamina basale (basal laminar drusen; BLD) sono un concetto patologico descritto per la prima volta nel 1977 da Gass, che osservò numerosi piccoli drusen gialli disseminati nel fondo oculare. Il pattern a “cielo stellato” all’angiografia con fluoresceina (FA) è caratteristico. 1)
Inizialmente denominate “basal laminar drusen” per un ispessimento nodulare della membrana basale dell’RPE, studi successivi hanno dimostrato che i depositi si trovano tra la membrana basale dell’RPE e lo strato collagenico della membrana di Bruch, cioè nella stessa sede dei tipici drusen molli. Pertanto, ora si raccomanda il termine “cuticular drusen” (drusen cuticolari). 1)
Appartengono allo spettro della degenerazione maculare legata all’età (AMD), ma presentano le seguenti caratteristiche che le distinguono dalla tipica AMD:
Sebbene faccia parte dello spettro della degenerazione maculare legata all’età, presenta caratteristiche distintive come un’età di insorgenza relativamente giovane, una predominanza femminile, reperti di imaging tipici a “cielo stellato” o “a dente di sega”, e una forte associazione con mutazioni del gene CFH. È anche considerata una lesione precursore della DMLE e può progredire verso complicazioni maculari durante il follow-up a lungo termine. 1)
All’inizio i sintomi soggettivi sono rari e la maggior parte dei pazienti rimane asintomatica fino all’età avanzata. Anche se le drusen sono presenti nella macula, rimangono asintomatiche finché non si verifica un danno agli strati esterni della retina.
Quando le drusen persistono a lungo, la disfunzione dell’RPE può progredire verso un danno agli strati esterni della retina. Quando la fovea è coinvolta, compaiono i seguenti sintomi.
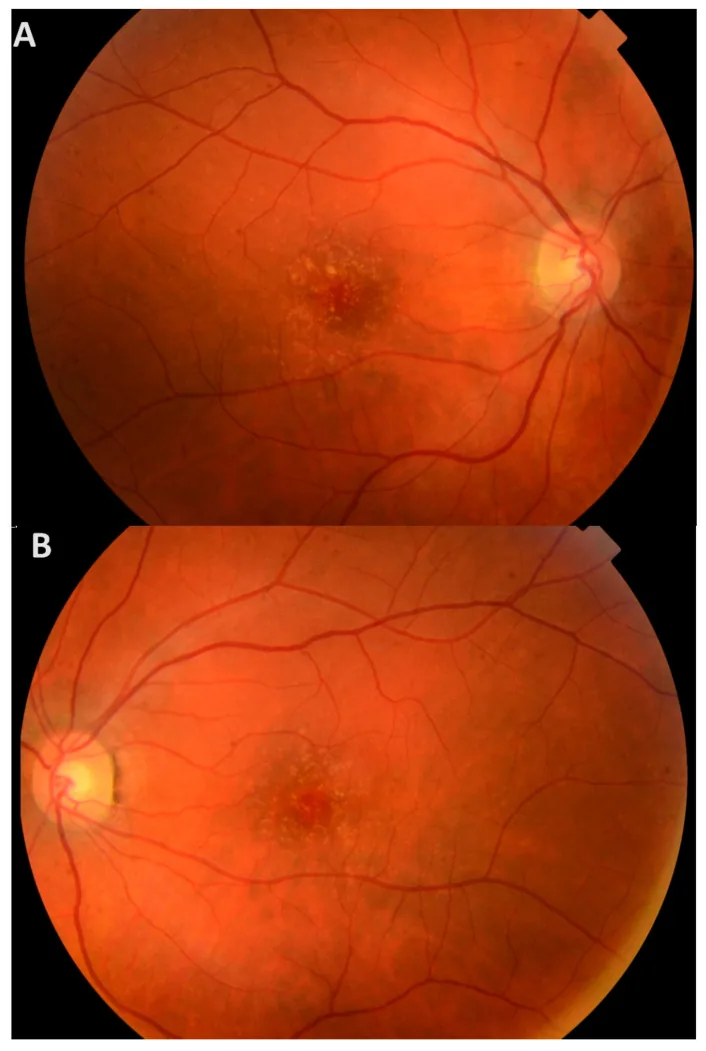
All’esame del fundus sotto dilatazione pupillare si osservano numerose piccole drusen gialle su tutta la retina. Vengono riconosciute come multiple drusen dure, rilevate, di colore giallo-biancastro sotto l’RPE.
Il fenotipo clinico è classificato in tre tipi. 1)
Fenotipo 1
Distribuzione: tipo concentrato nella regione maculare.
Rischio di complicanze: incidenza stimata a 5 anni di GA del 12,9%, la più bassa tra i 3 tipi.
Fenotipo 2
Distribuzione: tipo disperso nel polo posteriore, che si estende verso la periferia e il lato nasale.
Rischio di complicanze: incidenza stimata a 5 anni di GA del 38,7%. Rischio di MNV anche elevato.
Fenotipo 3
Distribuzione: tipo con grandi drusen misti (>200 μm).
Rischio di complicanze: incidenza stimata a 5 anni di GA del 43,6%, la più alta.
I principali reperti clinici sono mostrati di seguito.
All’OCT si classificano tre tipi.1)
L’eziologia dei drusen dello strato basale non è completamente chiarita. I fattori di rischio attualmente noti sono elencati di seguito.
Fattori genetici
Sesso e storia familiare
Associazioni con malattie sistemiche
Ciò è dovuto al fatto che un’anomalia della via alternativa del complemento causata da una mutazione del gene CFH porta alla formazione di depositi simili sia nell’occhio (tra l’EPR e la membrana di Bruch) che nel rene (membrana basale glomerulare). In particolare nei pazienti giovani (5-30 anni), si raccomanda lo screening per MPGN e sindrome emolitico-uremica atipica (aHUS). 1)
La diagnosi combina più modalità di imaging. Si raccomanda la conferma con almeno tre dei seguenti: fotografia del fondo (CFP), SD-OCT, angiografia con fluoresceina (FA) e autofluorescenza del fondo (FAF). 1)
I risultati tipici di ciascun esame sono mostrati di seguito.
| Metodo di esame | Risultati tipici | Note |
|---|---|---|
| Fotografia del fondo (CFP) | Numerosi piccoli drusen gialli | Disseminati dal polo posteriore alla periferia |
| FA | Pattern «cielo stellato» | Numerosi punti iperfluorescenti nella fase artero-venosa1) |
| FAF | Ipoautofluorescenza centrale con bordo iperautofluorescente | Tasso di identificazione corretto del 62% in presenza, 100% in assenza1) |
| SD-OCT | Sollevamento triangolare della RPE-BL, «a dente di sega» | Classificato in 3 tipi1) |
Angiografia con verde di indocianina (ICGA) : mostra iperfluorescenza precoce, ma in circa il 50% dei casi i drusen non sono rilevabili.1)
Punti chiave della diagnosi differenziale
Non esiste una terapia consolidata per far scomparire i drusen stessi. I drusen isolati dello strato basale non richiedono trattamento; il follow-up regolare è la regola.
Sono state riportate le seguenti frequenze di complicanze. 1)
Le strategie terapeutiche specifiche per complicanza sono illustrate di seguito.
In caso di CNV
Iniezione intravitreale di anti-VEGF : terapia di prima linea. Utilizzo di ranibizumab, aflibercept, brolucizumab, ecc.
Terapia fotodinamica (PDT) : considerata in caso di inefficacia o controindicazione agli anti-VEGF.
In caso di GA
Nessuna terapia efficace : non esiste un metodo consolidato per arrestare la progressione.
Monitoraggio continuo : si proseguono esami regolari per la diagnosi precoce di CNV.
Lesioni vitelliformi
Osservazione : può regredire spontaneamente.
Casi con CNV : considerare la terapia anti-VEGF.
Integratori alimentari
L’efficacia degli integratori AREDS (Age-Related Eye Disease Study) nei pazienti con drusen dello strato basale non è stabilita. Esempi di formulazioni AREDS comuni: Ocuvite PreserVision 2 (3 compresse in 3 somministrazioni) o Sante Retax 20+ Vitamina & Minerali (3 compresse in 3 somministrazioni).
Auto-monitoraggio
Il monitoraggio quotidiano con la griglia di Amsler consente di rilevare precocemente i cambiamenti di metamorfopsia e scotoma centrale.
Attualmente non esiste una terapia in grado di far scomparire le drusen stesse. In caso di CNV associata, sono indicate iniezioni intravitreali di anti-VEGF o terapia fotodinamica (PDT). Per la GA non esiste una terapia consolidata ed è importante un follow-up continuo. Per i dettagli, vedere la sezione «Terapia standard».
Le drusen dello strato basale sono depositi polimorfi che si accumulano tra la membrana basale dell’RPE e lo strato di collagene interno della membrana di Bruch. I loro componenti includono residui membranosi, colesterolo non esterificato e complemento.
Meccanismo di formazione
L’RPE è responsabile dell’escrezione delle lipoproteine, ma con l’invecchiamento il suo ricambio metabolico peggiora. La matrice extracellulare degenerata si accumula, formando la base dei drusen. L’iperattivazione della cascata del complemento dovuta alla mutazione del gene CFH (in particolare Tyr402His) accelera questo processo. 1)
Ciclo di vita dei drusen
I drusen cuticolari sono entità dinamiche che attraversano un ciclo di crescita, fusione e regressione. 1)
Evoluzione della lesione vitelliforme
La lesione vitelliforme progredisce nel seguente ordine. 1)
I portatori di varianti rare del gene CFH (come p.Arg1210Cys) tendono a sviluppare la malattia in età più giovane. Si ritiene che l’iperattivazione cronica della via alternativa del complemento dovuta alla mutazione del gene CFH causi la formazione di drusen prima rispetto alla tipica AMD. 1)
Terapie mirate alla via del complemento
Poiché l’anomalia della via alternativa del complemento dovuta a una mutazione del gene CFH è alla base della patologia, i composti che mirano alla via del complemento sono oggetto di attive ricerche. La somministrazione sistemica comporta un alto rischio di effetti collaterali, quindi la somministrazione locale (intraoculare) è considerata un approccio promettente.
Previsione prognostica mediante imaging multimodale
I progressi nell’imaging multimodale stanno consentendo l’identificazione precoce dei pazienti ad alto rischio di complicanze. 1) La classificazione fenotipica (1-3) è utile per la previsione prognostica; i fenotipi 2 e 3 sono gruppi ad alto rischio di GA e MNV e richiedono un follow-up particolarmente rigoroso. 1)
Possibilità di medicina personalizzata
I progressi nell’analisi genetica fanno sperare nella realizzazione di una medicina personalizzata basata sulle varianti dei geni associati alla AMD, incluso il gene CFH. In particolare, i portatori di varianti rare (come p.Arg1210Cys) potrebbero essere bersaglio di screening e intervento precoci.