Kiểu hình 1
Phân bố: Dạng tập trung ở vùng hoàng điểm.
Nguy cơ biến chứng: Tỷ lệ mắc GA ước tính trong 5 năm là 12,9%, thấp nhất trong 3 dạng.

Drusen lớp đáy (basal laminar drusen; BLD) là một khái niệm bệnh được Gass mô tả lần đầu vào năm 1977 với nhiều drusen nhỏ màu vàng rải rác ở đáy mắt. Hình ảnh “sao trên bầu trời” trên chụp mạch huỳnh quang (FA) là đặc trưng. 1)
Ban đầu được đặt tên là “drusen lớp đáy” (basal laminar drusen) như một sự dày lên dạng nốt của màng đáy RPE, nhưng các nghiên cứu sau đó cho thấy sự lắng đọng xảy ra giữa màng đáy RPE và lớp collagen trong màng Bruch, tức là cùng vị trí với drusen mềm thông thường. Do đó, tên gọi “drusen cuticular” hiện được khuyến nghị. 1)
Thuộc phổ thoái hóa hoàng điểm liên quan đến tuổi (AMD), nhưng có các đặc điểm sau khác với AMD điển hình:
Mặc dù là một phần của phổ thoái hóa điểm vàng liên quan đến tuổi tác, nhưng nó có các đặc điểm riêng như khởi phát tương đối trẻ hơn, ưu thế nữ giới, hình ảnh đặc trưng “sao trên trời” và “răng cưa”, và liên quan chặt chẽ với đột biến gen CFH. Nó cũng được coi là tổn thương tiền thân của thoái hóa điểm vàng liên quan đến tuổi tác và có thể tiến triển thành các biến chứng điểm vàng khi theo dõi lâu dài. 1)
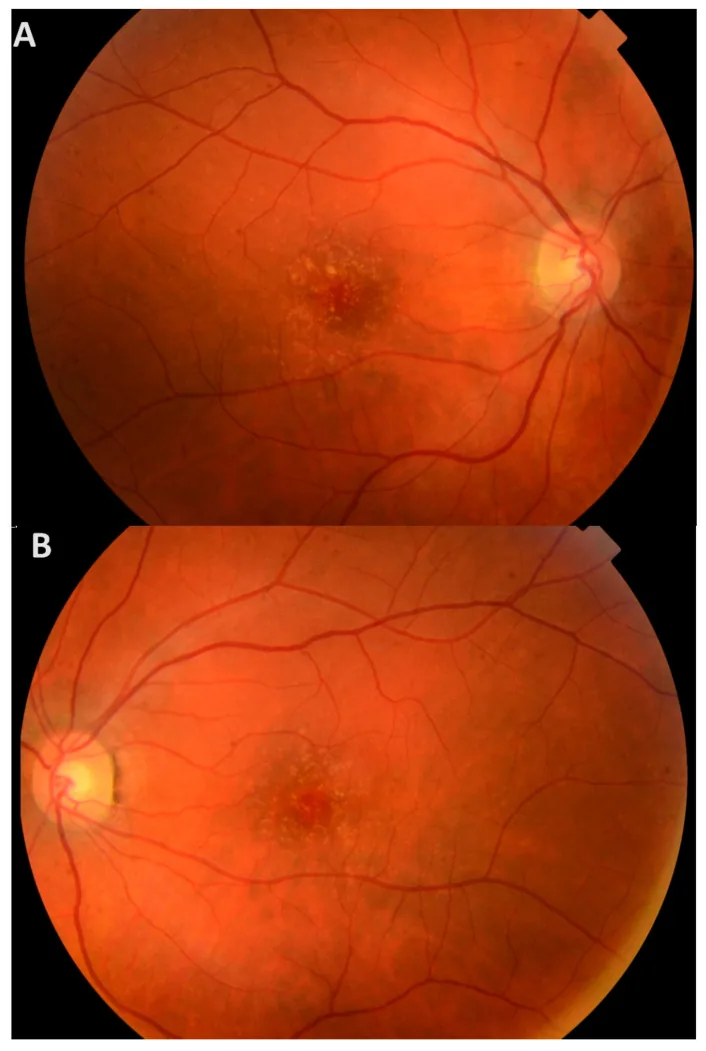
Ở giai đoạn đầu, triệu chứng chủ quan hiếm gặp, và hầu hết bệnh nhân không có triệu chứng cho đến tuổi già. Ngay cả khi có drusen ở điểm vàng, sẽ không có triệu chứng nếu không có tổn thương các lớp ngoài võng mạc.
Nếu drusen tồn tại trong thời gian dài, rối loạn chức năng biểu mô sắc tố võng mạc (RPE) có thể tiến triển thành tổn thương các lớp ngoài võng mạc. Khi lan đến hố trung tâm, các triệu chứng sau xuất hiện.
Khi khám đáy mắt với đồng tử giãn, quan sát thấy nhiều drusen nhỏ màu vàng rải rác khắp võng mạc. Chúng được nhận biết là các drusen cứng, nổi cao, màu trắng vàng dưới RPE.
Kiểu hình lâm sàng được phân loại thành ba loại. 1)
Kiểu hình 1
Phân bố: Dạng tập trung ở vùng hoàng điểm.
Nguy cơ biến chứng: Tỷ lệ mắc GA ước tính trong 5 năm là 12,9%, thấp nhất trong 3 dạng.
Kiểu hình 2
Phân bố: Dạng rải rác ở cực sau, lan ra ngoại vi và phía mũi.
Nguy cơ biến chứng: Tỷ lệ mắc GA ước tính trong 5 năm là 38,7%. Nguy cơ MNV cũng cao.
Kiểu hình 3
Phân bố: Dạng có lẫn các drusen lớn (>200 μm).
Nguy cơ biến chứng: Tỷ lệ mắc GA ước tính trong 5 năm là 43,6%, cao nhất.
Các dấu hiệu lâm sàng chính được trình bày dưới đây.
Trên OCT, được phân loại thành ba dạng.1)
Nguyên nhân của drusen nền chưa được hiểu rõ hoàn toàn. Các yếu tố nguy cơ hiện được biết đến được liệt kê dưới đây.
Yếu tố Di truyền
Khác biệt Giới tính và Tiền sử Gia đình
Liên quan với Bệnh Toàn thân
Điều này là do bất thường con đường thay thế bổ thể (complement alternative pathway) do đột biến gen CFH dẫn đến hình thành các lắng đọng tương tự ở cả mắt (giữa RPE và màng Bruch) và thận (màng đáy cầu thận). Đặc biệt ở bệnh nhân trẻ (5–30 tuổi), khuyến cáo tầm soát MPGN và hội chứng urê huyết tán huyết không điển hình (aHUS). 1)
Chẩn đoán cần kết hợp nhiều phương thức hình ảnh. Khuyến cáo xác nhận bằng ít nhất ba trong số: chụp ảnh đáy mắt (CFP), SD-OCT, chụp mạch huỳnh quang (FA) và tự huỳnh quang đáy mắt (FAF). 1)
Các dấu hiệu điển hình của từng xét nghiệm được trình bày dưới đây.
| Phương pháp xét nghiệm | Dấu hiệu điển hình | Ghi chú đặc biệt |
|---|---|---|
| Chụp ảnh đáy mắt (CFP) | Nhiều drusen nhỏ màu vàng | Rải rác từ cực sau ra ngoại vi |
| FA | Hình ảnh “bầu trời đầy sao” | Nhiều điểm tăng huỳnh quang ở thì động-tĩnh mạch 1) |
| FAF | Tự phát huỳnh quang trung tâm thấp kèm viền tăng huỳnh quang | Tỷ lệ xác định chính xác 62% ở trường hợp có, 100% ở trường hợp không có 1) |
| SD-OCT | Chỗ lồi hình tam giác của RPE-BL và hình “răng cưa” | Phân loại thành 3 loại 1) |
Chụp mạch ICG (ICGA): Có tăng huỳnh quang sớm, nhưng khoảng 50% không phát hiện được drusen. 1)
Điểm chẩn đoán phân biệt
Chưa có phương pháp điều trị nào được thiết lập để loại bỏ drusen. Đối với drusen nền đơn độc, không có chỉ định điều trị, theo dõi định kỳ thường xuyên là cơ bản.
Tỷ lệ mắc các biến chứng sau đã được báo cáo: 1)
Dưới đây là kế hoạch điều trị theo từng biến chứng:
Khi có CNV kèm theo
Tiêm nội nhãn kháng VEGF: Lựa chọn đầu tiên. Sử dụng ranibizumab, aflibercept, brolucizumab, v.v.
Liệu pháp quang động (PDT): Được xem xét khi kháng VEGF không hiệu quả hoặc không phù hợp.
Khi có GA kèm theo
Không có điều trị hiệu quả: Không có phương pháp nào được thiết lập để ngăn chặn tiến triển.
Theo dõi liên tục: Tiếp tục khám định kỳ để phát hiện sớm sự xuất hiện của CNV.
Tổn thương dạng noãn hoàng
Theo dõi: Có thể tự thoái lui.
Trường hợp có CNV: Cân nhắc chỉ định thuốc kháng VEGF.
Về thực phẩm bổ sung
Hiệu quả của thực phẩm bổ sung AREDS (Nghiên cứu bệnh mắt liên quan đến tuổi) ở bệnh nhân drusen nền chưa được thiết lập. Các ví dụ về đơn AREDS phổ biến bao gồm Ocuvite PreserVision 2 (3 viên, chia 3 lần) và Sante Lutax 20+ Vitamin & Khoáng chất (3 viên, chia 3 lần).
Tự theo dõi
Theo dõi hàng ngày bằng lưới Amsler có thể phát hiện sớm các thay đổi về rối loạn thị giác và ám điểm trung tâm.
Hiện tại không có phương pháp điều trị nào làm biến mất drusen. Khi có CNV, tiêm nội nhãn kháng VEGF hoặc liệu pháp quang động (PDT) được chỉ định. Đối với GA, chưa có phương pháp điều trị xác lập, và việc theo dõi liên tục là quan trọng. Xem phần “Phương pháp điều trị tiêu chuẩn” để biết chi tiết.
Drusen nền là chất đa hình tích tụ giữa màng đáy RPE và lớp collagen trong của màng Bruch. Các thành phần của nó bao gồm mảnh vụn màng, cholesterol không ester hóa, bổ thể và các chất khác.
Cơ chế hình thành
RPE chịu trách nhiệm bài tiết lipoprotein, nhưng khi lão hóa, quá trình trao đổi chất của nó trở nên tồi tệ hơn. Chất nền ngoại bào thoái hóa tích tụ, tạo nền cho drusen. Sự hoạt hóa quá mức dòng thác bổ thể do đột biến gen CFH (đặc biệt là Tyr402His) làm tăng tốc quá trình này. 1)
Vòng đời của Drusen
Drusen dạng cuticular là những thực thể động, lặp lại chu kỳ tăng trưởng, hợp nhất và thoái lui. 1)
Diễn tiến của tổn thương dạng noãn hoàng
Tổn thương dạng noãn hoàng (vitelliform lesion) tiến triển theo thứ tự sau. 1)
Người mang biến thể hiếm của gen CFH (ví dụ p.Arg1210Cys) có xu hướng khởi phát bệnh ở độ tuổi trẻ hơn. Sự hoạt hóa quá mức mãn tính của con đường bổ thể thay thế do đột biến gen CFH được cho là gây ra sự hình thành drusen sớm hơn so với AMD thông thường. 1)
Liệu pháp nhắm vào con đường bổ thể
Vì sự bất thường của con đường bổ thể thay thế do đột biến gen CFH là cơ sở bệnh lý, các hợp chất nhắm vào con đường bổ thể đang được nghiên cứu tích cực. Do nguy cơ tác dụng phụ cao khi dùng toàn thân, đường dùng tại chỗ (trong mắt) được coi là một phương pháp đầy hứa hẹn.
Dự đoán tiên lượng bằng hình ảnh đa phương thức
Với sự tiến bộ của hình ảnh đa phương thức, việc xác định sớm bệnh nhân có nguy cơ biến chứng cao đã trở nên khả thi. 1) Phân loại kiểu hình (1-3) hữu ích cho dự đoán tiên lượng, trong đó kiểu hình 2 và 3 là nhóm nguy cơ cao cho GA và MNV, cần được theo dõi chặt chẽ. 1)
Tiềm năng của y học cá thể hóa
Với sự tiến bộ của phân tích di truyền, y học cá thể hóa dựa trên các biến thể của gen liên quan đến AMD, đặc biệt là gen CFH, được kỳ vọng sẽ trở thành hiện thực. Những người mang biến thể hiếm (như p.Arg1210Cys) có thể là mục tiêu cho sàng lọc và can thiệp sớm.