Phénotype 1
Distribution : type concentré dans la région maculaire.
Risque de complications : incidence estimée de GA à 5 ans de 12,9 %, la plus faible des 3 types.

Les drusen de la lame basale (basal laminar drusen ; BLD) sont un concept pathologique décrit pour la première fois en 1977 par Gass, qui a observé de nombreux petits drusen jaunes disséminés dans le fond d’œil. L’aspect en « ciel étoilé » à l’angiographie à la fluorescéine (FA) est caractéristique. 1)
Initialement nommés « basal laminar drusen » en raison d’un épaississement nodulaire de la membrane basale de l’EPR, des études ultérieures ont montré que les dépôts se situent entre la membrane basale de l’EPR et la couche collagène interne de la membrane de Bruch, c’est-à-dire au même endroit que les drusen mous typiques. Ainsi, le terme « cuticular drusen » (drusen cuticulaires) est désormais recommandé. 1)
Ils appartiennent au spectre de la dégénérescence maculaire liée à l’âge (DMLA), mais présentent les caractéristiques suivantes qui les distinguent de la DMLA typique :
Bien qu’elle fasse partie du spectre de la dégénérescence maculaire liée à l’âge, elle présente des caractéristiques distinctives telles qu’un âge d’apparition relativement jeune, une prédominance féminine, des signes d’imagerie typiques en “ciel étoilé” ou “dents de scie”, et une forte association avec les mutations du gène CFH. Elle est également considérée comme une lésion précurseur de la DMLA et peut évoluer vers des complications maculaires lors d’un suivi à long terme. 1)
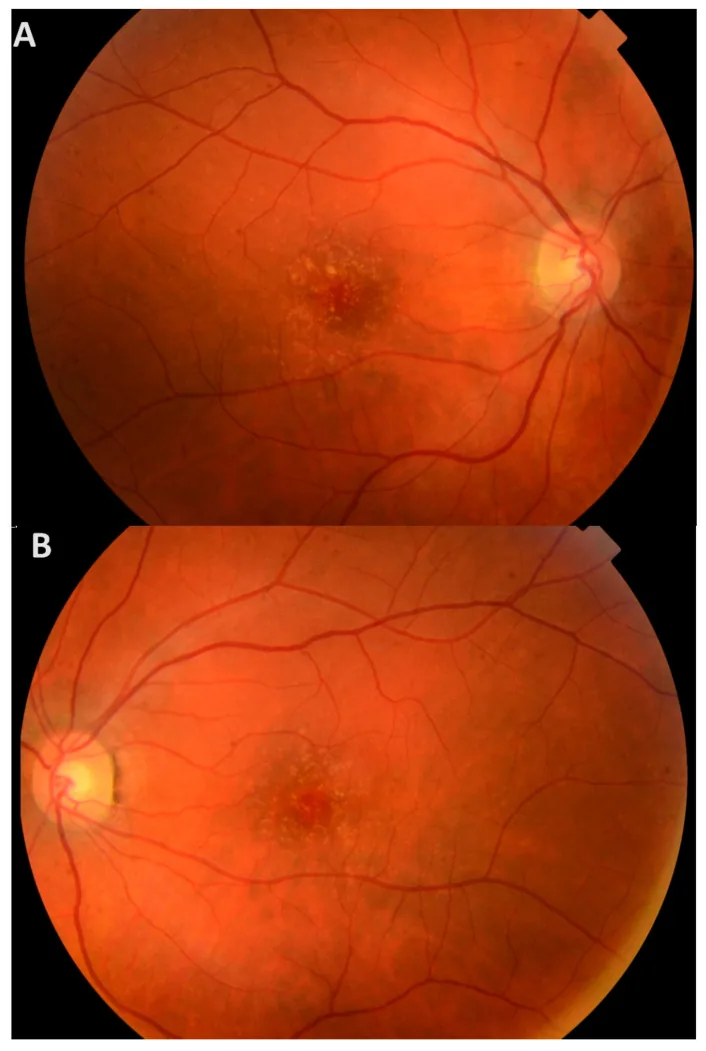
Au début, les symptômes subjectifs sont rares et la plupart des patients restent asymptomatiques jusqu’à un âge avancé. Même si des drusen sont présentes dans la macula, elles sont asymptomatiques tant qu’il n’y a pas de lésion des couches externes de la rétine.
Lorsque les drusen persistent longtemps, un dysfonctionnement de l’EPR peut évoluer vers une atteinte des couches externes de la rétine. Lorsque la fovéa est touchée, les symptômes suivants apparaissent.
L’examen du fond d’œil sous dilatation pupillaire révèle de nombreuses petites drusen jaunes réparties sur toute la rétine. Elles sont perçues comme de multiples drusen dures, surélevées, de couleur blanc-jaunâtre sous l’EPR.
Le phénotype clinique est classé en trois types. 1)
Phénotype 1
Distribution : type concentré dans la région maculaire.
Risque de complications : incidence estimée de GA à 5 ans de 12,9 %, la plus faible des 3 types.
Phénotype 2
Distribution : type dispersé dans le pôle postérieur, s’étendant vers la périphérie et le côté nasal.
Risque de complications : incidence estimée de GA à 5 ans de 38,7 %. Risque de MNV également élevé.
Phénotype 3
Distribution : type avec de grandes drusen (>200 μm) mélangées.
Risque de complications : incidence estimée de GA à 5 ans de 43,6 %, la plus élevée.
Les principales observations cliniques sont présentées ci-dessous.
En OCT, trois types sont classés.1)
L’étiologie des drusen de la couche basale n’est pas complètement élucidée. Les facteurs de risque actuellement connus sont présentés ci-dessous.
Facteurs génétiques
Sexe et antécédents familiaux
Associations avec des maladies systémiques
Cela est dû au fait qu’une anomalie de la voie alterne du complément causée par une mutation du gène CFH entraîne la formation de dépôts similaires à la fois dans l’œil (entre l’EPR et la membrane de Bruch) et dans le rein (membrane basale glomérulaire). En particulier chez les jeunes patients (5 à 30 ans), un dépistage de la MPGN et du syndrome hémolytique et urémique atypique (SHUa) est recommandé. 1)
Le diagnostic combine plusieurs modalités d’imagerie. Il est recommandé de confirmer par au moins trois des examens suivants : photographie du fond d’œil (CFP), SD-OCT, angiographie à la fluorescéine (FA) et autofluorescence du fond d’œil (FAF). 1)
Les résultats typiques de chaque examen sont présentés ci-dessous.
| Méthode d’examen | Résultats typiques | Remarques |
|---|---|---|
| Photographie du fond d’œil (CFP) | Nombreux petits drusen jaunes | Disséminés du pôle postérieur à la périphérie |
| FA | Motif « ciel étoilé » | Nombreux points hyperfluorescents dans les phases artério-veineuses1) |
| FAF | Hypoautofluorescence centrale avec bord hyperautofluorescent | Taux d’identification correct de 62 % en présence, 100 % en absence1) |
| SD-OCT | Élévation triangulaire de la RPE-BL, aspect « en dents de scie » | Classé en 3 types1) |
Angiographie au vert d’indocyanine (ICGA) : hyperfluorescence précoce, mais les drusen ne sont pas détectables dans environ 50 % des cas.1)
Points clés du diagnostic différentiel
Il n’existe pas de traitement établi pour faire disparaître les drusen eux-mêmes. Les drusen de la couche basale isolés ne nécessitent pas de traitement ; une surveillance régulière est la règle.
Les fréquences de complications suivantes ont été rapportées. 1)
Les stratégies de traitement en fonction des complications sont présentées ci-dessous.
En cas de CNV
Injections intravitréennes d’anti-VEGF : traitement de première intention. Utilisation de ranibizumab, aflibercept, brolucizumab, etc.
Thérapie photodynamique (PDT) : envisagée en cas d’inefficacité ou de contre-indication aux anti-VEGF.
En cas d'AG
Aucun traitement efficace : il n’existe pas de méthode établie pour arrêter la progression.
Surveillance continue : des examens réguliers sont poursuivis pour détecter précocement l’apparition d’une CNV.
Lésions vitelliformes
Surveillance : peut régresser spontanément.
Cas avec CNV : envisager un traitement anti-VEGF.
À propos des compléments alimentaires
L’efficacité des compléments AREDS (Age-Related Eye Disease Study) chez les patients présentant des drusen de la couche basale n’est pas établie. Exemples de formulations AREDS courantes : Ocuvite PreserVision 2 (3 comprimés en 3 prises) ou Sante Retax 20+ Vitamine & Minéraux (3 comprimés en 3 prises).
Auto-surveillance
La surveillance quotidienne à l’aide de la grille d’Amsler permet de détecter précocement les changements de métamorphopsie et de scotome central.
Il n’existe actuellement aucun traitement pour faire disparaître les drusen eux-mêmes. En cas de CNV associée, les injections intravitréennes d’anti-VEGF ou la thérapie photodynamique (PDT) sont indiquées. Il n’existe pas de traitement établi pour la GA, et une surveillance continue est importante. Voir la section « Traitement standard » pour plus de détails.
Les drusen de la couche basale sont des dépôts polymorphes qui s’accumulent entre la membrane basale de l’EPR et la couche collagène interne de la membrane de Bruch. Leurs composants comprennent des débris membranaires, du cholestérol non estérifié et du complément.
Mécanisme de formation
L’EPR assure la fonction d’excrétion des lipoprotéines, mais avec l’âge, son renouvellement se détériore. La matrice extracellulaire dégénérée s’accumule, formant la base des drusen. L’hyperactivation de la cascade du complément due à la mutation du gène CFH (notamment Tyr402His) accélère ce processus. 1)
Cycle de vie des drusen
Les drusen cuticulaires sont des entités dynamiques qui subissent un cycle de croissance, de fusion et de régression. 1)
Évolution de la lésion vitelliforme
La lésion vitelliforme progresse dans l’ordre suivant. 1)
Les porteurs de variants rares du gène CFH (tels que p.Arg1210Cys) ont tendance à développer la maladie plus jeunes. On pense que l’hyperactivation chronique de la voie alterne du complément due à la mutation du gène CFH provoque la formation de drusen plus tôt que dans la DMLA typique. 1)
Traitements ciblant la voie du complément
Étant donné que l’anomalie de la voie alterne du complément due à une mutation du gène CFH est à la base de la pathologie, des composés ciblant la voie du complément font l’objet de recherches actives. L’administration systémique présentant un risque élevé d’effets secondaires, l’administration locale (intraoculaire) est considérée comme une approche prometteuse.
Prédiction du pronostic par imagerie multimodale
Les progrès de l’imagerie multimodale permettent d’identifier de plus en plus tôt les patients à haut risque de complications. 1) La classification phénotypique (1 à 3) est utile pour la prédiction du pronostic ; les phénotypes 2 et 3 sont des groupes à haut risque de GA et de MNV, nécessitant une surveillance particulièrement stricte. 1)
Possibilités de médecine personnalisée
Les progrès de l’analyse génétique laissent espérer la réalisation d’une médecine personnalisée basée sur les variants des gènes liés à la DMLA, notamment le gène CFH. En particulier, les porteurs de variants rares (tels que p.Arg1210Cys) pourraient être ciblés pour un dépistage et une intervention précoces.