النمط الظاهري 1
التوزيع: نمط يتركز في منطقة البقعة.
خطر المضاعفات: معدل الإصابة التقديري لـ GA خلال 5 سنوات هو 12.9%، وهو الأدنى بين الأنواع الثلاثة.

الدرز القاعدي (basal laminar drusen; BLD) هو مفهوم مرض وصفه غاس لأول مرة في عام 1977 على أنه العديد من الدرزات الصفراء الصغيرة المنتشرة في قاع العين. يتميز بنمط “النجوم في السماء” في تصوير الأوعية الفلوريسيني (FA). 1)
في البداية، سُمي “الدرز القاعدي” (basal laminar drusen) باعتباره سماكة عقيدية للغشاء القاعدي للظهارة الصباغية الشبكية، لكن الأبحاث اللاحقة أظهرت أن الترسب يحدث بين الغشاء القاعدي للظهارة الصباغية الشبكية والطبقة الكولاجينية داخل غشاء بروخ، أي نفس موقع الدرز اللين المعتاد. ولهذا، يُوصى حاليًا باسم “الدرز الجلدي” (cuticular drusen). 1)
ينتمي إلى طيف التنكس البقعي المرتبط بالعمر (AMD)، لكنه يتميز بالخصائص التالية المختلفة عن التنكس البقعي النمطي:
على الرغم من أنه جزء من طيف التنكس البقعي المرتبط بالعمر، إلا أنه يتميز بخصائص فريدة مثل الظهور في سن مبكرة نسبيًا وغلبة الإناث، ونتائج التصوير المميزة “نجوم في السماء” و”سن المنشار”، والارتباط القوي بطفرات جين CFH. كما يُعتبر آفة سابقة للتنكس البقعي المرتبط بالعمر، وقد يتطور إلى مضاعفات بقعية مع المتابعة طويلة الأمد. 1)
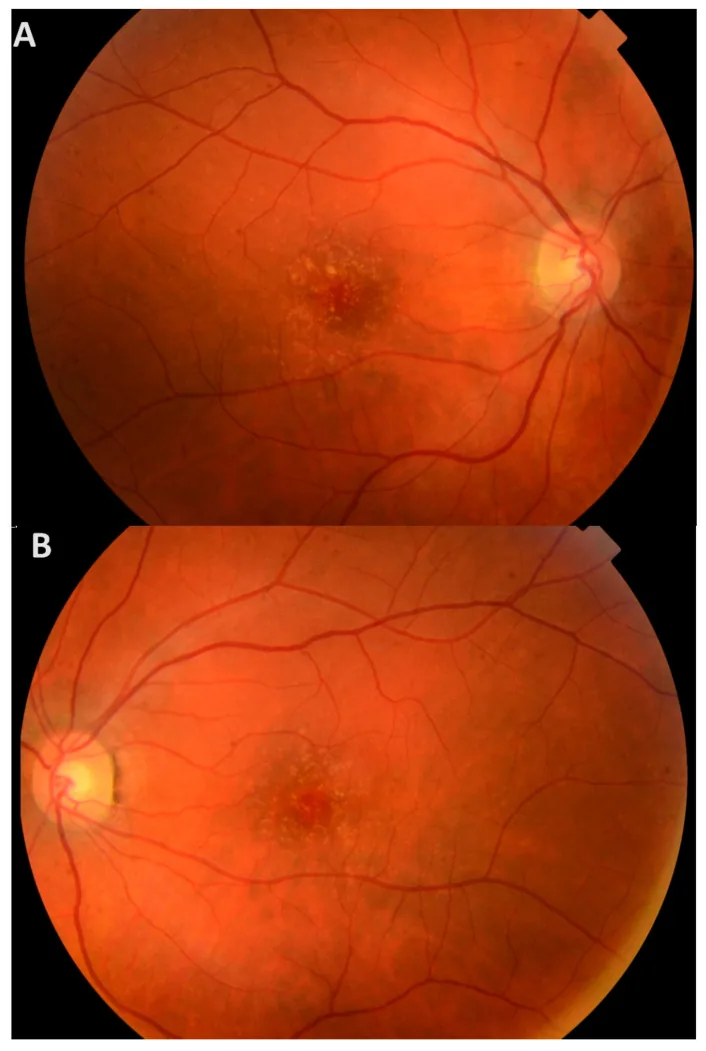
في المراحل المبكرة، تكون الأعراض الذاتية نادرة، ويظل معظم المرضى بدون أعراض حتى سن متأخرة. حتى في حالة وجود درزن في البقعة، لا تظهر أعراض إذا لم يحدث تلف في الطبقات الخارجية للشبكية.
عند استمرار وجود الدرزن لفترة طويلة، يتطور الأمر من خلل وظيفي في الظهارة الصباغية للشبكية إلى تلف في الطبقات الخارجية للشبكية. عندما يمتد إلى النقرة، تظهر الأعراض التالية.
في فحص قاع العين تحت التوسيع، يُلاحظ وجود العديد من الدرزن الصفراء الصغيرة المنتشرة في جميع أنحاء الشبكية. يتم التعرف عليها كدرزن صلبة مرتفعة صفراء-بيضاء تحت الظهارة الصباغية للشبكية.
يُصنف النمط الظاهري السريري إلى ثلاثة أنواع. 1)
النمط الظاهري 1
التوزيع: نمط يتركز في منطقة البقعة.
خطر المضاعفات: معدل الإصابة التقديري لـ GA خلال 5 سنوات هو 12.9%، وهو الأدنى بين الأنواع الثلاثة.
النمط الظاهري 2
التوزيع: نمط منتشر في القطب الخلفي، يمتد إلى المحيط والجانب الأنفي.
خطر المضاعفات: معدل الإصابة التقديري لـ GA خلال 5 سنوات هو 38.7%. خطر MNV مرتفع أيضًا.
النمط الظاهري 3
التوزيع: نمط تختلط فيه دروزات كبيرة (>200 ميكرومتر).
خطر المضاعفات: معدل الإصابة التقديري لـ GA خلال 5 سنوات هو 43.6%، وهو الأعلى.
فيما يلي أهم النتائج السريرية.
في OCT، تُصنف إلى ثلاثة أنواع.1)
لم يتم فهم سبب الدروز القاعدي بشكل كامل. فيما يلي عوامل الخطر المعروفة حاليًا.
العوامل الوراثية
الفروق الجنسية والتاريخ العائلي
الارتباط بالأمراض الجهازية
يرجع ذلك إلى أن خلل المسار البديل للمتممة (complement alternative pathway) الناتج عن طفرة جين CFH يؤدي إلى تكوين رواسب مماثلة في كل من العين (بين الظهارة الصباغية للشبكية وغشاء بروخ) والكلى (الغشاء القاعدي الكبيبي). خاصة في المرضى الصغار (5-30 سنة)، يُوصى بإجراء فحص لالتهاب كبيبات الكلى الغشائي التكاثري (MPGN) ومتلازمة انحلال الدم اليوريمية غير النمطية (aHUS). 1)
يعتمد التشخيص على الجمع بين عدة طرائق تصويرية. يُوصى بالتأكيد باستخدام ثلاثة على الأقل من: تصوير قاع العين (CFP)، التصوير المقطعي التوافقي البصري ذو المجال الطيفي (SD-OCT)، تصوير الأوعية بالفلوريسين (FA)، والتصوير الذاتي الفلوري لقاع العين (FAF). 1)
فيما يلي النتائج النموذجية لكل فحص:
| طريقة الفحص | النتائج النموذجية | ملاحظات خاصة |
|---|---|---|
| تصوير قاع العين (CFP) | براريق صفراء صغيرة متعددة | منتشرة من القطب الخلفي إلى المحيط |
| FA | نمط “السماء المرصعة بالنجوم” | نقاط مفرطة التألق متعددة في الطور الشرياني الوريدي 1) |
| FAF | تألق ذاتي منخفض مركزي مع حافة مفرطة التألق | معدل تحديد دقيق 62% في الحالات الموجودة و100% في الحالات غير الموجودة 1) |
| SD-OCT | ارتفاع مثلثي لـ RPE-BL ونمط “سن المنشار” | مصنف إلى 3 أنواع 1) |
تصوير الأوعية بالصبغة الخضراء (ICGA): يظهر تألقًا مبكرًا، ولكن حوالي 50% لا يمكن اكتشاف البراريق فيها. 1)
نقاط التشخيص التفريقي
لا يوجد علاج مثبت لإزالة الدرزون نفسه. بالنسبة للدرزون القاعدي المنفرد، لا توجد مؤشرات للعلاج، والمتابعة الدورية المنتظمة هي الأساس.
تم الإبلاغ عن معدلات حدوث المضاعفات التالية: 1)
فيما يلي خطة العلاج حسب المضاعفات:
عند وجود CNV
الحقن داخل الزجاجي لمضاد VEGF: الخيار الأول. يستخدم رانيبيزوماب، أفليبيرسيبت، برولوسيزوماب وغيرها.
العلاج الضوئي الديناميكي (PDT): يُنظر فيه عندما يكون مضاد VEGF غير فعال أو غير مناسب.
عند وجود GA
لا يوجد علاج فعال: لا توجد طريقة مثبتة لوقف التقدم.
المتابعة المستمرة: استمرار الفحوصات المنتظمة للكشف المبكر عن ظهور CNV.
الآفات الصفارية
المراقبة: قد يحدث تراجع تلقائي.
حالات المصاحبة لـ CNV: النظر في استخدام مضادات VEGF.
حول المكملات الغذائية
لم تثبت فعالية مكملات AREDS (دراسة أمراض العيون المرتبطة بالعمر) لمرضى الدرن القاعدي. من أمثلة وصفات AREDS الشائعة: Ocuvite PreserVision 2 (3 أقراص مقسمة على 3 جرعات) و Sante Lutax 20+ فيتامين ومعادن (3 أقراص مقسمة على 3 جرعات).
المراقبة الذاتية
يمكن للمراقبة اليومية باستخدام شبكة آمسلر أن تكشف مبكرًا عن تغيرات في تشوه الرؤية والعتمة المركزية.
لا يوجد حاليًا علاج يزيل الدرن نفسه. في حالة حدوث CNV، يُستخدم الحقن داخل الزجاجي لمضادات VEGF أو العلاج الضوئي الديناميكي (PDT). لا يوجد علاج مثبت للضمور الجغرافي، وتكون المراقبة المستمرة مهمة. راجع قسم «العلاج القياسي» للتفاصيل.
الدرن القاعدي هو مادة متعددة الأشكال تتراكم بين الغشاء القاعدي للخلايا الصبغية الشبكية والطبقة الكولاجينية الداخلية لغشاء بروخ. تتكون مكوناته من بقايا غشائية وكوليسترول غير أستري ومتممة وغيرها.
آلية التكوين
تتحمل RPE وظيفة إفراز البروتينات الدهنية، ولكن مع تقدم العمر، يتدهور التمثيل الغذائي لها. تتراكم المادة خارج الخلية المتغيرة، مما يشكل أساس البراريق. يؤدي التنشيط المفرط لسلسلة المتممة بسبب طفرة جين CFH (خاصة Tyr402His) إلى تسريع هذه العملية. 1)
دورة حياة البراريق
البراريق الجلدية هي كيانات ديناميكية، تتكرر دورة النمو والاندماج والانحدار. 1)
مسار الآفة الصفراوية
تتقدم الآفة الصفراوية (vitelliform lesion) بالترتيب التالي. 1)
يميل حاملو المتغيرات النادرة لجين CFH (مثل p.Arg1210Cys) إلى الإصابة في سن أصغر. يُعتقد أن التنشيط المفرط المزمن للمسار البديل للمتممة بسبب طفرة جين CFH يؤدي إلى تكوين البراريق في وقت أبكر من AMD العادي. 1)
العلاج الموجه للمسار المتمم
نظرًا لأن خلل المسار البديل للمتمم الناتج عن طفرات جين CFH هو الأساس المرضي، فإن المركبات التي تستهدف المسار المتمم قيد البحث النشط. نظرًا لارتفاع خطر الآثار الجانبية للإعطاء الجهازي، يُعتبر الإعطاء الموضعي (داخل العين) نهجًا واعدًا.
التنبؤ بالتشخيص باستخدام التصوير متعدد الوسائط
بفضل التقدم في التصوير متعدد الوسائط، أصبح من الممكن تحديد المرضى ذوي المخاطر العالية للمضاعفات مبكرًا. 1) تصنيف النمط الظاهري (1-3) مفيد للتنبؤ بالتشخيص، حيث أن النمطين 2 و3 هما مجموعتان عاليتا الخطورة للضمور الجغرافي والأوعية الدموية الجديدة المشيمية، وتتطلبان متابعة دقيقة بشكل خاص. 1)
إمكانية الطب الشخصي
مع التقدم في التحليل الجيني، يُتوقع تحقيق الطب الشخصي بناءً على المتغيرات في جينات AMD المرتبطة، وخاصة جين CFH. حاملو المتغيرات النادرة (مثل p.Arg1210Cys) قد يكونون أهدافًا للفحص المبكر والتدخل.