Fenotipo 1
Distribución: Tipo concentrado en el área macular.
Riesgo de complicaciones: El más bajo de los tres tipos, con una incidencia estimada a 5 años de GA del 12,9%.

Las drusas de la lámina basal (BLD) son un concepto de enfermedad descrito por primera vez por Gass en 1977 como numerosas drusas amarillas pequeñas dispersas en el fondo de ojo. El patrón de “estrellas en el cielo” en la angiografía fluoresceínica (AF) es característico. 1)
Inicialmente denominadas “drusas de la lámina basal” como engrosamiento nodular de la membrana basal del EPR, investigaciones posteriores revelaron que los depósitos ocurren entre la membrana basal del EPR y la capa colágena interna de la membrana de Bruch, es decir, la misma ubicación que las drusas blandas típicas. Por lo tanto, ahora se recomienda el término “drusas cuticulares”. 1)
Aunque pertenece al espectro de la degeneración macular asociada a la edad (DMAE), tiene las siguientes características distintas de la DMAE típica:
Aunque es parte del espectro de la degeneración macular asociada a la edad, tiene características únicas como inicio relativamente más joven, predominio femenino, hallazgos de imagen característicos de “estrellas en el cielo” y “diente de sierra”, y fuerte asociación con mutaciones del gen CFH. También se considera una lesión precursora de la degeneración macular asociada a la edad y puede progresar a complicaciones maculares durante el seguimiento a largo plazo. 1)
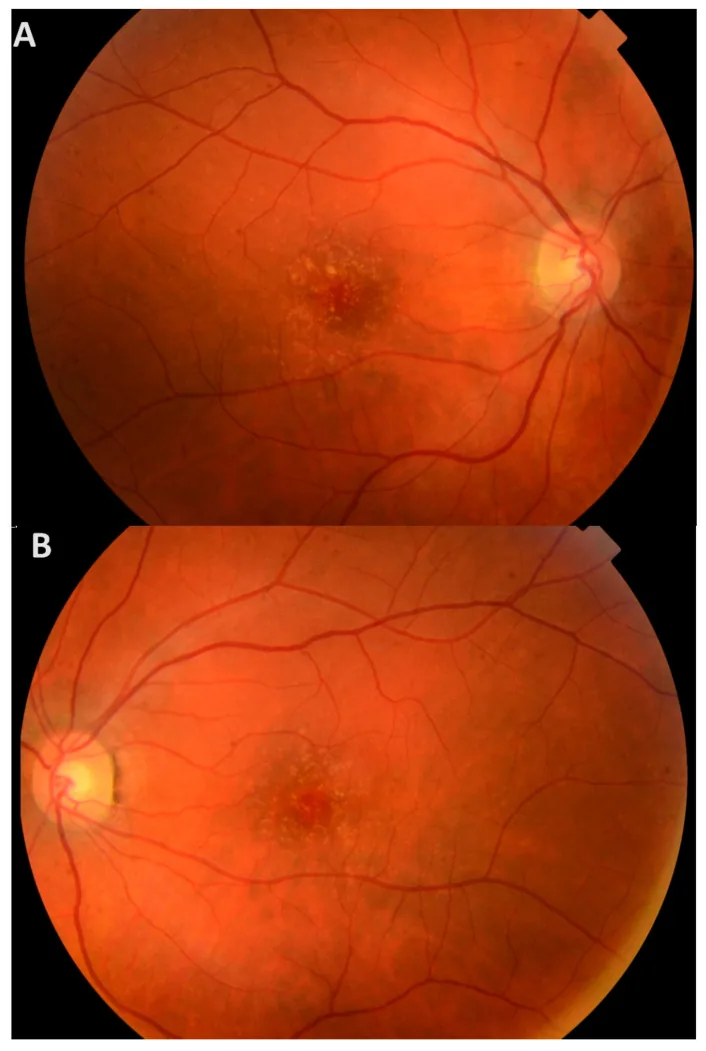
En las etapas tempranas, los síntomas subjetivos son escasos, y la mayoría de los pacientes permanecen asintomáticos hasta edades avanzadas. Incluso si hay drusen en la mácula, no hay síntomas a menos que las capas externas de la retina estén dañadas.
Si las drusen persisten durante mucho tiempo, la disfunción del EPR conduce a daño de las capas externas de la retina. Cuando la fóvea está afectada, aparecen los siguientes síntomas.
En el examen de fondo de ojo con dilatación pupilar, se observan numerosas drusen amarillas pequeñas en toda la retina. Se reconocen como múltiples drusen duras, elevadas, de color amarillo blanquecino debajo del EPR.
El fenotipo clínico se clasifica en tres tipos. 1)
Fenotipo 1
Distribución: Tipo concentrado en el área macular.
Riesgo de complicaciones: El más bajo de los tres tipos, con una incidencia estimada a 5 años de GA del 12,9%.
Fenotipo 2
Distribución: Tipo disperso en el polo posterior, que se extiende hacia la periferia y el lado nasal.
Riesgo de complicaciones: Incidencia estimada a 5 años de GA del 38,7%. El riesgo de MNV también es alto.
Fenotipo 3
Distribución: Tipo con drusas grandes mixtas (>200 μm).
Riesgo de complicaciones: El más alto, con una incidencia estimada a 5 años de GA del 43,6%.
Los principales hallazgos clínicos se muestran a continuación.
En la OCT se clasifica en tres tipos.1)
La etiología de los drusen de la lámina basal no se comprende completamente. Los factores de riesgo actualmente conocidos se enumeran a continuación.
Factores genéticos
Diferencias de sexo y antecedentes familiares
Asociación con enfermedades sistémicas
Esto se debe a que las anomalías en la vía alternativa del complemento causadas por mutaciones en el gen CFH forman depósitos similares tanto en el ojo (entre el EPR y la membrana de Bruch) como en el riñón (membrana basal glomerular). Especialmente en pacientes jóvenes (5-30 años), se recomienda el cribado de MPGN y síndrome hemolítico urémico atípico (aHUS). 1)
El diagnóstico combina múltiples modalidades de imagen. Se recomienda la confirmación con al menos tres de las siguientes: fotografía de fondo de ojo (CFP), SD-OCT, AFG y autofluorescencia de fondo (FAF). 1)
A continuación se muestran los hallazgos típicos de cada exploración.
| Método de exploración | Hallazgos típicos | Notas |
|---|---|---|
| Fotografía de fondo de ojo (CFP) | Numerosas drusas pequeñas amarillas | Dispersas desde el polo posterior hasta la periferia |
| FA | Patrón “cielo estrellado” | Múltiples puntos hiperfluorescentes en la fase arteriovenosa 1) |
| FAF | Hipoautofluorescencia central con borde hiperautofluorescente | Tasa de identificación precisa: 62% en casos presentes, 100% en casos ausentes 1) |
| SD-OCT | Elevación triangular de RPE-BL, “diente de sierra” | Clasificado en 3 tipos 1) |
Angiografía con ICG (ICGA): Muestra hiperfluorescencia temprana, pero en aproximadamente el 50% de los casos no se detectan drusas. 1)
Puntos clave para el diagnóstico diferencial
No existe un tratamiento establecido para eliminar las drusas en sí mismas. Las drusas basales laminares aisladas no requieren tratamiento; el seguimiento regular es la base.
Se han reportado las siguientes frecuencias de complicaciones. 1)
Las estrategias de tratamiento según la complicación se muestran a continuación.
Cuando hay CNV
Inyección intravítrea de anti-VEGF: Primera línea. Usar ranibizumab, aflibercept, brolucizumab, etc.
Terapia fotodinámica (PDT): Considerada cuando el anti-VEGF es ineficaz o está contraindicado.
Cuando hay GA
Sin tratamiento efectivo: No hay método establecido para detener la progresión.
Observación continua: Exámenes regulares para detectar CNV tempranamente.
Lesiones viteliformes
Observación: Puede remitir espontáneamente.
Casos con CNV: Considerar terapia anti-VEGF.
Sobre los suplementos
No se ha establecido la eficacia de los suplementos AREDS (Estudio de Enfermedades Oculares Relacionadas con la Edad) en pacientes con drusas de la lámina basal. Ejemplos comunes de formulaciones AREDS incluyen Ocuvite PreserVision 2 (3 comprimidos, 3 veces al día) y Sante Lutax 20+ Vitamina y Mineral (3 comprimidos, 3 veces al día).
Automonitoreo
El monitoreo diario con una rejilla de Amsler puede detectar cambios tempranos en metamorfopsia y escotoma central.
Actualmente no existe un tratamiento para eliminar las drusas en sí. Si hay CNV, se puede considerar la inyección intravítrea de anti-VEGF o la terapia fotodinámica (PDT). No hay un tratamiento establecido para la GA, y es importante la observación continua. Consulte la sección “Tratamiento estándar” para más detalles.
Las drusas de la lámina basal son material polimorfo que se acumula entre la membrana basal del EPR y la capa colágena interna de la membrana de Bruch. Sus componentes incluyen restos membranosos, colesterol no esterificado y complemento.
Mecanismo de formación
El EPR es responsable de la excreción de lipoproteínas, pero su recambio metabólico se deteriora con la edad. La matriz extracelular degenerada se acumula, formando la base de las drusas. La sobreactivación de la cascada del complemento debida a mutaciones del gen CFH (especialmente Tyr402His) acelera este proceso. 1)
Ciclo de vida de las drusas
Las drusas cuticulares son entidades dinámicas y repiten ciclos de crecimiento, fusión y regresión. 1)
Curso de las lesiones viteliformes
Las lesiones viteliformes progresan en el siguiente orden. 1)
Los portadores de variantes raras del gen CFH (p. ej., p.Arg1210Cys) tienden a desarrollar la enfermedad a una edad más temprana. Se cree que la sobreactivación crónica de la vía alternativa del complemento debida a mutaciones del CFH causa la formación de drusas antes que en la DMAE típica. 1)
Terapias dirigidas a la vía del complemento
Dado que las anomalías en la vía alternativa del complemento debidas a mutaciones en el gen CFH constituyen la base patológica, se están investigando activamente compuestos dirigidos a la vía del complemento. Debido al alto riesgo de efectos secundarios de la administración sistémica, la administración local (intraocular) está atrayendo la atención como un enfoque prometedor.
Predicción pronóstica mediante imágenes multimodales
Los avances en imágenes multimodales están permitiendo la identificación temprana de pacientes con alto riesgo de complicaciones. 1) La clasificación fenotípica (1-3) es útil para la predicción del pronóstico, y los fenotipos 2 y 3, como grupos de alto riesgo de GA y MNV, requieren un seguimiento particularmente estricto. 1)
Potencial de la medicina personalizada
Los avances en el análisis genético permiten esperar una medicina personalizada basada en variantes de genes relacionados con la DMAE, incluido el gen CFH. En particular, los portadores de variantes raras (p. ej., p.Arg1210Cys) pueden convertirse en objetivos de detección e intervención tempranas.