Fenótipo 1
Distribuição: Tipo concentrado na região macular.
Risco de complicações: Incidência estimada de GA em 5 anos de 12,9%, a mais baixa entre os 3 tipos.

Drusas da lâmina basal (BLD) são um conceito de doença descrito pela primeira vez por Gass em 1977 como múltiplas pequenas drusas amarelas espalhadas no fundo de olho. O padrão “estrelas no céu” na angiografia fluoresceínica (AF) é característico. 1)
Inicialmente denominadas “drusas da lâmina basal” como espessamento nodular da membrana basal do EPR, estudos posteriores mostraram que o depósito ocorre entre a membrana basal do EPR e a camada colágena dentro da membrana de Bruch, ou seja, a mesma localização das drusas moles comuns. Por isso, o nome “drusas cuticulares” é agora recomendado. 1)
Pertencem ao espectro da degeneração macular relacionada à idade (DMAE), mas apresentam as seguintes características diferentes da DMAE típica:
Embora faça parte do espectro da degeneração macular relacionada à idade, apresenta características únicas, como início relativamente mais jovem, predominância feminina, achados de imagem característicos de “estrelas no céu” e “dente de serra”, e forte associação com mutações no gene CFH. Também é considerada uma lesão precursora da degeneração macular relacionada à idade e pode progredir para complicações maculares com acompanhamento de longo prazo. 1)
Nos estágios iniciais, os sintomas subjetivos são raros, e a maioria dos pacientes permanece assintomática até a idade avançada. Mesmo com drusens na mácula, não há sintomas se não houver dano às camadas externas da retina.
Se os drusens persistirem por um longo período, a disfunção do epitélio pigmentar da retina (EPR) pode progredir para dano às camadas externas da retina. Quando a fóvea é envolvida, os seguintes sintomas aparecem.
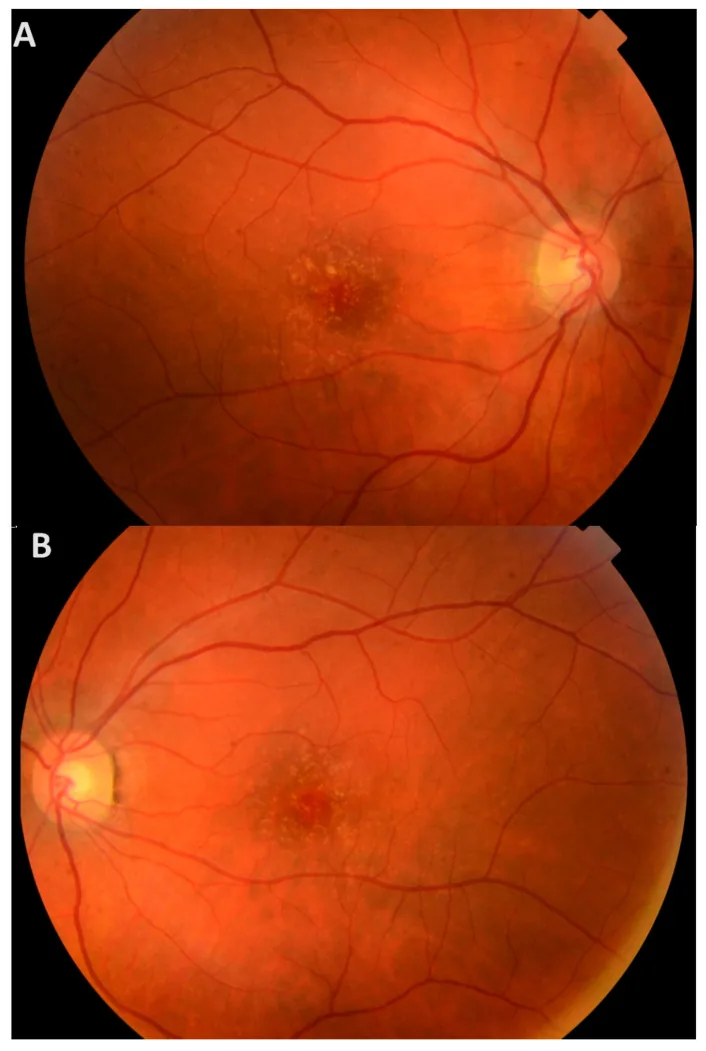
No exame de fundo de olho com dilatação pupilar, observam-se numerosos drusens amarelos pequenos espalhados por toda a retina. Eles são reconhecidos como drusens duros, elevados, amarelo-esbranquiçados sob o EPR.
O fenótipo clínico é classificado em três tipos. 1)
Fenótipo 1
Distribuição: Tipo concentrado na região macular.
Risco de complicações: Incidência estimada de GA em 5 anos de 12,9%, a mais baixa entre os 3 tipos.
Fenótipo 2
Distribuição: Tipo disseminado no polo posterior, estendendo-se para a periferia e lado nasal.
Risco de complicações: Incidência estimada de GA em 5 anos de 38,7%. Risco de MNV também elevado.
Fenótipo 3
Distribuição: Tipo com drusas grandes (>200 μm) misturadas.
Risco de complicações: Incidência estimada de GA em 5 anos de 43,6%, a mais alta.
Os principais achados clínicos são mostrados abaixo.
Na OCT, são classificados em três tipos.1)
A etiologia da drusen basal não é completamente compreendida. Os fatores de risco atualmente conhecidos estão listados abaixo.
Fatores Genéticos
Diferenças de Sexo e Histórico Familiar
Associação com Doenças Sistêmicas
Isso ocorre porque a anormalidade da via alternativa do complemento devido à mutação no gene CFH leva à formação de depósitos semelhantes tanto no olho (entre o EPR e a membrana de Bruch) quanto no rim (membrana basal glomerular). Especialmente em pacientes jovens (5–30 anos), recomenda-se triagem para MPGN e síndrome hemolítico-urêmica atípica (aHUS). 1)
O diagnóstico requer a combinação de múltiplas modalidades de imagem. Recomenda-se confirmação com pelo menos três dos seguintes: fotografia de fundo de olho (CFP), SD-OCT, angiografia fluoresceínica (FA) e autofluorescência de fundo (FAF). 1)
Os achados típicos de cada exame são mostrados abaixo.
| Método de Exame | Achados Típicos | Observações Especiais |
|---|---|---|
| Fotografia de Fundo (CFP) | Múltiplos drusen amarelos pequenos | Espalhados do polo posterior à periferia |
| FA | Padrão “céu estrelado” | Múltiplos pontos hiperfluorescentes na fase arteriovenosa 1) |
| FAF | Autofluorescência central baixa com borda hiperfluorescente | Taxa de identificação precisa de 62% nos casos presentes e 100% nos ausentes 1) |
| SD-OCT | Elevação triangular do RPE-BL e padrão “dente de serra” | Classificado em 3 tipos 1) |
Angiografia com ICG (ICGA): Apresenta hiperfluorescência precoce, mas cerca de 50% das drusas não são detectadas. 1)
Pontos de Diagnóstico Diferencial
Não há tratamento estabelecido para eliminar as drusas em si. Para drusas basais isoladas, não há indicação de tratamento, sendo o acompanhamento periódico regular a base.
As seguintes incidências de complicações foram relatadas: 1)
A seguir, o plano de tratamento de acordo com a complicação:
Quando associado a CNV
Injeção intravítrea de anti-VEGF: Primeira escolha. Utiliza-se ranibizumabe, aflibercepte, brolucizumabe, etc.
Terapia fotodinâmica (PDT): Considerada quando o anti-VEGF é ineficaz ou contraindicado.
Quando associado a AG
Nenhum tratamento eficaz: Não há método estabelecido para interromper a progressão.
Observação continuada: Continuar exames regulares para detecção precoce do aparecimento de CNV.
Lesões viteliformes
Observação: Pode haver regressão espontânea.
Casos com CNV: Considerar indicação de anti-VEGF.
Sobre Suplementos
A eficácia dos suplementos AREDS (Age-Related Eye Disease Study) em pacientes com drusas basais não está estabelecida. Exemplos de prescrições comuns de AREDS incluem Ocuvite PreserVision 2 (3 comprimidos, 3 vezes ao dia) e Sante Lutax 20+ Vitamina & Mineral (3 comprimidos, 3 vezes ao dia).
Automonitoramento
O monitoramento diário com a grade de Amsler pode detectar precocemente alterações na metamorfopsia e escotoma central.
Atualmente não existe tratamento que elimine as drusas em si. Quando ocorre CNV, a injeção intravítrea de anti-VEGF ou a terapia fotodinâmica (PDT) são indicadas. Para GA, não há tratamento estabelecido, e a observação contínua é importante. Consulte a seção “Tratamento Padrão” para detalhes.
As drusas basais são substâncias polimórficas que se acumulam entre a membrana basal do EPR e a camada colágena interna da membrana de Bruch. Seus componentes incluem debris membranares, colesterol não esterificado, complemento e outros.
Mecanismo de Formação
O EPR é responsável pela excreção de lipoproteínas, mas com o envelhecimento, seu metabolismo piora. A matriz extracelular degenerada se acumula, formando a base das drusas. A ativação excessiva da cascata do complemento devido à mutação no gene CFH (especialmente Tyr402His) acelera esse processo. 1)
Ciclo de Vida das Drusas
As drusas cuticulares são entidades dinâmicas, repetindo um ciclo de crescimento, fusão e regressão. 1)
Evolução da Lesão Viteliforme
A lesão viteliforme progride na seguinte ordem. 1)
Portadores de variantes raras do gene CFH (como p.Arg1210Cys) tendem a ter início mais jovem. Acredita-se que a ativação excessiva crônica da via alternativa do complemento devido à mutação no gene CFH cause formação de drusas mais precocemente do que na DMRI comum. 1)
Terapia direcionada à via do complemento
Como a anormalidade da via alternativa do complemento devido a mutações no gene CFH é a base fisiopatológica, compostos que visam a via do complemento estão sendo ativamente pesquisados. Como a administração sistêmica apresenta alto risco de efeitos colaterais, a administração local (intraocular) é considerada uma abordagem promissora.
Predição de prognóstico por imagem multimodal
Com o avanço da imagem multimodal, tornou-se possível identificar precocemente pacientes com alto risco de complicações. 1) A classificação de fenótipos (1-3) é útil para predição de prognóstico, sendo os fenótipos 2 e 3 grupos de alto risco para GA e MNV, exigindo acompanhamento rigoroso. 1)
Potencial para medicina personalizada
Com o avanço da análise genética, espera-se que a medicina personalizada baseada em variantes de genes relacionados à AMD, especialmente o gene CFH, se torne realidade. Portadores de variantes raras (como p.Arg1210Cys) podem ser alvos para triagem e intervenção precoces.