Phänotyp 1
Verteilung : Typ, der auf die Makularegion konzentriert ist.
Komplikationsrisiko : Geschätzte 5-Jahres-Inzidenz von GA 12,9 %, die niedrigste der 3 Typen.

Basallaminäre Drusen (basal laminar drusen; BLD) sind ein Krankheitskonzept, das erstmals 1977 von Gass beschrieben wurde, der zahlreiche kleine gelbe Drusen im Augenhintergrund beobachtete. Das „Sternenhimmel“-Muster in der Fluoreszenzangiographie (FA) ist charakteristisch. 1)
Ursprünglich als „basal laminar drusen“ aufgrund einer knotigen Verdickung der RPE-Basalmembran benannt, zeigten spätere Studien, dass die Ablagerungen zwischen der Basalmembran des RPE und der Kollagenschicht der Bruch-Membran liegen, also an derselben Stelle wie gewöhnliche weiche Drusen. Daher wird heute der Begriff „kutikuläre Drusen“ (cuticular drusen) empfohlen. 1)
Sie gehören zum Spektrum der altersbedingten Makuladegeneration (AMD), weisen jedoch folgende Merkmale auf, die sie von der typischen AMD unterscheiden:
Obwohl sie Teil des Spektrums der altersbedingten Makuladegeneration ist, hat sie eigene Merkmale wie ein relativ junges Erkrankungsalter, eine weibliche Dominanz, charakteristische Bildgebungsbefunde wie “Sternenhimmel” oder “Sägezahn”, und eine starke Assoziation mit CFH-Genmutationen. Sie wird auch als Vorläuferläsion der AMD angesehen und kann bei Langzeitbeobachtung zu Makulakomplikationen fortschreiten. 1)
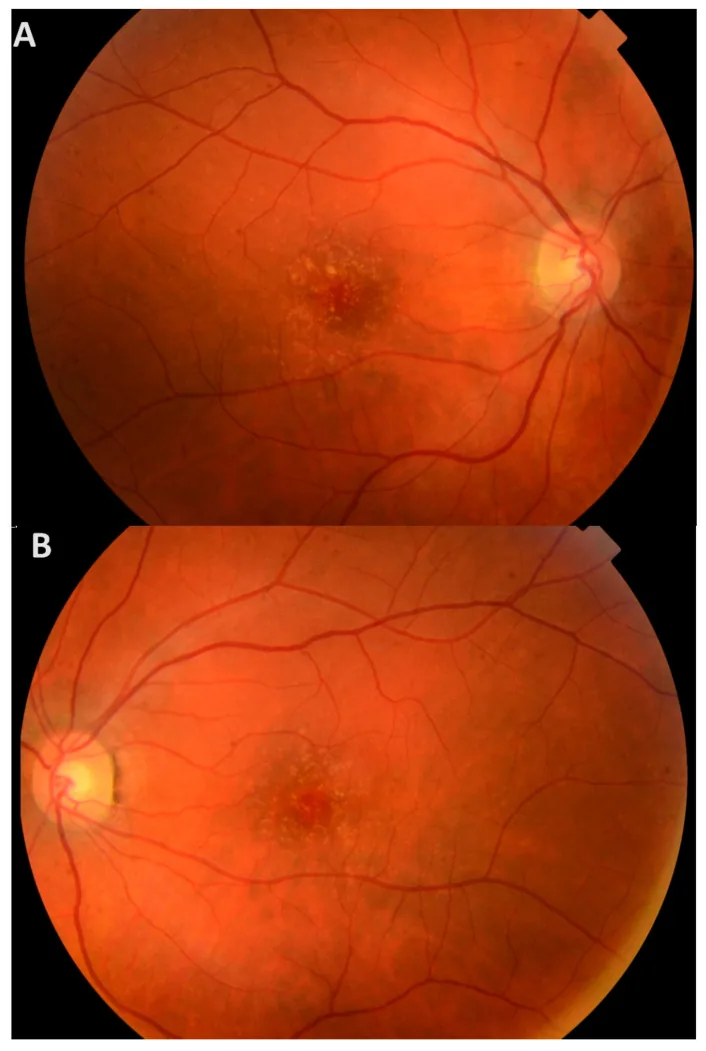
Zu Beginn sind subjektive Symptome selten, und die meisten Patienten bleiben bis ins hohe Alter asymptomatisch. Selbst wenn Drusen in der Makula vorhanden sind, bleiben sie asymptomatisch, solange keine Schädigung der äußeren Netzhautschichten auftritt.
Wenn Drusen über einen langen Zeitraum bestehen, kann eine RPE-Dysfunktion zu einer Schädigung der äußeren Netzhautschichten führen. Wenn die Fovea betroffen ist, treten die folgenden Symptome auf.
Bei der Fundusuntersuchung unter Pupillenerweiterung werden zahlreiche kleine gelbe Drusen über die gesamte Netzhaut beobachtet. Sie werden als multiple harte, erhabene gelb-weiße Drusen unter dem RPE erkannt.
Der klinische Phänotyp wird in drei Typen eingeteilt. 1)
Phänotyp 1
Verteilung : Typ, der auf die Makularegion konzentriert ist.
Komplikationsrisiko : Geschätzte 5-Jahres-Inzidenz von GA 12,9 %, die niedrigste der 3 Typen.
Phänotyp 2
Verteilung : Typ, der im hinteren Pol verstreut ist und sich zur Peripherie und nasalen Seite ausdehnt.
Komplikationsrisiko : Geschätzte 5-Jahres-Inzidenz von GA 38,7 %. Auch MNV-Risiko hoch.
Phänotyp 3
Verteilung : Typ mit gemischten großen Drusen (>200 μm).
Komplikationsrisiko : Geschätzte 5-Jahres-Inzidenz von GA 43,6 %, die höchste.
Die wichtigsten klinischen Befunde sind unten aufgeführt.
Im OCT werden drei Typen klassifiziert.1)
Die Ätiologie der Basal-layer-Drusen ist nicht vollständig geklärt. Die derzeit bekannten Risikofaktoren sind unten aufgeführt.
Genetische Faktoren
Geschlecht und Familienanamnese
Assoziation mit systemischen Erkrankungen
Eine durch CFH-Genmutation verursachte Anomalie des alternativen Komplementwegs führt zur Bildung ähnlicher Ablagerungen sowohl im Auge (zwischen RPE und Bruch-Membran) als auch in der Niere (glomeruläre Basalmembran). Insbesondere bei jungen Patienten (5–30 Jahre) wird ein Screening auf MPGN und atypisches hämolytisch-urämisches Syndrom (aHUS) empfohlen. 1)
Die Diagnose kombiniert mehrere Bildgebungsmodalitäten. Eine Bestätigung durch mindestens drei der folgenden Verfahren wird empfohlen: Fundusfotografie (CFP), SD-OCT, Fluoreszenzangiographie (FA) und Fundusautofluoreszenz (FAF). 1)
Die typischen Befunde der einzelnen Untersuchungen sind unten aufgeführt.
| Untersuchungsmethode | Typischer Befund | Bemerkungen |
|---|---|---|
| Fundusfotografie (CFP) | Zahlreiche kleine gelbe Drusen | Vom hinteren Pol bis zur Peripherie verstreut |
| FA | ”Sternenhimmel”-Muster | Zahlreiche hyperfluoreszente Punkte in der arteriovenösen Phase1) |
| FAF | Zentrale Hypoautofluoreszenz mit hyperautofluoreszentem Rand | 62 % korrekte Identifikationsrate bei Vorhandensein, 100 % bei Fehlen1) |
| SD-OCT | Dreieckige Erhebung der RPE-BL, “saw-tooth” | Einteilung in 3 Typen1) |
ICG-Angiographie (ICGA) : zeigt frühe Hyperfluoreszenz, aber in etwa 50 % der Fälle sind Drusen nicht nachweisbar.1)
Schlüsselpunkte der Differentialdiagnose
Es gibt keine etablierte Therapie, um Drusen selbst verschwinden zu lassen. Bei isolierten Basallayer-Drüsen besteht keine Behandlungsindikation; regelmäßige Verlaufskontrollen sind die Grundlage.
Folgende Häufigkeiten von Komplikationen wurden berichtet. 1)
Die komplikationsspezifischen Behandlungsstrategien sind unten aufgeführt.
Bei CNV
Intravitreale Anti-VEGF-Injektion : Erstlinientherapie. Verwendung von Ranibizumab, Aflibercept, Brolucizumab usw.
Photodynamische Therapie (PDT) : Wird in Betracht gezogen, wenn Anti-VEGF unwirksam oder kontraindiziert ist.
Bei GA
Keine wirksame Behandlung : Es gibt keine etablierte Methode, um das Fortschreiten zu stoppen.
Fortlaufende Überwachung : Regelmäßige Untersuchungen werden fortgesetzt, um das Auftreten einer CNV frühzeitig zu erkennen.
Vitelliforme Läsionen
Beobachtung : kann spontan zurückgehen.
Fälle mit CNV : Prüfung auf Anti-VEGF-Therapie.
Zu Nahrungsergänzungsmitteln
Die Wirksamkeit von AREDS (Age-Related Eye Disease Study)-Nahrungsergänzungsmitteln bei Patienten mit Basallayer-Drusen ist nicht belegt. Beispiele für gängige AREDS-Rezepturen: Ocuvite PreserVision 2 (3 Tabletten, verteilt auf 3 Einnahmen) oder Sante Retax 20+ Vitamin & Mineral (3 Tabletten, verteilt auf 3 Einnahmen).
Selbstüberwachung
Die tägliche Überwachung mit der Amsler-Tafel ermöglicht die frühzeitige Erkennung von Veränderungen der Metamorphopsie und des Zentralskotoms.
Es gibt derzeit keine Behandlung, die die Drusen selbst verschwinden lässt. Bei begleitender CNV sind intravitreale Anti-VEGF-Injektionen oder photodynamische Therapie (PDT) indiziert. Für die GA gibt es keine etablierte Behandlung, und eine kontinuierliche Nachbeobachtung ist wichtig. Einzelheiten finden Sie im Abschnitt „Standardtherapie“.
Basallayer-Drusen sind polymorphe Ablagerungen, die sich zwischen der RPE-Basalmembran und der inneren Kollagenschicht der Bruch-Membran ansammeln. Ihre Bestandteile umfassen Membranreste, nicht verestertes Cholesterin und Komplement.
Bildungsmechanismus
Das RPE ist für die Ausscheidung von Lipoproteinen zuständig, aber mit zunehmendem Alter verschlechtert sich sein Stoffwechselumsatz. Degenerierte extrazelluläre Matrix sammelt sich an und bildet die Grundlage für Drusen. Die Überaktivierung der Komplementkaskade durch CFH-Genmutationen (insbesondere Tyr402His) beschleunigt diesen Prozess. 1)
Lebenszyklus der Drusen
Kutikuläre Drusen sind dynamische Gebilde, die einen Zyklus aus Wachstum, Fusion und Rückbildung durchlaufen. 1)
Verlauf der vitelliformen Läsion
Die vitelliforme Läsion schreitet in der folgenden Reihenfolge fort. 1)
Träger seltener CFH-Genvarianten (wie p.Arg1210Cys) neigen dazu, die Krankheit in jüngerem Alter zu entwickeln. Es wird angenommen, dass die chronische Überaktivierung des alternativen Komplementwegs durch CFH-Mutationen früher zur Drusenbildung führt als bei typischer AMD. 1)
Therapie, die auf den Komplementweg abzielt
Da die Anomalie des alternativen Komplementwegs aufgrund einer CFH-Genmutation die pathologische Grundlage bildet, werden Verbindungen, die auf den Komplementweg abzielen, intensiv erforscht. Da die systemische Verabreichung ein hohes Risiko von Nebenwirkungen birgt, wird die lokale (intraokulare) Verabreichung als vielversprechender Ansatz angesehen.
Prognosevorhersage durch multimodale Bildgebung
Fortschritte in der multimodalen Bildgebung ermöglichen zunehmend die frühzeitige Identifizierung von Patienten mit hohem Komplikationsrisiko. 1) Die Phänotyp-Klassifikation (1–3) ist für die Prognosevorhersage nützlich; Phänotyp 2 und 3 sind Hochrisikogruppen für GA und MNV und erfordern eine besonders strenge Nachbeobachtung. 1)
Möglichkeiten der personalisierten Medizin
Fortschritte in der genetischen Analyse lassen die Verwirklichung einer personalisierten Medizin auf der Grundlage von Varianten AMD-assoziierter Gene, einschließlich des CFH-Gens, erwarten. Insbesondere Träger seltener Varianten (wie p.Arg1210Cys) könnten Ziel eines frühen Screenings und Eingreifens sein.