基底层玻璃膜疣(角质样玻璃膜疣 )是年龄相关性黄斑变性 谱系的一种类型,表现为视网膜色素上皮 (RPE )基底膜与Bruch膜之间积聚大量小型黄色玻璃膜疣 。
发病年龄较典型AMD 年轻(平均57.9岁),患者中60%至92.1%为女性。1)
荧光素眼底血管造影 (FA )上的“星空”模式、OCT 上的“锯齿”模式是特征性表现。1) 与CF H基因突变(p.Tyr402His)密切相关,补体 替代途径异常是病理基础。1)
玻璃膜疣 本身无治疗方法,关键在于早期发现并发症(脉络膜新生血管 、地图状萎缩 )并进行适当治疗。年轻患者可能合并膜增生性肾小球肾炎(MPGN)等肾脏疾病,有时需要全身评估。1)
基底层玻璃膜疣(BLD)是1977年Gass首次描述的疾病概念,表现为眼底散在大量小型黄色玻璃膜疣 。荧光素眼底血管造影 (FA )上的“星空”模式是其特点。1)
最初因RPE 基底膜的结节状增厚而命名为“基底层玻璃膜疣”,但后续研究表明沉积物位于RPE 基底膜与Bruch膜内胶原层之间,即与典型软性玻璃膜疣 位置相同。因此,目前推荐使用“角质样玻璃膜疣 ”这一名称。1)
虽然属于年龄相关性黄斑变性 (AMD )谱系,但具有以下不同于典型AMD 的特征:
发病年龄 :相对年轻,平均57.9 ± 13.4岁性别差异 :60%至92.1%的患者为女性。女性患病概率约为典型AMD 的5倍。1) 玻璃膜疣 大小玻璃膜疣 。1) 分布 :可从后极部延伸至周边部及视盘周围。
Q
基底层玻璃膜疣和年龄相关性黄斑变性是同一种疾病吗?
A
虽然它是年龄相关性黄斑变性 谱系的一部分,但具有相对年轻发病、女性优势、特征性的“星空”和“锯齿”影像学表现以及与CF H基因突变的强关联等独特特征。它也被视为年龄相关性黄斑变性 的前驱病变,长期随访中可能进展为黄斑 并发症。1)
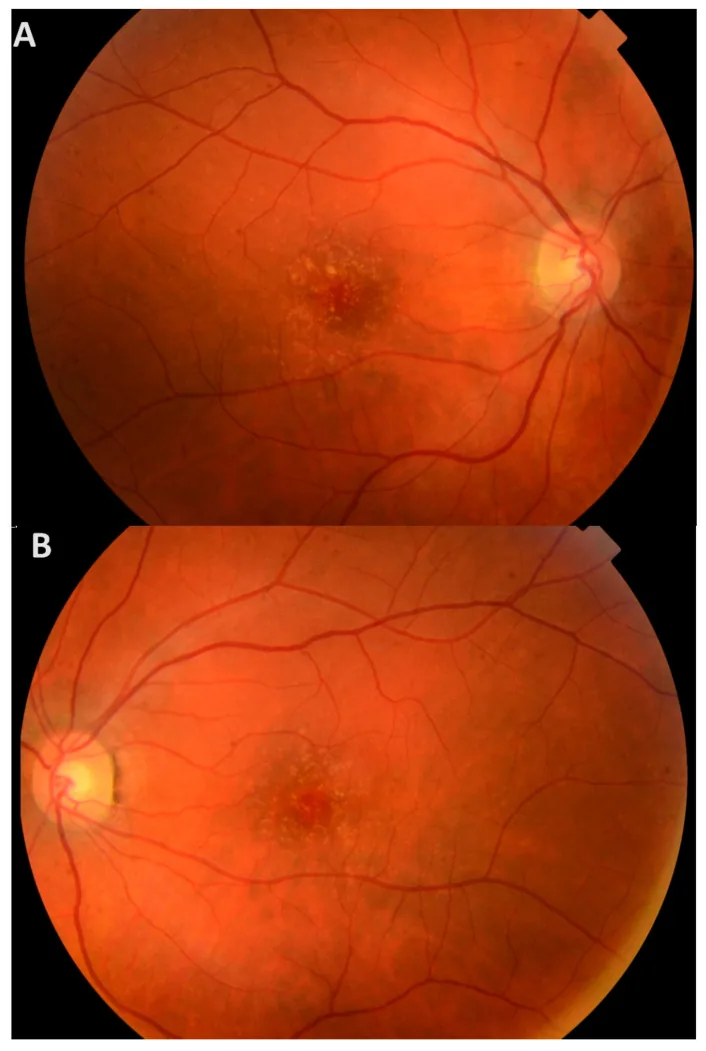
基底层玻璃膜疣图像 Egle Preiksaitiene; Viktorija Gurskytė; Violeta Mikštienė; Rasa Strupaitė-Šileikienė; Ramūnas Dzindzalieta; Gunda Petraitytė. Evidence for the Pathogenicity of a
CF H Variant in a Multigenerational Family with Cuticular Drusen. Medicina (Kaunas). 2025 Sep 11; 61(9):1649 Figure 2. PM
CI D: PMC12472062. License: CC BY.
先证者右眼(A)和左眼(B)的眼底照片显示后极部大量小而硬的黄色玻璃膜疣 。
早期自觉症状很少,大多数患者直到晚年仍无症状。即使黄斑部 存在玻璃膜疣 ,只要视网膜 外层未受损,就无症状。
如果玻璃膜疣 长期存在,RPE 功能障碍会进展为视网膜 外层损伤。当累及中心凹 时,会出现以下症状。
散瞳 眼底检查 可见整个视网膜 有大量小的黄色玻璃膜疣 。它们被识别为RPE 下的多个硬性、隆起的黄白色玻璃膜疣 。
临床表型分为三种类型。1)
表型1
分布 :集中于黄斑 区的类型。
并发症风险 :GA的5年估计发生率为12.9%,在3型中最低。
表型2
分布 :散在于后极部,向周边和鼻侧扩展的类型。
并发症风险 :GA的5年估计发生率为38.7%。MNV风险也高。
表型3
分布 :混合有大玻璃膜疣 (>200 μm)的类型。
并发症风险 :最高,GA的5年估计发生率为43.6%。
主要临床所见如下所示。
合并大玻璃膜疣 (>200 μm) :25~59.3%可见,60岁以上常伴有色素异常1) 向视乳头周围扩展 :63.3~75.3%可见1) 色素性RPE 改变 :最常见的合并所见(47.5%)OCT 所见RPE -BL的三角形隆起,特征性的“锯齿状”图案1)
OCT 上分为三种类型。1)
1型(33%) :浅的RPE -BL隆起2型(49%) :锯齿状模式(最典型)3型(18%) :丘状模式
基底层玻璃膜疣的病因尚未完全阐明。目前已知的风险因素如下。
遗传因素
CF H基因p.Tyr402His变异玻璃膜疣 年龄相关性黄斑变性 患者中为70%,高于普通年龄相关性黄斑变性 (55%)1) CF H基因罕见变异玻璃膜疣 具有特异性1) FBLN5基因突变 :已有相关报道1) 年龄相关性黄斑变性 常见高风险SNPsCF H、ARMS 2、CF B、C2、C3、APOE相关1)
性别差异和家族史
60–92.1%的患者为女性,女性是独立风险因素1)
44–53%的BLD患者有年龄相关性黄斑变性 家族史
与全身疾病的关联
MPGN(膜增生性肾小球肾炎)II型 :补体 替代途径异常导致眼和肾脏出现类似沉积物。所有长期MPGN患者(>16个月)均出现玻璃膜疣 样沉积物1) C3肾小球肾炎 :已有类似眼部表现的报道1) 80%的致密沉积物病患者可见角质层玻璃膜疣 。
即使视力 没有变化,也请从年轻时(50多岁)开始定期进行眼底检查 。
如果有AMD 或基底层玻璃膜疣的家族史,尤其需要早期进行眼科随访。
如果诊断为肾脏疾病(如MPGN),建议也接受眼科检查。
在家使用阿姆斯勒方格表进行自我监测有助于早期发现并发症。
Q
为什么与肾脏疾病相关?
A
这是因为CF H基因突变导致的补体 替代途径异常,会在眼睛(RPE -布鲁赫膜 之间)和肾脏(肾小球基底膜)形成类似的沉积物。特别是年轻患者(5-30岁),建议进行MPGN和非典型溶血性尿毒症综合征(aHUS)的筛查。1)
诊断需结合多种影像学检查。建议在眼底照相 (CF P)、SD-OCT 、FA 、眼底自发荧光 (FAF )中至少三项确认。1)
各项检查的典型表现如下所示。
检查方法 典型表现 备注 眼底照相 (CF P)大量小的黄色玻璃膜疣 从后极部到周边散在分布 FA ”星空”模式 动静脉期多个高荧光点 1) FAF 中心低自发荧光伴高自发荧光边缘 存在病例62%,不存在病例100%的准确识别率 1) SD-OCT RPE -BL三角形隆起、“锯齿状”分为3种类型 1)
ICG血管造影(ICGA ) :早期呈高荧光,但约50%病例无法检测到玻璃膜疣 。1)
鉴别诊断要点
硬性玻璃膜疣 和软性玻璃膜疣 :根据大小、形状和OCT 表现鉴别。硬性玻璃膜疣 均匀、边缘清晰,软性玻璃膜疣 较大、边缘模糊 1) 网状假玻璃膜疣 :OCT 和FAF 上的分布模式不同常染色体显性玻璃膜疣 :通过家族史和基因检测鉴别模式黄斑 营养不良和Best病 :电生理检查和基因检测有用与色素上皮脱离(PED )的鉴别 :OCT 显示隆起RPE 内部低反射→色素上皮脱离,高反射→玻璃膜疣 。
尚无消除玻璃膜疣 本身的治疗方法。孤立性基底层玻璃膜疣无需治疗,定期随访是基本原则。
以下并发症的发生率已有报道。1)
脉络膜新生血管 (MNV/CNV )地图状萎缩 (GA)卵黄状病变 :白人24.2%,亚洲人1.2%,合并MNV者30%。
按并发症分类的治疗方针如下。
合并CNV时
抗VEGF药物 玻璃体内注射 雷珠单抗 、阿柏西普 、布罗珠单抗等。
光动力疗法 (PDT )抗VEGF药物 无效或不适用时考虑。
合并GA时
无有效治疗方法 :尚无阻止进展的确定方法。
持续观察 :为早期发现CNV ,定期检查。
卵黄状病变
观察 :可能自行消退。
合并CNV 病例 :考虑抗VEGF药物 治疗。
关于补充剂
AREDS(年龄相关性眼病研究)补充剂对基底层玻璃膜疣患者的疗效尚未确定。常见的AREDS配方包括Ocuvite PreserVision 2(每日3次,每次3片)和Sante Lutax 20+维生素与矿物质(每日3次,每次3片)。
自我监测
使用阿姆斯勒方格表进行日常监测可以早期发现视物变形 和中心暗点 的变化。
由于玻璃膜疣 本身没有治疗方法,因此早期发现并发症(脉络膜新生血管 、GA)至关重要。
MNV在表型2和3中风险特别高,对于这些表型应考虑缩短观察间隔。1)
年轻患者(≤60岁)中GA的发生率为9.2%,因此不能因年龄而掉以轻心。1)
对于年轻发病病例(5-30岁),也建议进行MPGN和aHUS的筛查。
基底层玻璃膜疣是积聚在RPE 基底膜和Bruch膜内胶原层之间的多形性物质。其成分包括膜样碎片、非酯化胆固醇和补体 等。
形成机制
RPE 负责脂蛋白的排泄,但随着年龄增长,其代谢周转能力下降。变性的细胞外基质积累,形成玻璃膜疣 的基础。CF H基因突变(尤其是Tyr402His)导致的补体 级联过度激活加速了这一过程。1)
玻璃膜疣 的生命周期
Cuticular drusen是动态存在的,经历生长、融合和消退的循环。1)
生长/融合期 :单个玻璃膜疣 扩大并与相邻玻璃膜疣 融合消退期 :RPE 异常积累,玻璃膜疣 消退→RPE 萎缩→地图状萎缩 新生血管 脉络膜新生血管 侵入(CNV 形成)
卵黄样病变的病程
卵黄样病变按以下顺序进展。1)
卵黄样物质形成
脉络膜 血管高通透性增加RPE 萎缩脉络膜 变薄
Q
为什么年轻人也会发病?
A
携带CF H基因罕见变异(如p.Arg1210Cys)的人倾向于更年轻发病。CF H基因突变导致的补体 替代途径慢性过度激活被认为比典型AMD 更早引起玻璃膜疣 形成。1)
靶向补体 途径的治疗
由于CF H基因突变导致的补体 替代途径异常是病理基础,靶向补体 途径的化合物正在积极研究中。由于全身给药副作用风险高,局部(眼内)给药作为一种有前景的方法受到关注。
通过多模态成像进行预后预测
多模态成像的进步使得早期识别并发症高风险患者成为可能。1) 表型分类(1-3)对预后预测有用,表型2和3作为GA和MNV的高风险组,需要特别严格的随访。1)
个体化医疗的可能性
基因分析的进步有望实现基于AMD 相关基因(包括CF H基因)变异的个体化医疗。特别是罕见变异(如p.Arg1210Cys)携带者可能成为早期筛查和干预的目标。
Fragiotta S, Fernandez-Avellaneda P, Breazzano MP, Scuderi G. Clinical manifestations of cuticular drusen: current perspectives. Clin Ophthalmol. 2021;15:3877-3887.
van de Ven JP, Boon CJ, Smailhodzic D, Lechanteur YT, den Hollander AI, Hoyng CB, et al. Short-term changes of Basal laminar drusen on spectral-domain optical coherence tomography. Am J Ophthalmol. 2012;154(3):560-7. PMID: 22626619.
Russell SR, Mullins RF, Schneider BL, Hageman GS. Location, substructure, and composition of basal laminar drusen compared with drusen associated with aging and age-related macular degeneration. Am J Ophthalmol. 2000;129(2):205-14. PMID: 10682974.
复制全文后,可以粘贴到你常用的 AI 助手中提问。
打开下面的 AI 助手,并把复制的内容粘贴到聊天框。