فنوتیپ 1
توزیع: نوع متمرکز در ناحیه ماکولا.
خطر عوارض: بروز تخمینی ۵ ساله GA 12.9% که پایینترین میزان در بین سه نوع است.

دروزن لایه پایه (Basal laminar drusen; BLD) یک مفهوم بیماری است که اولین بار در سال ۱۹۷۷ توسط گاس به عنوان وجود تعداد زیادی دروزن کوچک زرد رنگ پراکنده در فوندوس توصیف شد. الگوی “ستارگان در آسمان” در آنژیوگرافی فلورسئین (FA) مشخصه آن است. 1)
در ابتدا به دلیل ضخیم شدن ندولار غشای پایه RPE “دروزن لایه پایه” نامیده شد، اما مطالعات بعدی نشان داد که رسوب بین غشای پایه RPE و لایه کلاژنی غشای بروخ، یعنی همان محل دروزن نرم معمولی، رخ میدهد. بنابراین، نام “دروزن کوتیکولار” (cuticular drusen) در حال حاضر توصیه میشود. 1)
این بیماری به طیف دژنراسیون ماکولای وابسته به سن (AMD) تعلق دارد اما ویژگیهای متفاوتی با AMD معمولی دارد:
اگرچه بخشی از طیف دژنراسیون ماکولا وابسته به سن است، اما ویژگیهای منحصر به فردی مانند شروع در سنین نسبتاً پایینتر و غلبه در زنان، یافتههای تصویربرداری مشخصه “ستارگان در آسمان” یا “دندان ارهای”، و ارتباط قوی با جهش ژن CFH دارد. همچنین به عنوان ضایعه پیشدرآمد دژنراسیون ماکولا وابسته به سن در نظر گرفته میشود و در پیگیری طولانیمدت ممکن است به عوارض ماکولا پیشرفت کند. 1)
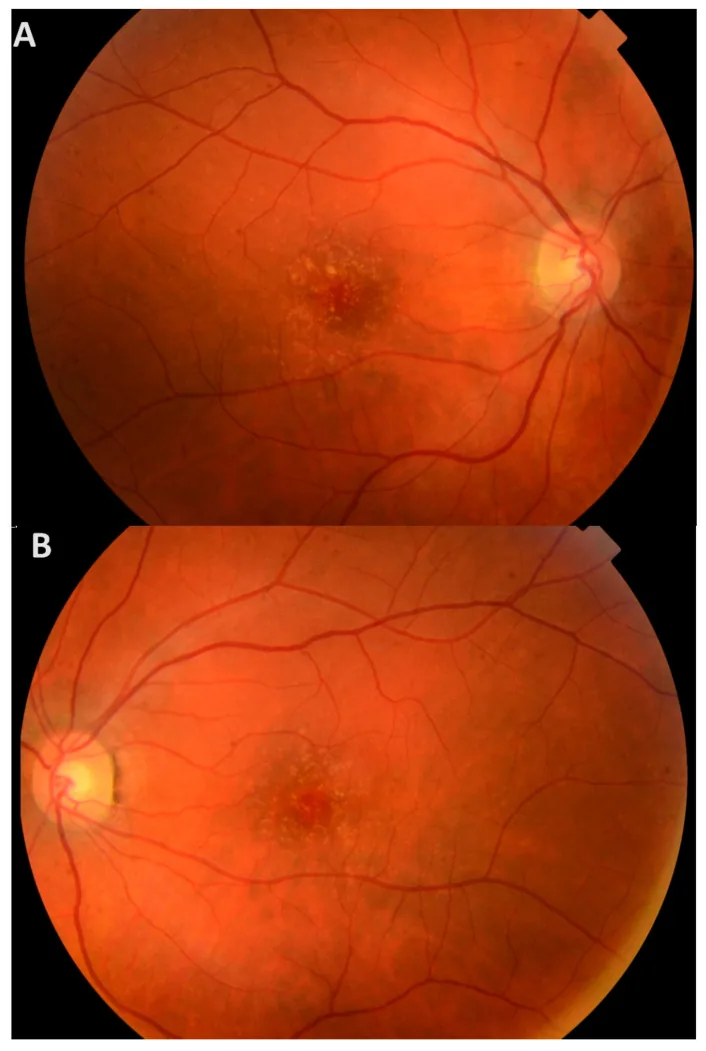
در مراحل اولیه، علائم ذهنی اندک است و اکثر بیماران تا سنین بالا بدون علامت باقی میمانند. حتی اگر دروزن در ناحیه ماکولا وجود داشته باشد، تا زمانی که آسیب به لایههای خارجی شبکیه رخ ندهد، بدون علامت است.
اگر دروزن برای مدت طولانی وجود داشته باشد، از اختلال عملکرد RPE به آسیب لایههای خارجی شبکیه پیشرفت میکند. هنگامی که ناحیه فووه را درگیر کند، علائم زیر ظاهر میشوند.
در معاینه فوندوس با مردمک گشاد شده، تعداد زیادی دروزن زرد کوچک در سراسر شبکیه مشاهده میشود. این دروزنها به صورت برجستگیهای سخت زرد-سفید متعدد در زیر RPE دیده میشوند.
فنوتیپ بالینی به سه دسته تقسیم میشود. 1)
فنوتیپ 1
توزیع: نوع متمرکز در ناحیه ماکولا.
خطر عوارض: بروز تخمینی ۵ ساله GA 12.9% که پایینترین میزان در بین سه نوع است.
فنوتیپ ۲
توزیع: نوع پراکنده در قطب خلفی و گسترش به سمت محیط و بینی.
خطر عوارض: بروز تخمینی ۵ ساله GA 38.7%. خطر MNV نیز بالا است.
فنوتیپ ۳
توزیع: نوع همراه با دروزنهای بزرگ (>200 میکرومتر).
خطر عوارض: بروز تخمینی ۵ ساله GA 43.6% که بالاترین میزان است.
یافتههای بالینی اصلی در زیر آورده شده است.
در OCT به سه نوع طبقهبندی میشود.1)
علت دقیق دروزن لایه پایه (BLD) به طور کامل شناخته نشده است. عوامل خطر شناخته شده در زیر آورده شده است.
عوامل ژنتیکی
تفاوت جنسیتی و سابقه خانوادگی
ارتباط با بیماریهای سیستمیک
به دلیل ناهنجاری مسیر جایگزین کمپلمان ناشی از جهش ژن CFH، رسوبات مشابهی هم در چشم (بین RPE و غشای بروخ) و هم در کلیه (غشای پایه گلومرولی) تشکیل میشود. به ویژه در بیماران جوان (۵ تا ۳۰ سال) غربالگری MPGN و سندرم همولیتیک اورمیک آتیپیک (aHUS) توصیه میشود. 1)
تشخیص با ترکیبی از چند روش تصویربرداری انجام میشود. تأیید با حداقل سه روش از عکس فوندوس (CFP)، SD-OCT، FA و خودفلورسانس فوندوس (FAF) توصیه میشود. 1)
یافتههای معمول هر آزمایش در زیر آورده شده است.
| روش آزمایش | یافته معمول | نکات ویژه |
|---|---|---|
| عکس فوندوس (CFP) | دروزنهای کوچک زردرنگ متعدد | پراکنده در قطب خلفی تا محیط |
| FA | الگوی “آسمان پرستاره” | نقاط پرنور متعدد در فاز شریانی-وریدی 1) |
| FAF | خودفلورسانس کم مرکزی + حاشیه پرنور | نرخ شناسایی دقیق 62% در موارد وجود و 100% در موارد عدم وجود 1) |
| SD-OCT | برآمدگی مثلثی RPE-BL و “دندان ارهای” | طبقهبندی به 3 نوع 1) |
آنژیوگرافی با ایندوسیانین سبز (ICGA): فلورسانس زودرس نشان میدهد، اما در حدود 50% موارد دروسن قابل تشخیص نیست. 1)
نکات تشخیص افتراقی
روش درمانی برای از بین بردن خود دروزنها اثبات نشده است. برای دروزنهای پایهای منفرد، اندیکاسیون درمانی وجود ندارد و پیگیری منظم دورهای اساس کار است.
فراوانی بروز عوارض به شرح زیر گزارش شده است. 1)
راهکار درمانی بر اساس عارضه به شرح زیر است.
هنگام همراهی با CNV
تزریق داخل زجاجیهای داروهای ضد VEGF: خط اول. از رانیبیزوماب، آفلیبرسپت، برولوسیزوماب و غیره استفاده میشود.
فتودینامیک تراپی (PDT): در صورت عدم پاسخ یا عدم اندیکاسیون داروهای ضد VEGF در نظر گرفته میشود.
هنگام همراهی با GA
روش درمانی مؤثری وجود ندارد: هیچ روش اثبات شدهای برای توقف پیشرفت وجود ندارد.
پیگیری مداوم: معاینات دورهای به منظور تشخیص زودهنگام بروز CNV ادامه مییابد.
ضایعه زردهای
پیگیری: ممکن است خودبهخود برطرف شود.
موارد همراه با CNV: بررسی اندیکاسیون داروهای ضد VEGF.
در مورد مکملها
اثربخشی مکمل AREDS (مطالعه بیماری چشمی مرتبط با سن) برای بیماران دارای دروزن لایه پایه ثابت نشده است. نمونههای رایج تجویز AREDS عبارتند از: Ocuvite PreserVision 2 (3 قرص، سه بار در روز) و Sante Lutax 20+ ویتامین و مواد معدنی (3 قرص، سه بار در روز).
خودپایشی
پایش روزانه با استفاده از نمودار آمسلر میتواند تغییرات در دگردیسی و اسکوتوم مرکزی را زود تشخیص دهد.
در حال حاضر درمانی برای از بین بردن خود دروزن وجود ندارد. در صورت بروز CNV، تزریق داخل زجاجیهای داروهای ضد VEGF یا فوتودینامیک تراپی (PDT) اندیکاسیون دارد. برای GA درمان قطعی وجود ندارد و پیگیری مداوم مهم است. برای جزئیات به بخش «درمان استاندارد» مراجعه کنید.
دروزن لایه پایه، مواد پلیمورفی هستند که بین غشای پایه RPE و لایه کلاژنی داخلی غشای بروخ تجمع مییابند. اجزای تشکیلدهنده شامل بقایای غشایی، کلسترول غیراستری شده و کمپلمان هستند.
مکانیسم تشکیل
RPE وظیفه دفع لیپوپروتئین را بر عهده دارد، اما با افزایش سن، متابولیسم آن بدتر میشود. ماتریکس خارج سلولی تخریب شده تجمع یافته و بستر دروزن را تشکیل میدهد. فعال شدن بیش از حد آبشار کمپلمان به دلیل جهش ژن CFH (به ویژه Tyr402His) این فرآیند را تسریع میکند. 1)
چرخه زندگی دروزن
دروزن کوتیکولار موجودیتهای پویایی هستند که چرخه رشد، همجوشی و پسرفت را تکرار میکنند. 1)
سیر ضایعه ویتلی فرم
ضایعه ویتلی فرم (vitelliform lesion) به ترتیب زیر پیشرفت میکند. 1)
حاملان واریانتهای نادر ژن CFH (مانند p.Arg1210Cys) تمایل به بروز زودتر بیماری دارند. فعال شدن مزمن بیش از حد مسیر جایگزین کمپلمان به دلیل جهش ژن CFH تصور میشود که باعث تشکیل دروزن زودتر از AMD معمولی میشود. 1)
درمان هدفمند علیه مسیر کمپلمان
از آنجایی که ناهنجاری مسیر جایگزین کمپلمان ناشی از جهش ژن CFH اساس پاتولوژی است، ترکیبات هدفمند علیه مسیر کمپلمان به طور فعال در حال تحقیق هستند. از آنجایی که تجویز سیستمیک خطر عوارض جانبی بالایی دارد، تجویز موضعی (داخل چشمی) به عنوان یک رویکرد امیدوارکننده مورد توجه قرار گرفته است.
پیشبینی پیشآگهی با تصویربرداری چندوجهی
پیشرفت در تصویربرداری چندوجهی امکان شناسایی زودهنگام بیماران با خطر بالای عوارض را فراهم میکند. 1) طبقهبندی فنوتیپ (1 تا 3) برای پیشبینی پیشآگهی مفید است و فنوتیپهای 2 و 3 به عنوان گروههای پرخطر برای GA و MNV نیاز به پیگیری دقیقتری دارند. 1)
امکان پزشکی شخصیسازیشده
پیشرفت در تحلیل ژنتیکی امید به تحقق پزشکی شخصیسازیشده بر اساس واریانتهای ژنهای مرتبط با AMD از جمله ژن CFH را افزایش داده است. به ویژه، دارندگان واریانتهای نادر (مانند p.Arg1210Cys) میتوانند هدف غربالگری و مداخله زودهنگام باشند.