전형형(DOA)
증상: 양안성 서서히 진행하는 시력 저하.
유두 소견: 측두부 쐐기 모양 창백이 중심 소견입니다.
전신 증상: 시신경 위축만 있음.
시력: 80% 이상이 0.1 이상을 유지합니다.

상염색체 우성 시신경 위축증(Autosomal Dominant Optic Atrophy; ADOA)은 양안성 진행성 시신경 위축을 특징으로 하는 유전성 시신경병증입니다. OMIM 번호는 165500입니다. 가장 빈도가 높은 유전성 시신경병증이며, 유병률은 1:12,000~1:50,000으로 추정됩니다 2).
유전성 시신경병증은 크게 핵 유전자·멘델 유전 형식의 ADOA와 미토콘드리아 DNA 변이·모계 유전의 Leber 유전성 시신경병증(LHON)으로 나뉩니다. 상염색체 열성 유전 형식의 시신경 위축에는 Wolfram 증후군이 있습니다. ADOA와 LHON은 모두 미토콘드리아 기능 장애로 인한 망막 신경절 세포(RGC) 변성을 공통 병태로 하지만, 임상상과 유전적 원인은 다릅니다 6).
유병률은 1:12,000~1:50,000으로 추정되며, 유전성 시신경병증 중에서 가장 빈도가 높습니다 2). 영국에서 유전성 시신경병증 전체의 유병률은 약 1:25,000으로 보고되었습니다 6).
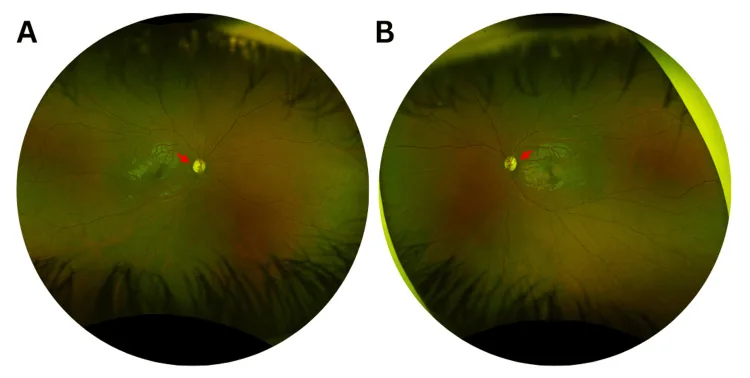
전형적인 발병은 인생의 첫 번째에서 두 번째 10년 사이입니다. 진행이 느리기 때문에 많은 환자들이 정확한 발병 시기를 특정할 수 없습니다.
있습니다. Tachibana 등(2025)의 보고에 따르면, 56세 시점에서 최대교정시력 0.8/0.6을 유지한 증례에서 OPA1의 새로운 변이가 확인되었습니다2). 침투율은 43~100%로 다양하며, 무증상 보인자에서도 OCT만으로 이상이 검출될 수 있습니다.
시신경 유두, 색각, 시야의 세 가지가 주요 소견입니다.
ADOA는 시신경 위축 외에 전신 이상을 동반하는 DOA 플러스(DOA plus) 표현형이 있습니다. 환자의 20~30%에서 난청, 말초신경병증, 근병증, 운동실조, 만성 진행성 외안근마비(CPEO) 등이 동반됩니다3).
전형형(DOA)
증상: 양안성 서서히 진행하는 시력 저하.
유두 소견: 측두부 쐐기 모양 창백이 중심 소견입니다.
전신 증상: 시신경 위축만 있음.
시력: 80% 이상이 0.1 이상을 유지합니다.
DOA 플러스
빈도: 환자의 20~30%에서 나타납니다3).
합병증: 난청, 말초신경병증, 근병증, 운동실조, CPEO 등.
중증형: 양대립유전자 OPA1 변이는 Behr 증후군(조기 발병, 중증 시력 장애, 운동실조, 경직)을 나타냅니다3).
ADOA의 60% 이상은 OPA1 유전자 변이가 원인입니다6). OPA1은 염색체 3q28-q29에 위치하며, 500개 이상의 병원성 변이가 확인되었습니다6). 일본에서는 c.2708_2711 delTTAG가 고빈도 변이로 알려져 있습니다.
OPA1 음성인 경우 다른 유전자 돌연변이를 검색해야 합니다. 주요 원인 유전자는 다음과 같습니다.
| 유전자 | 관련 질환 | 비고 |
|---|---|---|
| OPA1 | ADOA (전형형, DOA 플러스) | 전체의 60% 이상6) |
| AFG3L2 | 시신경 위축 12형 (OAT12), SCA28 | 유전성 시신경병증의 약 3%1) |
| OPA3 | 우성 시신경 위축 + 백내장·난청 (Costeff 증후군) | OMIM #258501 |
| WFS1 | Wolfram 증후군 유사 | OMIM #222370, #614296 |
| DNM1L | 시신경 위축 5형 (OPA5) | 미토콘드리아 분열 조절 |
Brodsky 등(2023)은 동아프리카(소말리)계 부녀에서 AFG3L2 유전자 c.1064C>T(p.Thr355Met) 돌연변이로 인한 시신경 위축 12형을 확인했습니다1). 2186명의 코호트 연구에서 유전성 시신경병증의 원인 유전자 상위 10위 안에 AFG3L2가 포함되었으며, 451명 중 14명(3%)을 차지했습니다.
있습니다. AFG3L2, OPA3, WFS1, DNM1L(OPA5) 등 여러 유전자가 확인되었습니다. 특히 AFG3L2는 유전성 시신경병증의 약 3%를 차지하며1), OPA1이 음성인 경우 엑솜/게놈 시퀀싱을 통한 포괄적 검색이 중요합니다.
학령기에 발견되는 양안성 원인 불명의 시력 발달 장애가 있으면 본 질환을 의심합니다. 유사한 증상의 가족력이 중요한 단서이지만, 불완전 침투로 인해 가족력이 없을 수도 있습니다.
Tachibana 등(2025)의 56세 남성 증례에서 HFA 24-2 백색 자극 시야는 정상이었으나 청-황 시야에서 민감도 저하가 검출되었습니다2). OCT에서 이측 RNFL 얇아짐, CFF는 30/31 Hz(정상 >39 Hz)로 감소를 보였습니다.
| 질환 | 발병 양상 | 유전 양식 | 감별 포인트 |
|---|---|---|---|
| LHON | 급성~아급성 | 모계 유전 | 젊은 남성 호발, 중증 |
| ADOA | 완만·잠행성 | 상염색체 우성 | 소아기, 양안 대칭 |
| 녹내장 | 완만 | 다인자 | 안압 상승, 시신경 유두 함몰 확대 |
| 압박성 시신경병증 | 완만~아급성 | 비유전성 | MRI에서 시교차부 병변 |
기타 감별: 중독성 시신경병증(에탐부톨 등), 영양 결핍성 시신경병증, 잠복 황반 이영양증, 원뿔세포 이영양증, 기능성 약시, 심인성 시각 장애.
확립된 효과적인 치료법은 없습니다. 저시력 관리와 환자 상담이 치료의 주축이 됩니다.
산화 스트레스 감소를 위해 다음이 제안되었으나, 어느 것도 표준 치료로 확립되지 않았습니다.
상염색체 우성 유전에 대한 설명과 이중 대립유전자 돌연변이로 인한 중증(Behr 증후군) 위험 정보 제공이 중요합니다 3).
시력 저하는 일반적으로 서서히 진행되며, LHON에 비해 경미한 경과를 보입니다. 80% 이상의 환자가 교정 시력 0.1 이상을 유지하지만, 교정 시력 0.1 이하로 떨어지는 경우도 있습니다. 발병이 서서히 진행되어 자각이 늦어지고, 검진에서 우연히 발견되기도 합니다. 확립된 치료법이 없으므로 정기적인 모니터링과 저시력 관리를 통한 장기 관리가 중요합니다.
현재 확립된 효과적인 치료법은 없습니다. 저시력 관리가 치료의 주축입니다. 이데베논은 시력 안정화 및 회복 가능성을 보여주는 보고가 있지만4)5), 표준 치료로 확립되지는 않았습니다. 연구 단계의 치료 접근법에 대해서는 [“최신 연구와 향후 전망” 항목](#7-최신의 연구와 향후 전망연구 단계의 보고)을 참조하십시오.
OPA1은 미토콘드리아 내막에 존재하는 다이내민 관련 GTPase입니다. 핵에서 합성된 후 미토콘드리아로 운반되어 다음과 같은 기능을 수행합니다6).
주요 병태 기전은 반수체 불충분입니다. 대부분의 OPA1 돌연변이는 번역의 조기 종결을 유발하여 OPA1 단백질 양이 부족해집니다6).
OPA1 단백질 감소 → 미토콘드리아 단편화 증가 및 재활용 항진3) → 미토콘드리아 대사 이상 및 산화적 인산화 장애 → 활성산소종(ROS) 상승 → RGC의 세포자멸사.
주로 유두황반섬유다발의 RGC가 변성되어 측두 시신경 위축으로 나타납니다.
AFG3L2는 미토콘드리아 기질 AAA 메탈로프로테아제(m-AAA)의 서브유닛을 코딩합니다1). SPG7(paraplegin)과 복합체를 형성하여 미토콘드리아 단백질의 가공, 성숙, 품질 관리를 ATP 의존적으로 수행합니다. 돌연변이는 OPA1과 유사하게 RGC 변성을 유발합니다1).
ASO 요법
표적: OPA1 pre-mRNA의 NMD(넌센스 매개 분해) 유도 엑손.
기전: NMD를 유도하는 엑손의 포함을 억제하여 돌연변이 비의존적 접근법으로 야생형 OPA1 번역을 강화 6).
현황: 3개의 ADOA 환자 유래 세포주에서 OPA1 단백질 증가 및 미토콘드리아 생체에너지 개선 확인 6). 유리체내 주사를 통한 정기적 반복 투여가 필요하며, 안내염 및 만성 포도막염 위험이 과제입니다.
유전자 치료
마우스 모델: OPA1 유전자 치료가 DOA 마우스 모델에서 RGC 소실을 예방 7).
아이소폼 최적화: 최적화된 OPA1 아이소폼 1 및 7이 미토콘드리아 기능 장애 모델에서 치료 효과를 나타냄 8).
현황: 전임상 단계.
유전자 편집
CRISPR-Cas9: iPSC에서 OPA1 c.1334G>A: p.R445H 돌연변이 교정이 미토콘드리아 항상성을 회복 9).
트랜스스플라이싱: mRNA 수준에서 병원성 돌연변이를 교정하는 접근법도 연구 중 6).
줄기세포: iPSC 유래 RGC를 이용한 시신경 재생이 전임상 연구에서 검토 중입니다6).
엑솜 시퀀싱의 반복적 재분석도 진단상 중요한 진전입니다. 유전학적 지식의 확장에 따라 이전 검사에서 음성이었던 데이터에서 새로운 진단이 얻어질 수 있습니다1).