HIT acuta
Conta piastrinica : ridotta
Test funzionale (SRA) : positivo
Test immunologico (ELISA) : positivo
Periodo a più alto rischio. Sospendere immediatamente tutta l’eparina e passare a un anticoagulante non eparinico.

La trombocitopenia indotta da eparina (HIT) è una reazione immuno-mediata alla somministrazione di eparina. Vengono prodotti anticorpi IgG contro il complesso formato dal fattore piastrinico 4 (PF4) e l’eparina, causando l’attivazione piastrinica. Di conseguenza, si verifica paradossalmente una riduzione del numero di piastrine mentre il sangue diventa ipercoagulabile.
La HIT è classificata in tipo I e II. La HIT di tipo I è una trombocitopenia transitoria che si risolve spontaneamente. La HIT di tipo II è mediata da anticorpi ed è una condizione grave con complicanze tromboemboliche. 1)
Le complicanze oftalmiche si verificano quando la trombosi o l’emorragia associata a HIT si estende al sistema vascolare oculare. È necessario un trattamento oftalmico parallelo alla gestione sistemica della HIT.
Nei pazienti trattati con UFH, l’incidenza è fino al 5%, mentre in quelli trattati con LMWH è circa 1/10. Dopo intervento chirurgico cardiaco, l’incidenza è dello 0,1-3%, più alta rispetto alla popolazione generale, e la mortalità può raggiungere il 10%. 2)
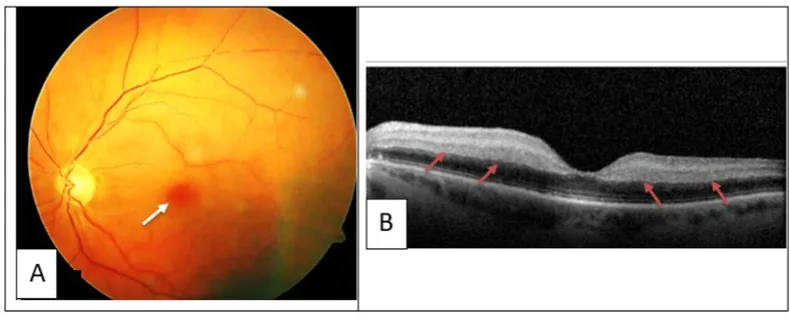
I sintomi oculari variano a seconda della sede del trombo o dell’emorragia.
La causa della HIT è una reazione immuno-mediata alla somministrazione di eparina. I principali fattori di rischio sono i seguenti.
Anche l’EBPM può causare TIE, ma l’incidenza è circa 1/10 rispetto all’ENF. Il rischio più basso non giustifica l’omissione del monitoraggio piastrinico.
La HIT è una diagnosi di esclusione. Viene sospettata in caso di trombosi e trombocitopenia che si verificano 5–14 giorni dopo la somministrazione di eparina, dopo aver escluso altre cause.
Il punteggio 4T è un punteggio di probabilità clinica basato su quattro criteri (trombocitopenia, tempistica, trombosi, altre cause). Ogni criterio viene valutato da 0 a 2 punti, e il totale classifica la probabilità.
| Punteggio totale | Classificazione di probabilità |
|---|---|
| 6–8 punti | Alta probabilità |
| 4–5 punti | Moderato |
| 0–3 punti | Bassa probabilità |
Il valore predittivo positivo del punteggio 4T è circa il 10% per un punteggio moderato di 4 punti e circa l’80% per un punteggio alto di 8 punti. 4)
Nei pazienti sottoposti a chirurgia cardiaca, una riduzione del 30-50% della conta piastrinica dopo CPB è normale, e un ulteriore pattern bifasico (trombocitopenia bifasica) è considerato caratteristico della HIT. 3)1)}
I principali metodi diagnostici sono il dosaggio degli anticorpi anti-PF4/eparina (anti-PF4 ELISA) e il test di rilascio della serotonina (SRA).
Le linee guida ASH raccomandano l’anti-PF4 ELISA per pazienti con punteggio 4T moderato o alto, e in caso di positività conferma con SRA. 2)
Rari casi di discordanza (anti-PF4 ELISA negativo e SRA positivo) sono stati riportati (16 su 8.546 casi, 0,2%) e, in caso di forte sospetto clinico di HIT, è necessario prestare attenzione alle discordanze dei test. 2)
La strategia di gestione della HIT varia a seconda della fase. 3)
HIT acuta
Conta piastrinica : ridotta
Test funzionale (SRA) : positivo
Test immunologico (ELISA) : positivo
Periodo a più alto rischio. Sospendere immediatamente tutta l’eparina e passare a un anticoagulante non eparinico.
HIT subacuta A
Conta piastrinica : normalizzata
Test funzionale (SRA) : positivo
Dosaggio immunologico (ELISA) : positivo
La conta piastrinica è normalizzata ma il test funzionale è positivo. La chirurgia cardiaca va rimandata se possibile.
HIT subacuto B
Conta piastrinica: normale
Test funzionale (SRA): negativo (negativizzazione mediana a 50 giorni)
Dosaggio immunologico (ELISA): positivo
L’esposizione intraoperatoria breve all’eparina è a basso rischio. Nel postoperatorio continuare a evitare l’eparina.
HIT remoto
Conta piastrinica: normale
Test funzionale (SRA): negativo
Dosaggio immunologico (ELISA): negativo (anticorpi PF4/H scompaiono in mediana a 85 giorni)
Stato che consente la somministrazione di eparina a breve termine in caso di riesposizione.
Nei pazienti con sintomi oculari secondari a HIT, è necessario eseguire un’anamnesi approfondita e un esame obiettivo per verificare la presenza di altri sintomi sistemici.
Si tratta di un punteggio che valuta la probabilità clinica di HIT secondo quattro criteri: grado di trombocitopenia, tempistica di insorgenza, presenza o assenza di trombosi ed esclusione di altre cause. Il punteggio totale va da 0 a 8, con 6 o più considerati ad alta probabilità.
Non appena la diagnosi di HIT viene posta o fortemente sospettata, è necessario eseguire immediatamente quanto segue.
Argatroban
Classificazione : Inibitore diretto della trombina
Emivita : 39-51 minuti (funzione epatica normale), prolungata fino a 181 minuti in caso di compromissione epatica
Metabolismo : Escrezione epatica. Vantaggioso nei pazienti con insufficienza renale.
Bivalirudina
Classificazione : Inibitore diretto della trombina
Emivita : 25 minuti (funzione renale normale o lievemente compromessa)
Dose per PCI : 0,75 mg/kg in bolo + 1,75 mg/kg/h
Dose per CEC : 1 mg/kg in bolo + 2,5 mg/kg/h (aggiungere 50 mg al liquido di priming) 3)
Le linee guida ASH 2018 raccomandano la bivalirudina per la PCI. In 52 casi di utilizzo in PCI, è stato riportato un successo procedurale del 98% e un’emorragia maggiore dell’1,9%. 3)
Nella HIT refrattaria con progressione della trombosi nonostante un’adeguata anticoagulazione non eparinica, considerare quanto segue. 5)
Se è necessario un intervento di chirurgia cardiaca in un paziente con HIT acuta/subacuta A, considerare le seguenti 3 opzioni. 3)
L’occlusione vascolare retinica e l’emorragia orbitaria vengono trattate oftalmologicamente in parallelo alla gestione sistemica della HIT.
Passare a un inibitore diretto della trombina come argatroban o bivalirudina. Entrambi inibiscono direttamente la trombina con un meccanismo diverso dall’eparina, quindi non sono influenzati dagli anticorpi HIT. La scelta del farmaco dipende dalla funzionalità epatica, renale e dalla situazione clinica.
Lo sviluppo della HIT procede attraverso le seguenti fasi.
Fase 1: Formazione del complesso e produzione di anticorpi
Il PF4 (fattore piastrinico 4) è una chemochina caricata positivamente derivata dai megacariociti, immagazzinata nei granuli alfa delle piastrine. Il PF4 forma complessi con l’eparan solfato caricato negativamente (GAG sulla superficie endoteliale vascolare) e il LPS (membrana esterna dei batteri Gram-negativi). Questi complessi funzionano come ‘segnali di pericolo’ consentendo la rapida produzione di anticorpi IgG.
Passaggio 2: Formazione del complesso PF4-eparina
La somministrazione di eparina porta alla formazione del complesso PF4-eparina. Poiché l’eparina ha una struttura molecolare simile a LPS e eparan solfato, le IgG preesistenti si legano ad essa.
Fase 3: Attivazione piastrinica e ipercoagulabilità
Il complesso IgG-PF4-eparina si lega al recettore FcγRII (FcγRIIa) sulle piastrine, attivandole. Viene avviata la via intrinseca della cascata coagulativa, causando contemporaneamente trombosi estesa e trombocitopenia da consumo piastrinico. Questa è l’essenza della patofisiologia «paradossale» della HIT.
Oltre al normale PF4, anticorpi diretti contro IL-8, protamina e NAP-2 vengono rilevati in meno dell’1% dei casi di sospetta HIT. 2) Inoltre, gli anticorpi anti-PF4 che attivano le piastrine anche in assenza di eparina (anticorpi HIT eparina-indipendenti) potrebbero essere coinvolti nella patogenesi della HIT refrattaria e della HIT autoimmune. 5)
Dopo CPB, fino al 50% dei pazienti presenta sieroconversione degli anticorpi PF4/H, ma solo l’1-2% sviluppa HIT clinica. 1) L’alta dose di UFH durante CPB, il rilascio di fattore tissutale e l’infiammazione sono considerati fattori che promuovono la produzione di anticorpi HIT. 3)
Si tratta di un preparato deglicosilato dell’anticorpo monoclonale murino IgG2b anti-PF4/H KKO. Bloccando il legame mediato da FcγRIIa, inibisce l’attivazione piastrinica e l’attivazione del complemento.
In modelli murini è stato riportato un miglioramento della trombocitopenia e una riduzione delle dimensioni del trombo. 5) Questa fase necessita di valutazione in futuri studi clinici.
È in fase di studio una strategia di ri-somministrazione di eparina durante la CEC utilizzando il cangrelor, un inibitore del P2Y12.
In una serie di 10 casi, la dose è stata aggiustata utilizzando VerifyNow P2Y12 PRU e non sono state riportate complicanze trombotiche.5) Non è stato ancora raggiunto un protocollo stabilito.
Sebbene l’efficacia della TPE sia riconosciuta, non è stato stabilito un protocollo standardizzato.
Una revisione sistematica (30 casi) riporta una media di 4 sedute di TPE con volume di scambio plasmatico di 1,3 PV, ma il livello di evidenza è basso e sono necessari futuri studi prospettici. 5)
Tugulan C, Chang DD, Bates MJ. Heparin-Induced Thrombocytopenia After Mitral Valve Replacement. Ochsner J. 2021;21(1):100-104.
Attah A, Peterson C, Jacobs M, et al. Anti-PF4 ELISA-Negative, SRA-Positive Heparin-Induced Thrombocytopenia. Hematol Rep. 2024;16(1):90-97.
Pishko AM, Cuker A. Heparin-induced thrombocytopenia and cardiovascular surgery. Hematology Am Soc Hematol Educ Program. 2021;2021(1):478-485.
Mele M, Iacoviello M, Casavecchia G, et al. Coronary thrombosis due to heparin-induced thrombocytopenia after percutaneous coronary intervention. Clin Case Rep. 2021;9(6):e04291.
Adeoye O, Zheng G, Onwuemene OA. Approaches to management of HIT in complex scenarios, including cardiac surgery. Hematology Am Soc Hematol Educ Program. 2024;2024(1):267-278.